إنتاج المواد الكيميائية من الغاز الطبيعي
أهمية الغاز الطبيعي
– يوجد الغاز الطبيعي في بعض الأحيان مصاحباً لزيت البترول، كما قد يوجد أحيانا في مكامن خاصة في باطن الأرض.
– يتكون الغاز الطبيعى أساساً من غاز الميثان، وهو يستخدم حالياً وقوداً وفي إدارة محطات توليد الكهرباء، وفى تسيير وسائل النقل والمواصلات، وكذلك في صناعة عديد من البتروكيميائيات.
– يمكن القول أن البترول قد حل محل الفحم كمصدر للطاقة ولكثير من الكيميائيات منذ نهاية القرن التاسع عشر. وأن الغاز الطبيعي قد بدأ يحل محل البترول فى هذا المجال فى نهاية القرن العشرين. وقد يصبح منافساً له تماما في خلال القرن الحادى والعشرين. وخاصة أن إحراق الغاز الطبيعي لا يسبب تلوثاً للبيئة والهواء، لخلوه من الكبريت.
– بلغ الاستهلاك العالمى من البترول عام 1988 نحو 3020 مليون طن، استخدم منه نحو 25% في إدارة محطات توليد الكهرباء ونحو 7% فقط في صناعة الكيميائيات، على حين استخدم الباقى منه وقوداً في المصانع وفي وسائل النقل وغيرها.
– كذلك بلغ الاستهلاك العالمى من الغاز الطبيعي عام 1988 نحو 1700 مليون طن، وهو قدر يصل إلى نحو نصف استهلاك البترول في نفس العام، واستخدم منه نحو 7% كذلك في صناعة الكيميائيات.
– ويتضح من ذلك أن هناك تقارباً كبيرا بين كل من كمية البترول وكمية الغاز المستخدمتين في صناعة الكيميائيات وهى تصل فى الحالة الأولى إلى نحو 200 مليون طن من البترول، وفى الحالة الثانية إلى نحو 120 مليون طن من الغاز.
إنتاج الغاز المائي من الغاز الطبيعي
– كانت أولى خطوات تحويل الغاز الطبيعى إلى كيميائيات عن طريق معاملته ببخار الماء عند درجة حرارة عالية وفى وجود حافز مثل فلز النيكل، فيتحول الميثان، وهو المكون الرئيسى للغاز الطبيعي إلى خليط من غازى الهدروجين وأول أكسيد الكربون، وهو خليط عرف باسم غاز التخليق Synthesis Gas أو الغاز المائي.
غاز التخليق CH4 + H2O → CO + 3H2
– يحتاج تفاعل غاز الميثان مع بخار الماء إلى درجة حرارة عالية لأنه تفاعل ماص للحرارة، ولذلك يمرر خليط البخار والميثان في أنبوبة لا يزيد قطرها على 10 سنتيمترات، وقد يصل طولها إلى نحو 15 متراً ويحتوى الفرن الواحد على مئات هذه الأنابيب المسخنة إلى نحو 900 سلزيوس وتحت ضغط 20 بار.
– يلاحظ أن هناك تفاعلاً ثانوياً آخر يحدث بين بخار الماء وبين أول أكسيد الكربون تحت هذه الظروف.
– يؤدى هذا التفاعل إلى تكوين مزيد من غاز الهدروجين الذى يستخدم في صناعات أخرى مثل صناعة النشادر من نتروجين
الهواء.
CO + H2O → CO2 + H2
إنتاج الكحول الميثيلي من الغاز المائي
– هكذا كانت أولى المواد الكيميائية التي صنعت من الغاز الطبيعي هي الكحول الميثيلي والنشادر.
CO + 2H2 → CH3OH
N2+ 3H2 → 2NH3
– يتم التفاعل بين غازى الهدروجين وأول أكسيد الكربون لتكوين الكحول المثيلي بطريقة سبق أن استخدمتها شركة الصناعات الكيميائية الإمبراطورية [ICI] عام 1971 ، وهى تتلخص في إمرار خليط الغازين على عامل مساعد من النحاس عند 250 سلزيوس وتحت ضغط 100 بار.
– وقد أجريت بعض التحسينات على هذه الطريقة في الولايات المتحدة الأمريكية، وذلك بإجراء التفاعل بين غازى الهدروجين وأول أكسيد الكربون في وسط سائل يسهل فيه انتقال الحرارة بكفاءة عالية واستخدم لذلك وسطاً من زيت معدنى لا يختلط بالكحول المثيلى الناتج في التفاعل، ويسهل بذلك فصله عن الوسط. وقد أقيمت وحدة تجريبية تعمل بهذا الأسلوب عام 1984 أنتجت نحو ثمانية أمتار مكعبة من الكحول المثيلي في اليوم.
– كان الكحول المثيلي يصنع قبل ذلك بطريقة التقطير الإتلافي للخشب وهي طريقة لا تعطى إلا كميات صغيرة منه لا يمكن أن تكفي لإضافتها إلى الكميات الهائلة من الجازولين التي تستهلك كل يوم.
– يضاف الكحول المثيلى إلى الجازولين بنسبة تصل إلى نحو 5 ٪ وتضاف معه بعض الكحولات الأخرى مثل الكحول البيوتيلى الثلاثي.
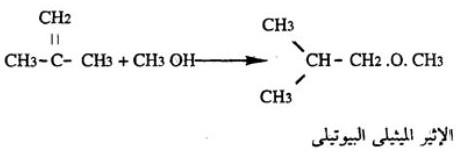
– كذلك يستخدم الكحول المثيلى فى صناعة الإثير المثيلى البيوتيلى، وهو يتكون بتفاعل الكحول المثيلي مع الأيزوبيوتيلين.
– وجدير بالذكر أن هذا الإثير يضاف كذلك للجازولين لتحسين خواصه وزيادة رقمه الأوكتاني.
– وقد بلغت كمية هذا الإثير التى تم إنتاجها عام 1944 نحو 20 مليوناً من الأطنان مما يدل على مقدار الحاجة إلى إنتاج كميات كبيرة من الكحول المثيلي، ويدل كذلك على الأهمية القصوى لصناعة البتروكيميائيات.
– كذلك تم تحضير حمض الخليك من الكحول المثيلي بتفاعله مع غاز أول أكسيد الكربون (تفاعل الكربنة) واستخدم فى هذا التفاعل حافز من فلز الكوبالت.
CH3OH + CO → CH3COOH
إنتاج الكحول الميثيلي مباشرة من الغاز الطبيعي
– وقد أجريت بعد ذلك عدة بحوث عام 1980 لتحويل الميثان مباشرة إلى كحول وغيره من الهدروكربونات دون الحاجة إلى المرور بخطوة غاز التخليق (الغاز المائي).
– وقد اكتشف کیمیائی بریطاني يدعى (تشات Chatt) عام 1960 أن فلز الروثينيوم له القدرة على كسر الرباط الكيميائي بين الكربون والهدروجين في جزيء الميثان، وذلك في درجات حرارة متوسطة نسبياً مع تكوين بعض المجموعات التالية:
CH4 + Ru → Ru-H , Ru-CH3 , Ru – CH2
– ثم تتفاعل هذه المجموعات بعد ذلك لتكوين بعض الأولفينات مثل الإثيلين كما أن بعضها يعطى الإيثان.
– كذلك تبين أن بعض الفلزات الأخرى مثل التيتانيوم والزركونيوم والهافنيوم لها نفس هذه القدرة.
– وقد طبقت طريقة مماثلة عام 1982 فى شركة يونيون كاربايد الأمريكية. ونجحت في تحويل الميثان صناعياً إلى الإيثان والإثيلين مباشرة. مما يعد نجاحاً كبير في تحويل الغاز الطبيعى إلى مركبات كيميائية دون المرور بخطوة غاز التخليق (الغاز المائي).
– كذلك تم تحويل الميثان إلى أسيتلين بإمراره فى قوس كهربائي مع الهواء.
– كما قامت شركة ديبون بإنتاج جليكول الإثيلين من الميثان عن طريق تحويله إلى غاز الإثيلين.
– الشكل التالي يوضح انتاج المواد الكيميائية المختلفة اعتماداً على الغاز الطبيعي كما يلي:
المراجع
– كتاب الصناعات الكيميائية – الجزء الثالث – البترول والكيمياويات، الصابون الممظفات الصناعية. ، المطاط – د/ أحمد مدحت عبد السلام – القاهرة – دار الفكر العربي – الطبعة الأولى 1997.
– أسس الكيمياء الصناعية – د/ محمد مجدى واصل – القاهرة – دار الفجر للنشر والتوزيع – الطبعة الأولى 2005.
– الكيمياء الصناعية – الجزء الثاني – تكنولوجيا الصناعات الكيميائية العضوية. – د/ طارق إسماعيل كاخيا – الطبعة الأولى.