معلومات هامة جداً عن غاز الأرجون Argon gas
ما هو غاز الأرجون Argon gas؟
– الأرجون عنصر من عناصر الجدول الدوري: العدد الذري = 18، العدد الكتلي = 40
– التوزيع الإلكتروني لعنصر الأرجون: 1S2 , 2S2 2P6 , 3S2 3P6
– الأرجون غاز أحادي الذرة، عديم اللون والرائحة، ذو وميض بنفسجي في حالة البلازما.
– الارجون خامل كيميائياً حيث ينتمي إلى فصيلة الغازات النبيلة، وهو أكثرها توفراً على سطح الأرض.
– للارجون التركيب الإلكتروني nS2 nP6 أي أن ذراته ذات تركيب إلكتروني مكتمل وهذا يعني أنه ثابت جداً.
– الارجون غير ميال للارتباط مع نفسه لتشكيل جزيئات ثنائية الذرة وحتى مع غيره من العناصر، وإنما يوجد بشكل ذرات منفصلة.
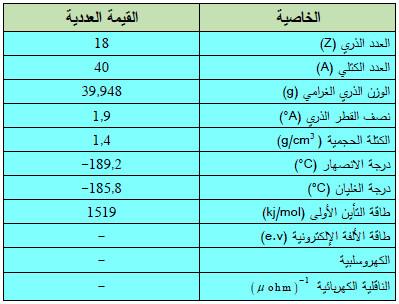
– الجدول التالي يوضح بعض الخواص العامة لعنصر الأرجون:
اكتشاف الأرجون ووجوده في الطبيعة Discovery of Argon
– اكتشف الارجون عام 1894م من قبل الكيميائي الإنجليزي (رامزي) (W. Ramsay) الذي وجده في الهواء بعد تقطيره الأكسجين والنتروجين منه.
– اشتق اسمه من اليونانية argos بمعنى خامل نظراً لما يتميز به خمول كيميائي.
– يعتبر الارجون الأكثر وجوداً في الجو من أي غاز نادر، حيث يقدر عند حجوم الهواء الحاوية حجماً واحداً منه بـ 107
تحضير غاز الأرجون Preparation of Argon
– يحضر الارجون بطريقة التقطير التجزيئي للهواء السائل.
– ويفصـل الارجون عن الأكسجين بتفاعل هذا الأكسجين مع الهيدروجين أو بإمرار المزيج على النحاس المسخن.
– وهو لا يتكثف خلال عملية التقطير لكنه يتجمع مع النتروجين الذي يحول إلى سائل ثم يتحد مع الماغنسيوم.
الخواص الكيميائية للأرجون Chemical properties of Argon
– إن التركيب الالكتروني للارجون من النوع nS2 nP6 حيث تكون طبقته الخارجيـة مشـبعـة الكترونياً.
– ومن هنا يمكن القول إن هذا الغاز لا يمكن أن يقوم بنشاطات كيميائية مع غيره من العناصـر إلا بصـورة محدودة جداً، وذلك عن طريق توسيع تركيبه الالكتروني بتحريض إلكترون أو أكثر من المدار (P) إلى المدار (d) الفارغ.
– لا يعرف حتى الآن مركبات كيميائية للارجون.
استخدامات غاز الأرجون Uses of Argon
(1) يستخدم الارجون في ملء:
- المصابيح الكهربائية
- مصابيح المذياع
- عدادات كايكر
(2) يستخدم كجو خامل في عمليات اللحام وخاصة في لحام الألمنيوم.
المراجع: دراسة كيميائية تحليلية مفصلة لعناصر الجدول الدوري / الأستاذ الدكتور حسن بوزيّان أستاذ بقسم الكيمياء بالمدرسة العليا للأساتذة / الجزء الأول / أبريل 2017 / الجزائر.