الموليبدنوم Molybdenum – الخواص الفيزيائية والكيميائية له
محتويات الموضوع
ما هو عنصر الموليبدنوم Molybdenum؟
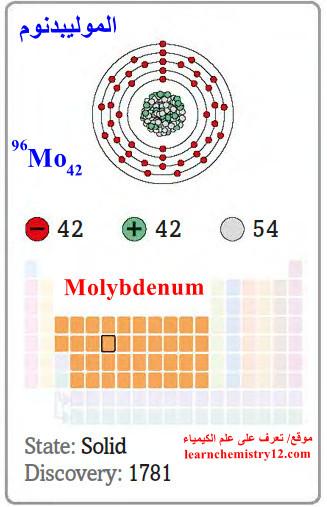
– الموليبدنوم Molybdenum هو عنصر من عناصر الجدول الدوري: العدد الذري = 42 ، العدد الكتلي = 96
– الرمز الكيميائي لعنصر الموليبدنوم يرمز له بالرمز: 96Mo42
– التوزيع الإلكتروني له: Kr]36 5s1, 4d5]
– الموليبدنوم معدن قابل لاطرق والسحب بشكل جيد في حالة نقاوته.
– ويكون هشاً سهل الكسر عند إدخال كمية ضئيلة من الشوائب بها.
– شكل هذا المعدن النقي رمادي فضي.
– وله نقطة انصهار عالية جدًا حوالي 2623 درجة مئوية (4753 درجة فهرنهايت).
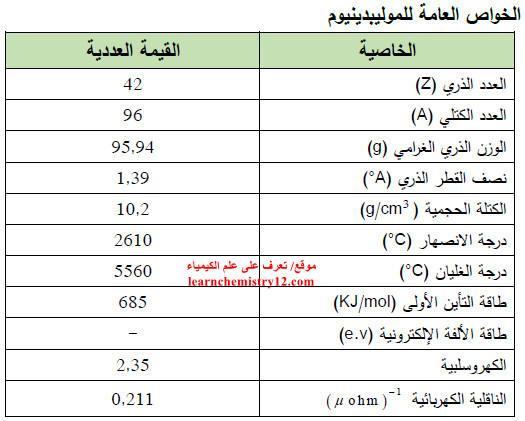
– الجدول التالي يوضح الخواص العامة لعنصر الموليبدنوم كما يلي:
اكتشافه ووجوده في الطبيعة Discovery of Molybdenum
– اكتشف من قبل Scheele في السويد سنة 1781م.
– اشتق اسمه من اليونانية molubdaina بمعنى الرصاص وهذا للتشابه الكبير بين العنصريين.
– كما يوجد الموليبدنيوم بنسبة 0.001% من وزن القشرة الأرضية.
– لا يوجد حراً في الطبيعة، بل يوجد على شكل فلزات ومن أهم فلزاته: مركب الموليبدنيت (MoS2).
– أخطأ عمال المناجم ذات مرة في فهم الموليبدينيت Molybdenite، وهو معدن داكن يحتوي على هذا المعدن، على أنه خام من الرصاص.
– هذا العنصر أكثر صلابة بكثير من الرصاص، لذلك من السهل التمييز بين هذين العنصرين عندما يكونان نقيين.
– الموليبدينيت Molybdenite معدن ناعم وزلِق وذو ملمس دهني، وهو خام الموليبدنوم الرئيسي.
طرق تحضير الموليبدنوم Preparation of Molybdenum
نحصل على أكسيد الموليبدنوم السداسي من حرق خام الموليبدنيت MoS2 كما في المعادلة:
MoS2 + 7/2 SO2 → 2SO2 ↑ + MoO3
وهو أكسيد متطاير لكننا نفضل إذابته بالأمونيا بغية تحويله إلى موليبدات الأمونيوم ثم بلورة الموليبدات من محلولها بعد الترشيح.
– نضيف حمضاً ما فيرسب أكسيد الموليبدات MoO3 مرة أخرى، ثم يذاب هذا الأكسيد بإضافة الأمونيوم له فنحصل على موليبدات أمونيوم من جديد، وبعد بلورتها نحصل على موليبدات نقية ذات تركيب محدد.
– ينصهر مسحوق معدن الموليبدنيوم بفرن كهربائي بجو من الأرجون Ar ليعطي معدن الموليبدنوم.
– يختزل الأكسيد MoO3 أحياناً الكربون، ولكن هذه الطريقة تؤدي إلى التلوث.
– هناك طريقة أخرى للحصول على معدن الموليبدنوم النقي وذلك بتحضير مركب كلوريد الموليبدنوم الثلاثي MoCl3 ، وبالتحليل الكهربائي نحصل على معدن الموليبدنوم.
الخواص الكيميائية لعنصر الموليبدنوم Chemical properties of Molybdenum
(1) التفاعل مع الأكسجين
– يتفاعل الموليبدنوم مع الأكسجين عند درجة الاحمرار أو تعطي أكاسيد كما في المعادلة:
Mo + 3/2 O2 → MoO3
(2) التفاعل مع الهالوجينات
– يتفاعل الموليبدنيوم مع البروم والكلور بالحرارة بينما يتفاعل مع الفلور عند درجة الحرارة العادية كما في المعادلة العامة الآتية:
Mo + X2 → MoX2
(3) تفاعلات أخرى
– لا يتأثر الموليبدنوم بالماء والهواء في الدرجة العادية من الحرارة.
– وتفاعلها مع اللامعادن لا يتم إلا عند الدرجات العالية من الحرارة.
– كما أن تفاعلها مع النيتروجين صعب.
استخدامات الموليبدنوم Uses of Molybdenum
(1) يضاف معدن الموليبدنوم للحديد لزيادة قوته وتحمله ضد تغير شكله عند ارتفاع درجة الحرارة
(2) كما يضاف المعدن إلى الفولاذ مع قليل من الكربون ليجعلاه مقاوماً للأكسدة اللاحقة.
(3) يدخل معدن الموليبدنيوم في تركيب الفولاذ القاسي المستخدم في صناعة الأدوات التي يستخدمها العمال في الصناعات المختلفة.
(4) كما تدخل في سبائك خاصة مع النيكل والكروم والتي تستخدم في صناعة المركبات الفضائية التي تتحمل ارتفاع الضغط والحرارة.
(5) علاوة على ذلك تستخدم موليبدات الرصاص في صناعة صبغات ثابتة ذات بريق أخاذ.
(6) تستخدم مركبات المولبيدنيوم القاسية جدًّا في تركيب قطع خاصة في جهاز صهر الزجاج.
(7) وفي صناعة الفولاذ المسقي ذي القساوة العالية وفي المواد البلاستيكية المقواة.
(8) يستخدم الموليبدنوم النقي بشكل أساسي في صناعة السبائك المقاومة للتآكل.
(9) تُستخدم سبائك الموليبدنيوم في أحدث تصميمات السيارات الخارقة، مثل Vencer Sarthe وهي مقاومة للصدأ.
(10) كما تستخدم في صناعة أطقم السقاطات Ratchet set لتجعلها صلبة بحيث لا تتلف بسهولة.
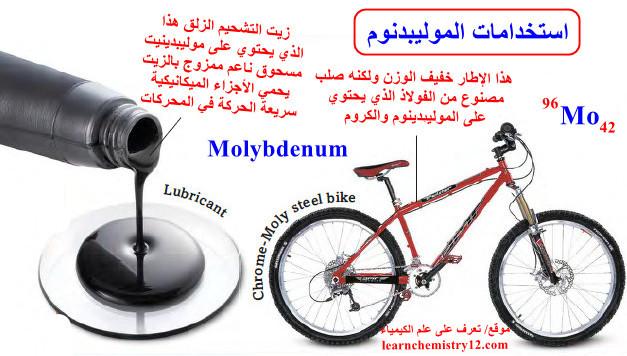
(11) يستخدم في صناعة إطارات خفيفة الوزن للدراجات ولكنها صلبة مصنوعة من الفولاذ الذي يحتوي على الموليبدنيوم والكروم.
(12) بالإضافة إلى ذلك تستخدم في صناعة زيوت التشحيم حيث يحتوي على موليبدينيت مسحوق ناعم ممزوج بالزيت، يحمي الأجزاء الميكانيكية سريعة الحركة في المحركات.
المراجع: دراسة كيميائية تحليلية مفصلة لعناصر الجدول الدوري / الأستاذ الدكتور حسن بوزيّان أستاذ بقسم الكيمياء بالمدرسة العليا للأساتذة / الجزء الأول / أبريل 2017 / الجزائر.