الجاليوم Gallium – الخواص الفيزيائية والكيميائية للجاليوم
محتويات الموضوع
ما هو عنصر الجاليوم Gallium؟
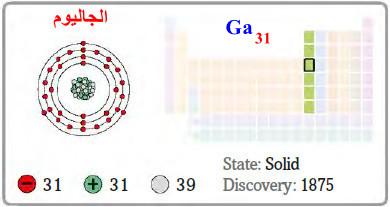
– الجاليوم أو الغاليوم هو عنصر من عناصر الجدول الدوري: العدد الذري = 31 ، العدد الكتلي = 70
– الرمز الكيميائي لعنصر الجاليـوم يرمز له بالرمز: 70Ga31
– التوزيع الإلكتروني له: Ar]18 4s2 3d10 4p1]
– الجاليوم عبارة عن معدن أبيض طري، فعال نسبياً.
– كما يتميز بأن مجال وجود حالته السائلة كبير.
– سائله لا يبلل الزجاج لذا يستخدم سائله في موازين الحرارة وحتى الآن ليس هناك تفسير مقبول لهذا المجال الواسع.
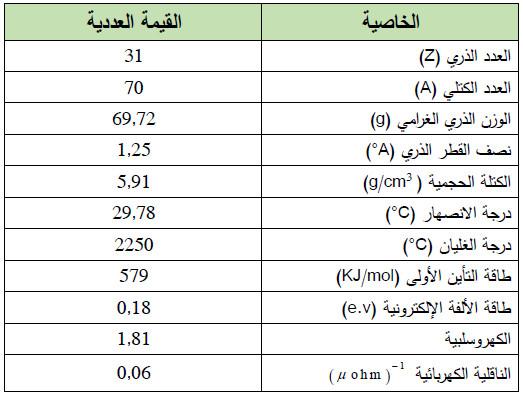
– الجدول التالي يوضح الخواص العامة لعنصر الجاليـوم كما يلي:
اكتشافه ووجوده في الطبيعة Discovery of Gallium
– اكتشف من طرف الكيميائي الفرنسي (ليكوك دي بوابودران) عام 1875م.
– وهو أول عنصر اكتشف بالتحليل الطيفي.
– اشتق اسمه من اللاتينية Galia وهو اسم فرنسا باللاتينية.
– كما يعتبر معدن الجاليوم من العناصر النادرة (أجزاء من المليون).
– بالإضافة إلى ذلك فأنه يوجد في فلزات الزنك والألومنيوم والجرمانيوم وأغنى هذه الفلزات لا يحوي أكثر من 1% من الجاليـوم.
طرق تحضير الجاليوم Preparation of Gallium
– يتم تحضير الجاليوم بالتحليل الكهربائي لمحاليل أملاحه المائية (وخاصة الكبريتات).
الخواص الكيميائية للجاليوم Chemical properties of Gallium
(1) التفاعل مع الهواء والأكسجين
– يعتبر الجاليوم غير فعال على عكس ما يتوقع، وذلك لتشكل طبقة رقيقة وكتيمة وشفافة من الأكسيد على سطحه، فهو ثابت في الهواء.
– عند التخلص من طبقة الأكسيد أو بالتسخين يتفاعل الجاليوم مع الأكسجين ويتشكل الأكسيد Ga2O3 كما بالمعادلة الآتية:
4Ga + 3O2 → 2Ga2O3
(2) التفاعل مع الهالوجينات
– يتفاعل الجاليوم مع الهالوجينات حتى في درجة الحرارة العادية عدا اليود، لتشكيل الهاليدات كما بالمعادلة الآتية:
2Ga + 3X2 → 2GaX3
(3) التفاعل مع الأحماض
– يكون تأثير الأحماض الممددة ضعيفاً في الجاليـوم ولكن بالتسخين يتأثر بسرعة وذلك لذوبان الطبقة Ga3+السطحية كما بالمعادلة الآتية::
2Ga + 6H+ → 2Ga3+ + 3H2
– يذوب الجاليوم في حمض الأزوت المركز والساخن وتتناقص درجة تأثره بالأحماض بازدياد نقاوته.
(4) التفاعل مع القواعد
– يتفاعل الجاليوم مع القواعد كما بالمعادلة الآتية:
2Ga + 6OH– → 2GaO33- + 3H2
(5) التفاعل مع العناصر الأخرى
يتفاعل الجاليـوم بالتسخين إلى درجات مرتفعة مع الفوسفور P والكبريت S والسيلينيوم Se كما بالمعادلات الآتية:
Ga + P → GaP
2Ga + 3S → Ga2S3
استخدامات الجاليوم Uses of Gallium
– يتسع تدريجياً مجال نشاط مركبات الجاليوم الكيميائية حيث يتم استخدمها كما يلي:
(1) تستخدم اليوم في الآلات الحاسبة وأجهزة الرادار والخلايا الحرارية والبطاريات الشمسية والأجهزة نصف الناقلة.
(2) يستخدم فى موازين الحرارة ( الثرمومتر) بدلاً من الزئبق.
(3) كما تستخدم في صناعة الصواريخ.
(4) تشترك في صنع أجهزة الليزر وتحضير المواد الوضاءة.
(5) يحصل المصباح الأحمر على لونه من مركبات الجاليـوم.
(6) تحتوى العربة Opportunity rover التى أرسلت لاستكشاف كوكب المريخ على ألواح شمسية من معدن الجاليـوم والزرنيخ.
(7) كما يلعب دور الوسيط في عدد كثير من العمليات الهامة في الكيمياء العضوية.
(8) تستعمل سبائك الجاليوم مع الأنديوم والقصدير كمواد تشحيم أثناء جمع القطع المصنوعة من الكوارتز والزجاج والخزف، وللصق هذه القطع مع بعضها تحت الضغط والملاحظ أن مدة استهلاك المحامل تزداد عندما يطلى سطحها بسبيكة من الجاليـوم والأنديوم.
(9) في الطب تستعمل مصابيح تعطي أشعة فوق بنفسجية، وكانت كاثودات هذه المصابيح تصنع من الزئبق، ولكن تبين فيما بعد أن سبيكة الألمنيوم مع الجاليـوم أفضل من الزئبق لهذا الغرض، فالضوء الذي تصدره هذه المصابيح أغنى بالأشعة المفيدة من ضوء المصابيح السابقة.
(10) للجاليوم قدرة جيدة على عكس الأشعة الضوئية، لهذا فقد جرب في صناعة المرايا ونجح، إذ تبين أن هذا الزجاج لا يتغبش ولا يكمد حتى في درجات الحرارة المرتفعة.
المراجع: دراسة كيميائية تحليلية مفصلة لعناصر الجدول الدوري / الأستاذ الدكتور حسن بوزيّان أستاذ بقسم الكيمياء بالمدرسة العليا للأساتذة / الجزء الأول / أبريل 2017 / الجزائر.