الروبيديوم Rubidium – الخواص الفيزيائية والكيميائية للروبيديوم
محتويات الموضوع
ما هو عنصر الروبيديوم Rubidium؟
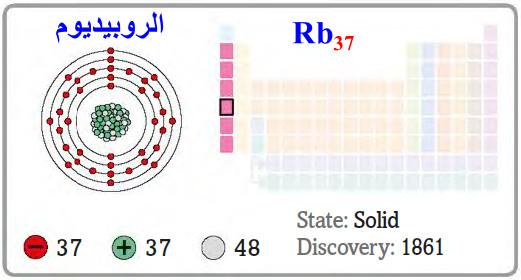
– الروبيديوم Rubidium هو عنصر من عناصر الجدول الدوري: العدد الذري = 37 ، العدد الكتلي = 85
– الرمز الكيميائي لعنصر الروبيديوم يرمز له بالرمز: 85Rb37
– التوزيع الإلكتروني له: Kr]36 5s1]
– الروبيديـوم معدن ذو مظهر فضي، طري يمكن قطعه بالسكين وذو كثافة منخفضة وناقليته الحرارية والكهربائية عالية.
– يحتوي هذا العنصر في طبقته الخارجية (التكافؤية) على إلكترون واحد في المدار (S) يمكن أن يفقده بسهولة ليعطي أيون موجب.
– كما تتميز مركبات هذا العنصر بكونها بلورية وأيونية.
– تتميز مركباته البسيطة أيضا بأنها غير ملونة إلا إذا كانت الشاردة السالبة ملونة.
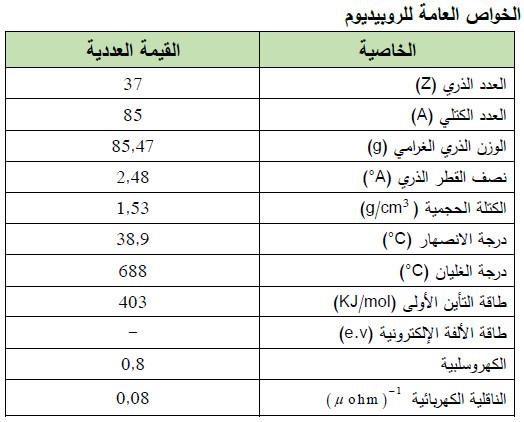
– الجدول التالي يوضح الخواص العامة لعنصر الروبيديوم كما يلي:
اكتشافه ووجوده في الطبيعة Discovery of Rubidium
– اكتشف الروبيديوم عام 1860م من طرف (كيرشوف) في ألمانيا وذلك خلال الدراسة الطيفية للعناصر الأساسية.
– اشتق اسمه من اللاتينية (rubidus) بمعنى (أحمر غامق) لأن لون طيفه أحمر غامق ويشير هذا أيضاَ إلى اللهب ذي اللون الأحمر الذي ينتجه عند الاحتراق.
– لشدة فعاليته، لا يوجد الروبيديوم بشكل حرفي الطبيعة، إلا أن مركباته واسعة الانتشار.
– لا يتركز الروبيديـوم في كثير من الأحيان في معادن معينة، ولكنه ينتشر بكميات صغيرة من خلال مجموعة واسعة من المعادن، مثل: Leucite وPollucite
– كما يتم الحصول على الروبيديـوم النقي بشكل أساسي من معدن Lepidolite
– يوجد معدن آخر يسمى Rubicline يحتوي على كمية كبيرة من الروبيديوم ولكنه نادر جدًا.
طرق تحضير الروبيديوم Preparation of Rubidium
– إن الفعالية العالية لعنصر الروبيديوم تخلق صعوبات جمة عند تحضيره بطريقة التحليل الكهربائي لمصهور أملاحه.
– لذا تستخدم طريقة اختزال الأكسيد أو الهيدروكسيد أو الكربونات أو الهاليدات أو الكبريتات أو الكرومات أو النترات لهذا المعدن بمعدن مختزل قوي مثل الصوديوم أو الكالسيوم أو المغنيزيوم أو الباريوم أو الألمنيوم… إلخ عند درجات مرتفعة.
– إلا أن الطريقة المفضلة لتحضيره هي مزيج كلوريده مع كمية زائدة من قطع الكالسيوم وتسخينها تحت الفراغ عند 700 – 800 مo وعندما يرجع الكلوريد تساق أبخرة المعدن تحت التفريغ إلى المبرد لتتكثف وتجمع.
الخواص الكيميائية لعنصر الروبيديوم Chemical properties of Rubidium
(1) التفاعل مع الهواء
يتفاعل الروبيديوم مع الهواء حيث عند تعرضه إلى الهواء الرطب يخبو بريقه بسرعة ويعطي في النهاية طبقة بيضاء، إذ يتشكل في البداية الهيدروكسيد ثم الكربونات.
(2) التفاعل مع الماء
يتفاعل Rb مع الماء ويكون التفاعل عنيفاً جداً وينصهر المعدن والحرارة المنتشرة تكون كافية لاشتعال الهيدروجين المتحرر، ويتشكل بالإضافة إلى الهيدروجين الهيدروكسيد كما بالمعادلة الآتية:
2Rb + 2H2O → 2RbOH + H2
(3) التفاعل مع الأكسجين
يتفاعل الروبيديوم مع الأكسجين بسهولة، وبوجود زيادة من الأكسجين يتشكل فوق أكسيد الروبيديوم RbO2 بالإضافة إلى الأكسيد العادية.
(4) التفاعل مع الهيدروجين
يتفاعل هذا المعدن مع الهيدروجين في المجال 300 – 400مo، ليشكل الهيدريد –Rb+H كما بالمعادلة الآتية:
2Rb + H2 → 2RbH
(5) التفاعل مع أشباه المعادن
يتفاعل الروبيديوم مع الكبريت والسيلينيوم، ويشكل الكبريتيدات والسليندات كما بالمعادلة الآتية:
2Rb + S → Rb2S
2Rb + Se → Rb2Se
أما مع الكربون فإنه يتفاعل عند الدرجات العالية من الحرارة ليشكل كربيدات.
(6) التفاعلات الأخرى
– يغير الروبيديـوم من المعادن الأساسية والتي تعتبر أساساً قوية جداً لذلك يستطيع أن يحرر الهيدروجين حتى من الأمونيا.
– وهذا يتم إما بتفاعل Rb مع غاز النشادر عند الدرجات العالية أو بين Rb و سائل الأمونيا بوجود وسيط وفي كلتا الحالتين يتشكل الأميد كما بالمعادلة الآتية:
2Rb + 2NH3 → 2RbNH2 + H2
استخدامات الروبيديوم Uses of Rubidium
(1) يستخدم في صنع الخلايا الكهروضوئية وأنابيب التفريغ.
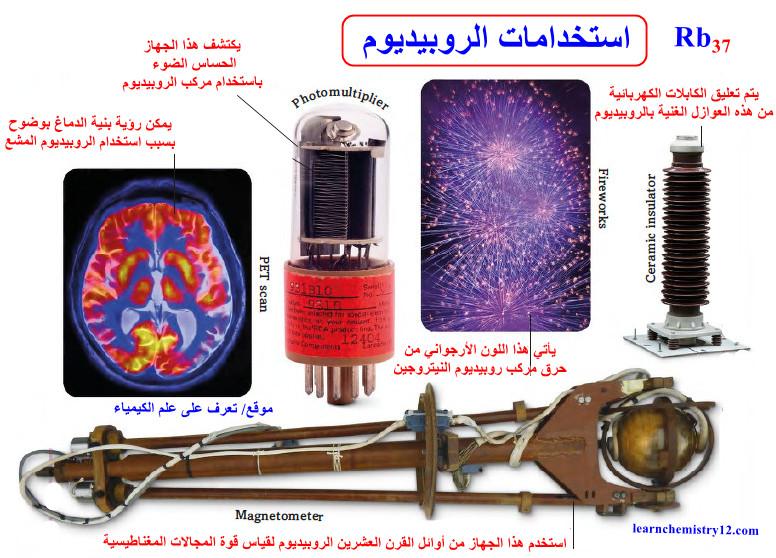
(2) يأتي هذا اللون الأرجواني من حرق مركب روبيديـوم النيتروجين.
(3) استخدم جهاز Magnetometer من أوائل القرن العشرين الروبيديوم لقياس قوة المجالات المغناطيسية
(4) كما تعتبر ذرات الروبيديوم حساسة للضوء ويمكن استخدامها في الخلايا الكهروضوئية (الأجهزة التي تحول الطاقة الضوئية إلى كهرباء) ومعدات الرؤية الليلية night-vision equipment
(5) بالإضافة إلى ذلك فأن هذا العنصر له أشكال مشعة يمكن استخدامها لقياس عمر الصخور.
(6) عند حقن الروبيديوم في جسم المريض، يستهدف الأورام التي تظهر بوضوح في التصوير المقطعي بالإصدار البوزيتروني PET scans
(7) كما يستخدم الروبيديوم أيضًا في الإلكترونيات الحساسة للضوء والتي تسمى المضاعفات الضوئية photomultipliers
(8) وفي صنع عوازل للكابلات عالية الجهد insulators وبعض أنواع الزجاج الخاصة.
المراجع: دراسة كيميائية تحليلية مفصلة لعناصر الجدول الدوري / الأستاذ الدكتور حسن بوزيّان أستاذ بقسم الكيمياء بالمدرسة العليا للأساتذة / الجزء الأول / أبريل 2017 / الجزائر.