الكيمياء العامةعناصر الجدول الدورى
معلومات هامة جداً عن عنصر النيون Neon

أولاً/ ما هو عنصر النيون؟ What is Neon element
– النيون عنصر من عناصر الجدول الدوري ينتمي إلى مجموعة الغازات النبيلة.
– العدد الذري له = 10 ، والعدد الكتلي = 20
– يرمز له بالرمز (Ne)
– التوزيع الإلكتروني لعنصر النيون 1S2 , 2S2 2P6
– (Ne) هو عنصر كيميائي من الغازات النبيلة التي تتصف بأنها إذا ما أضيفت إلى مصباح ضوئي زادت من توهجه وأعطته بريقاً مختلفاً.

– (Ne) هو عبارة عن غاز عديم اللّون ذو وميض أحمر برتقالي في حالة البلازما.
– للنيون التركيب الإلكتروني nS2 nP6 أي أنّ ذراته ذات تركيب إلكتروني مكتمل وهذا يعني أنّه ثابت جدا ، وهو غير ميّال للارتباط مع نفسه لتشكيل جزيئات ثنائية وحتى مع غيره من العناصر وانما يوجد بشكل ذرات منفصلة.
– الجدول التالي يوضح بعض الخواص العامة لعنصر النيون:
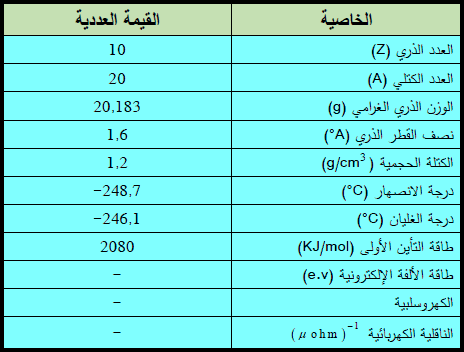
ثانياً/ اكتشاف النيون ووجوده في الطبيعة Discovery of Neon
– اكتشف (Ne) من قبل رامزى وترافرس Travers عام 1898م وعزلاه من تمييع الأرغون الناتج عن الهواء ومن ثم بالتقطير الجزئي للسائل الناتج.
– اشتق النيون اسمه من اللاتينية من كلمة (Neos) بمعنى (جديد).
– (Ne) أكثف من الهيدروجين بحوالي عشر مرات.
– يتألف (Ne) من مزيج من ثلاثة نظائر ثابتة وهي: Ne20, Ne21, Ne22 . وله أربعة نظائر مشعة وهي: Ne18, Ne19, Ne23 .Ne24
– يقدّر عدد حجوم الهواء الحاوية حجماً واحداً من غاز النيون بـــ 55000 . أما نسبته المئوية الحجمية في الهواء فتقدر 1.82 × 10-3%
ثالثاً/ تحضير عنصر النيون Preparation of Neon
يحضر (Ne) حالياً من الهواء الجوي بتمييعه وتقطيره جزئياً.
رابعاً/ الخواص الكيميائية لعنصر النيون Chemical properties of Neon
– إنّ التركيب الإلكتروني لغاز النيون من النوع nS2 nP6 حيث تكون طبقته الخارجية مشبعة إلكترونياً، ومن هنا يمكن القول إن هذا الغاز لا يمكن بتركيبه الإلكتروني هذا أن يقوم بنشاطات كيميائية مع غيره من العناصر إلاّ بصورة محدودة جداً، وذلك عن طريق توسيع تركيبه الإلكتروني بتحريض إلكترون أو أكثر من المدار p إلي المدار (d) الفارغ.
– لا يعرف حتى الآن مركبات كيميائية للنيون.
خامساً/ استخدامات عنصر النيون Uses of Neon
(1) يستخدم (Ne) في أنابيب الإفراغ وخاصة لأغراض الإعلان ومصابيح الشوارع، وذلك لأنه إذا أفرغ عند الضغط 2mmHg تألق بلون برتقالي محمر مميز قادر على اختراق الضباب.
(2) يعطي (Ne) لوناً أزرق أو أخضر عند مزجه مع كمية قليلة من بخار.
(3) يستخدم (Ne) مع مركباته في إنتاج اليورانيوم.
المراجع: دراسة كيميائية تحليلية مفصلة لعناصر الجدول الدوري / الأستاذ الدكتور حسن بوزيّان أستاذ بقسم الكيمياء بالمدرسة العليا للأساتذة / الجزء الأول / أبريل 2017 / الجزائر.







لو سمحت ابا مقدمه بحث عن النيون وخاتمه للبحث ارجوا المساعده
آسف واللهى هذا الموضوع فقط هو المتوفر لدينا
شكراً على المعلومات جزاك الله خيراً