القصدير Tin – الخواص الفيزيائية والكيميائية للقصدير
محتويات الموضوع
ما هو عنصر القصدير Tin؟
– القصدير tin هو عنصر من عناصر الجدول الدوري: العدد الذري = 50 ، العدد الكتلي = 119
– الرمز الكيميائي لعنصر القصدير يرمز له بالرمز: 119Sn50
– التوزيع الإلكتروني له: Kr]36 5s2 4d10 5p2]
– القصديـر النقي معدن أبيض فضي ذو ليونة عظيمة تكسبه قابلية كبيرة للطرق والسحب والتصفيح.
– يستعمل نظرًا لقدرته على مقاومة التآكل في وقاية الفولاذ.
– هناك أنواع أخرى من القصديـر كما يلي:
- قصديـر لونه رمادي ذو شكل لا معدني تشبه بنيته بنية الماس.
- قصديـر منشوري أقسى من الشكلين السابقين وهو قابل للكسر بسرعة.
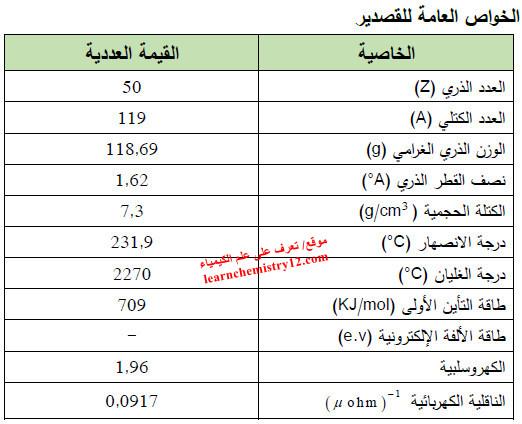
– الجدول التالي يوضح الخواص العامة لعنصر القصدير كما يلي:
اكتشافه ووجوده في الطبيعة Discovery of Tin
– كان القصدير من أوائل المعادن التي استخدمها البشر منذ 5000 عام مضت.
– كان القصديـر يخلط مع النحاس لصنع البرونز ، وهو سبيكة أقوى من أي معدن نقي
– مصدر اسمه من اللغة اللاتينية (Stannum) وتعني الحديد الأبيض.
– يشكل القصدير 0.001% من القشرة الأرضية، لذلك فإن كمية القصدير المستخدمة من المناجم صغيرة جدًا إذا ما قورنت بالفلزات الأخرى.
– أهم خاماته: أكاسيد SnO2، الحجر القصديري، كباريت كما في الستانيت : CuS, FeS, SnS2
طرق تحضير القصدير Preparation of Tin
– يعتبر الحجر القصديـري (كاستريت Cassiterite) SnO2 من أهم فلزات القصديـر في الطبيعة.
– يحضر القصدير باختزال هذا الفلز في فرن منقلب اللهب بواسطة الكربون كما يلي:
SnO2 + 2C → Sn + 2CO
– وقبل هذه العملية يسحق الفلز ويغسل بالماء، ثم يشوى حيث يخلص من أكاسيد الزرنيخ والكبريت.
الخواص الكيميائية لعنصر القصدير Chemical properties of Tin
(1) التفاعل مع الأكسجين
– القصديـر العادي لا يتأثر بالهواء في درجة الحرارة العادية.
– وبالتسخين يتشكل الأكسيد SnO2 كما بالمعادلة التالية:
Sn + O2 → SnO2
(2) التفاعل مع الهالوجينات
– يتفاعل القصديـر بسهولة مع الهالوجينات تحت تأثير الحرارة كما بالمعادلة التالية:
Sn + 2X2 → SnX4
(3) التفاعل مع الأحماض
– يتفاعل القصديـر مع حمض كلور الماء الساخن ويشكل كلوريد القصديـر كما بالمعادلة التالية:
Sn + 4HCl → SnCl4 + 2H2
– ومع الأحماض المؤكسدة المركزة والساخنة يشكل الأكسيد كما بالمعادلة التالية:
3Sn + 4HNO3 → 3SnO2 + 4NO + 2H2O
(4) التفاعل مع القواعد
– يتمتع القصديـر بصفات مذبذبة، حيث يذوب في القواعد المركزة ويشكل شاردة القصديرات كما بالمعادلة التالية:
Sn + 2OH– + 4H2O → SnO22- + H2O
(5) التفاعل مع الكبريت
– يتفاعل القصديـر مع الكبريت بالتسخين، مشكلاً كبريتيد كما بالمعادلة التالية:
Sn + 2S → SnS2
استخدامات القصدير Uses of Tin
– يستعمل القصدير في طلاء الحديد وفي صنع الخلائط المعدنية ليجعلها أكثر مقاومة للتآكل.
– كما يستخدم أيضاً في صنع صفائح القصدير الرقيقة المستخدمة في تغليف المعجنات والأطعمة.
– يستخدم كلوريد القصديـر لصبغ الحرير.
– يستمر استخدام هذا المعدن في مجموعة متنوعة من السبائك الصلبة، بما في ذلك القصديـر واللحام الناعم والبرونز.
تأثير القصدير على جسم الإنسان
– يعتبر القصدير من أخطر المعادن تأثيرًا على صحة الإنسان.
– ومن أخطر هذه المركبات العضوية Triethyltin والتي يمتصها جسم الإنسان من خلال الطعام والهواء والجلد وتسبب أعراض حادة وعلى مدى الطويل ومنها كما يلي:
الأعراض الحادة:
- احتياج في العين والجلد
- عدم القدرة على التنفس
- آلام المعدة
- صداع
- إحساس بالمرض والدوار.
الأعراض على مدى الطويل:
- الاكتئاب.
- ضمور في خلايا الكبد.
- نقص خلايا الدم الحمراء.
المراجع: دراسة كيميائية تحليلية مفصلة لعناصر الجدول الدوري / الأستاذ الدكتور حسن بوزيّان أستاذ بقسم الكيمياء بالمدرسة العليا للأساتذة / الجزء الأول / أبريل 2017 / الجزائر.