اللوتيتيوم Lutetium – الخواص الفيزيائية والكيميائية
محتويات الموضوع
ما هو عنصر اللوتيتيوم Lutetium؟
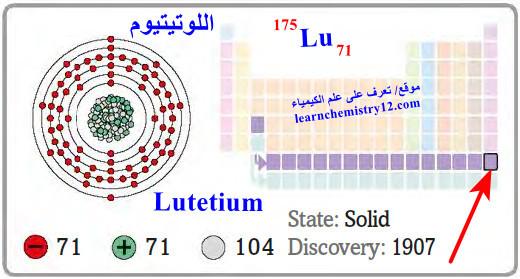
– اللوتيتيوم Lutetium هو عنصر من عناصر الجدول الدوري: العدد الذري = 71، العدد الكتلي = 175
– الرمز الكيميائي لعنصر اللوتيتيوم يرمز له بالرمز: 175Lu71
– التوزيع الإلكتروني له: Xe]54 6s2 4f14 5d1]
– اللوتيتيوم هو عنصر فلزي من عناصر المجموعة الأرضية النادرة، وغالباً ما يقع اللوتيتيوم مع الإيتريوم.
– عند التقيد بقواعد المستويات الفرعية للجدول الدوري والسلاسل الكيميائية، فإنه يتم وصف اللوتيتيوم كعنصر انتقالي، لكنه عموماً يوصف على أنه من اللانثانيدات وذلك حسب الإيوباك IUPAC
– هذا العنصر هو أصلب وأكثف معدن من اللانثانيدات.
– كان اللوتيتيوم آخر المعادن الأرضية النادرة التي تم اكتشافها.
– وهو أيضًا العضو الأخير في اللانثانيدات.
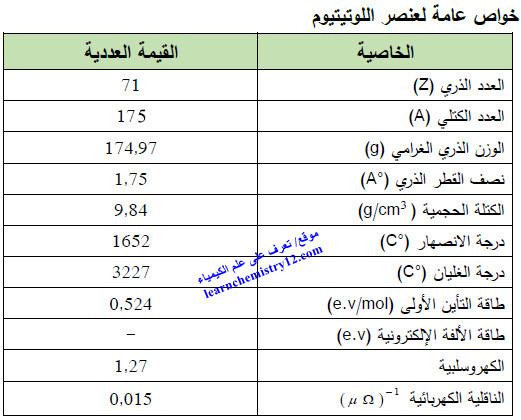
– الجدول التالي يوضح الخواص العامة لعنصر اللوتيتيوم كما يلي:
اكتشافه ووجوده في الطبيعة Discovery of Lutetium
– تعني كلمة لوتيتيا باللاتينية (باريس) تم اكتشافه مستقلاً في عام 1907م بواسطة العالم الفرنسي جورج أوربان وأحد علماء المعادن الأستراليين البارون كارل أوير فون ويلسباخ.
– ووجد كلاهما اللوتيتيوم كتلوث في معدن اليتربيا والذي كان يظن أنه يحتوي على العنصر إيتربيوم من الكيميائي جين كارليس جاليسارد ماريناك وآخرون.
– تم وصف فصل اللوتيتيوم من ايتريوم ماريناك عن طريق أوربان وبالتالي كان له شرف الاكتشاف.
– اختار للعنصر نيو إيتريوم ولوتيكيوم كأسماء له، ولكن تم إرجاع الاسم نيو إيتريوم إلى عنصر الإيتريوم في عام 1949م وتم تسمية العنصر باللوتيتيوم.
– يتواجد مع تقريباً كل الفلزات الأرضية النادرة ولكن لا يتواجد بمفرده، ويصعب للغاية فصل اللوتيتيـوم من العناصر الأخرى.
– هو أقل العناصر وفرة على الإطلاق وبالتالي، هو أحد أغلى الفلزات، وتبلغ قيمته 6 مرات تقريباً مثل الذهب.
تحضير اللوتيتيوم Preparation of Lutetium
– أهم مصادر اللوتيتيوم هو المعدن الأرضي النادر للفوسفات المونازايت: ( Ce, La, PO4)، ويحتوى على %0.003 من العنصر
– فلز اللوتيتيوم النقي تم عزله حديثاً وهو صعب للغاية في تحضيره (وهو أحد وأغلى العناصر الأرضية النادرة).
– يتم فصله من العناصر الأرضية النادرة الأخرى بواسطة التبادل الأيوني.
– ثم يتم الحصول عليه في شكله العنصري باختزال LuCl3 المائي أو LuF3 بواسطة فلز أو فلز قلوي ترابي.
مركبات اللوتيتيوم Lutetium Compound
(1) ثلاثي كلوريد اللوتيتيوم LuCl3
– هو مركب كيميائي يتكون من الكلور واللوتيتيوم.
– وهو عبارة عن بلورات استرطابية بيضاء عند تسخينها مع معدن الكالسيوم تنتج لنا معدن اللوتيتيـوم النقي كما بالتفاعل التالي:
2LuCl3 + 3Ca → 2Lu + 3CaCl2
(2) مركب جرانيت الومنيوم اللوتيتيـوم Al5Lu3O12
– يسمى هذا المركب بالإنجليزية Lutetium aluminum garnet.
– كما يتم استخدامها كمادة الانكسار عالية في العدسات.
– كما يمكن استخدامها كمخدر مع السيريوم.
– علاوة على ذلك فأن مظهرها المتلألئ يجعل منه مرشحاً لارتفاع طاقة الفوتون.
(3) ثلاثي أكسيد اللوتيتيوم Lu2O3
– عبارة عن مادة صلبة بيضاء، تستخدم أحياناً في إعداد النظارات الخاصة. ويسمى أيضاً lutecia، أو اللوتيسيا.
– يستخدم في المواد الفائقة التوصيل وهي مادة خام مهمة ليزر البلورات.
– كما أن لديها استخدامات متخصصة في السيراميك والزجاج، وأشعة الليزر.
– كما يستخدم كمحفز في الكسير، الألكلة، والهدرجة والبلمرة.
(4) مركبات أخرى
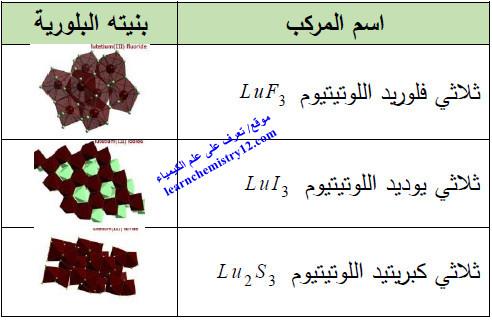
كما يوجد مركبات أخرى مشهورة لهذا العنصر كما بالجدول التالي:
الخواص الكيميائية لعنصر اللوتيتيوم Chemical properties of Lutetium
– اللوتيتيوم في شكله النقي شديد التفاعل ويشتعل بسهولة.
(1) التفاعل مع الهواء
– اللوتيتيـوم يتشوه ببطء في الهواء ويحترق بسهولة لتشكيل ثلاثي أكسيد اللوتيتيـوم ذو الصيغة Lu2O3 كما بالتفاعل التالي:
4Lu + 3O2 → 2Lu2O3
(2) التفاعل مع الماء
– اللوتيتيـوم يتفاعل ببطء مع الماء البارد وبسرعة مع الماء الساخن لتشكيل هيدروكسيد اللوتيتيـوم Lu(OH)3 وغاز الهيدروجين H2 كما بالتفاعل التالي:
2Lu (s) + 6H2O (g) → 2Lu(OH)3 (aq) + 3H2 (g)
(3) التفاعل مع الهالوجينات
– اللوتيتيـوم يتفاعل مع كل الهالوجينات لتشكيل هاليداته، كما بالتفاعلات التالية:
(أبيض) 2Lu (s) + 3F2 (g) → 2 LuF3 (s)
(أبيض) 2Lu (s) + 3Cl2 (g) → 2 LuCl3 (s)
– كما يتفاعل أيضاً بنفس الطريقة مع البروم واليود:
(أبيض) 2Lu (s) + 3Br2 (g) → 2 LuBr3 (s)
(أبيض) 2Lu (s) + 3I2 (g) → 2 LuI3 (s)
(4) التفاعل مع الأحماض
– اللوتيتيوم يذوب بسهولة في حمض الكبريتيك لتشكيل محاليل تحتوي على أيونه الثلاثي كما بالتفاعل التالي:
2Lu (s) + 3H2SO4 (aq) → 2Lu3+ (aq) + 3SO42- (aq) + 3H2 (g)
استخدامات اللوتيتيوم Uses of Lutetium
(1) يستخدم في سبائك المعادن كحافز في بعض العمليات.
(2) كما يتم استخدام جرانيت اللوتيتيـوم ألومنيوم Al5Lu3O12 كعدسة في الطباعة الحجرية المغموسة ذات معامل الانكسار العالي.
(3) يستخدم كحفاز في عمليات تكرير البترول في المصافي ويمكن أن يستخدم أيضاً في الألكلة، والهدرجة، والبلمرة.
تأثير اللوتيتيوم على الإنسان والبيئة
– مثل الفلزات الأرضية النادرة الأخرى، ينظر للوتيتيوم على أن له سمية منخفضة، ولكن يجب التعامل معه بحرص وخاصة مركباته.
– لتراب الفلز خطورة من ناحية الاشتعال والانفجار، ولا يلعب اللوتيتيوم أي دور حيوي في جسم الإنسان ولكن يظن أنه يساعد في حث عملية الأيض.
– المراجع:
- دراسة كيميائية تحليلية مفصلة لعناصر الجدول الدوري / الأستاذ الدكتور حسن بوزيّان أستاذ بقسم الكيمياء بالمدرسة العليا للأساتذة / الجزء الأول / أبريل 2017 / الجزائر.
- The periodic table book – A visual Encyclopedia of elements written by Tom Jackson – consultant Jack Challoner – Great Britain 2017