المخطط العملي للكشف عن الشقوق القاعدية (Basic radicals (Cations
المخطط العملي للكشف عن الشقوق القاعدية في الأملاح البسيطة (Scheme for identification of basic radicals (Cation
الكشف عن الشقوق القاعدية في الأملاح البسيطة
Identification of Basic radical (Cation) in sample salts
الشق Radical
عبارة عن ذرة أو مجموعة من الذرات تسلك وكأنها ذرة واحدة وإذا كان يحمل شحنة سالبة يسمى شق حامضي (أنيون (anion وإذا كان يحمل شحنة موجبة يسمى شق قاعدي (كاتيون).
- شق بسيط : يتكون من ذرة واحدة مثل : K+ , Cl– , Na+
- شق مركب: يتكون من مجموعة من الذرات ويسمى مجموعة ذرية مثل : NH4+ , NO3– , SO42-
تحضير محلول الملح
– يكشف عن الشقوق الحامضية أو القاعدية في المحلول لأنها لا تتفاعل إلا إذا كانت على هيئة أيونات ، لذلك لابد من تحويل الأملاح الصلبة إلى محاليل بإذابتها في مذيب مناسب وذلك بجزء من الملح الصلب مع حجم مناسب من المذيب.
– لكن السؤال الذي يطرح نفسه هو: ما كمية أو كتلة العينة التي يجب أخذها لإجراء عملية التحليل والكشف عن الأنيونات الموجودة فيها؟
– وهنا يمكن القول يمنع أخذ كمية كبيرة من المادة، لأن هذا قد يؤدي إلى الحصول على معلومات مشوهة عن خصائص العينة ، إذا كانت تذوب في هذا المذيب أو ذاك. وكذلك يجب أن لا تكون الكمية المأخوذة من المادة قليلة جداً، لأنه في هذه الحالة يصبح من الصعب الكشف عن الأيونات الموجودة في العينة.
– لذلك يجب أن الوزن المثالي للعينة المدروسة من مرتبة 25 mg ، والذي يؤدي بعد إذابة العينة إلى زيادة حجم المحلول بمقدار 1 ml تقريباً.
– وتستخدم هذه المذيبات حسب الترتيب الآتي:
- الماء البارد
- الماء الساخن
- حمض الهيدروكلوريك المخفف البارد أو الساخن
- حمـض الهيدروكلوريك المركز البارد أو الساخن
- حمض النيتريك المخفف البارد أو الساخن
- حمض النيتريك المركز البارد أو الساخن
- الماء الملكي ويتكون من ثلاث حجوم من حمض الهيدروكلوريك المركز + حجم واحد من حمض النيتريك المركز مع التسخين الحذر.
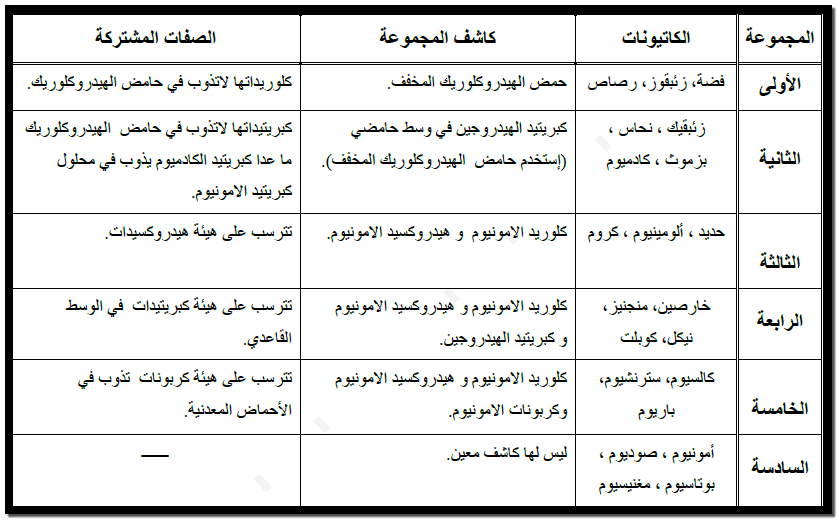
توزيع الكاتيونات Cations distribution
– صنفت الكاتيونات الشائعة إلى ست مجموعات وكل مجموعة تمتاز بكاشفها الخاص بها ، والذي يرسب كل الأيونات التي تحتويها. ويسمى هذا الكاشف بكاشف المجموعة Group reagent
– أما الكواشف التي تستعمل أثناء التجارب التأكيدية التي تجرى للتعرف عن أيونات مجموعة ما فهي تسمى بالكواشف النوعية.
– ويجب الملاحظة أن كاتيونات كل مجموعة لا تتفاعل مع كواشف المجموعة السابقة. ولكن يمكن أن تتفاعل مع كواشف المجموعات التالية.
– ويجب إتباع خطوات الكشف كما هو موضح هنا لكي تتم عملية الكشف بنجاح.
ملاحظات هامة على خطوات الكشف عن كاتيونات الشقوق القاعدية
(1) قبل الكشف عن كاتيونات أي مجموعة لابد من تنظيف أنابيب الاختبار وهذا باستعمال فرشة تنظيف الأنابيب المستعملة في نهاية كل حصص العملي.
(2) يجب الكشف عن المجموعات الست حسب الترتيب كما يجب إتباع طرق العمل بدقة للحصول على نتائج صحيحة.
(3) ضع في الأنبوبة (Tube) النظيفة محلول العينة وأضف محلول (solution) كاشف المجموعة وإذا لم يحدث أي شيء انتقل إلى المجموعة التالية أما إذا تكون راسب فأجري التجارب التأكيدية مستعملاً جدول الكشف المناسب.
الكشف عن كاتيونات المجموعة الأولى من الشقوق القاعدية
الخلفية النظرية
– تشتمل هذه المجموعة على الكاتيونـات الآتية: الفضة Ag+ ، الرصاص Pb2+ ، الزئبقوز Hg22+
– كاشف المجموعة: هو حمض الكبريتيك المخفف HCl
– الصورة الترسيبية:
كلوريدات بيضاء اللون وهي:
- كلوريد الفضة (راسب أبيض) AgCl
- كلوريـد الرصاص (راسب أبيض) PbCl2
- كلوريد الزئبقوز (راسب أبيض) Hg2Cl2
– وتتميز هذه الكلوريدات بأنها لا تذوب في الماء فيما عدا كلوريد الرصاص يذوب في الماء الساخن.
– لرؤية التجربة الأساسية والتجارب التأكيدية والتجارب المميزة لهذة المجموعة : أضغط هنا
الكشف عن كاتيونات المجموعة الثانية من الشقوق القاعدية
الخلفية النظرية
– تتميز كاتيونات هذه المجموعة بترسبها على هيئة كبريتيدات بواسطة محلول H2S من محاليلها الساخنة المحمضة بحمض HCl المخفف، وبعبارة أخري يمكن القول بأن كبريتيداتها لا تذوب في حمض الهيدروكلوريك المخفف.
– قسمت كاتيونات المجموعة الثانية على مجموعتين فرعتين، إعتماداً على ذوبانها في محلول كبريتيد الأمونيوم (NH4)2S
– المجموعة الفرعية 2A أو مجموعة النحاس:
- وتشمل على الكاتيونات التي لا تذوب في محلول كبريتيد الأمونيوم (NH4)2S وهي كما يلي:
- نحاسيك Cu2+ ، كادميوم Cd2+ ، بزموث Bi2+ ، زئبقيك Hg2+
– المجموعة الفرعية 2B – مجموعة الزرنيخ:
- وتشمل على الكاتيونات التي تذوب في محلول كبريتيد الأمونيوم (NH4)2S وهي كما يلي:
- قصديروز Sn2+ ، قصديريك Sn4+ ، زرنيخوز As3+ ، زرنيخيك As5+ ، أنتيمونوز Sb3+ ، أنتيمونيك Sb5+
– سنتطرق بالدراسة هنا لكاتيونات المجموعة 2A فقط. وتوضيح جدول الكشف مباشرة لكاتيونات المجموعة 2B
– كاشف المجموعة:
محلول كبريتيد الهيدروجين H2S ويتم ترسيبها في وسط حامضي HCl المخفف.
– الصورة الترسيبية:
كبريتيدات ذات ألوان مختلفة وهي كالآتي:
- كبريتيد النحاس (راسب أسود) CuS
- كبريتيد الكادميوم (راسب أصفر) CdS
- كبريتيـد البزموت (راسب بني) Bi2S2
- كبريتيد الزئبقيك (راسب أسود) HgS
– لرؤية التجربة الأساسية والتجارب التأكيدية والتجارب المميزة لهذه المجموعة : أضغط هنا
الكشف عن كاتيونات المجموعة الثالثة من الشقوق القاعدية
الخلفية النظرية
تشمل هذه المجموعة على أربعة كاتيونات وهي كما يلي:
- حديدوز (Fe2+) Iron II
- حديديك (Fe3+) Iron III
- الومنيوم (Al3+) Aluminium
- كروم (Cr3+) Chromium
والتي تترسب على هيئة هيدروكسيدات عند معاملة محاليلها بمحلول هيدروكسيد الأمونيوم NH4OH وفي وجود كمية قليلة من محلول كلوريد الأمونيوم NH4Cl ، وتتميز هيدروكسيدات هذه المجموعة بأنها لا تذوب في الماء.
– كاشف المجموعة:
محلول هيدروكسيد الأمونيوم NH4OH وفي وجود كمية قليلة من محلول كلوريد الأمونيوم NH4Cl
– الصورة الترسيبية:
هيدروكسيدات ذات ألوان مختلفة وهي كما يلي:
- هيدروكسيد الحديدك (راسب بني) Fe(OH)3
- هيدروكسـيد الألمونيوم (راسب أبيض جيلاتيني) Al(OH)3
- هيدروكسيد الكروم (راسب رمادي مخضر) Cr(OH)3
– لرؤية التجربة الأساسية والتجارب التأكيدية والتجارب المميزة لهذه المجموعة : أضغط هنا
الكشف عن كاتيونات المجموعة الرابعة من الشقوق القاعدية
الخلفية النظرية
تشمل هذه المجموعة على الكاتيونات وهي كما يلي:
- خارصين (Zn2+) Zinc
- منجنيز (Mn2+) Manganese
- كوبلت (Co2+) Cobalt
- نيكل (Ni2+) Nickel
والتي تترسب على هيئة كبريتيدات عند معاملة محاليلها بمحلول كبريتيد الهيدروجين H2S في وسط قاعدي ، وتتميز كبريتيدات هذه المجموعة بأنها لا تذوب في الماء.
– كاشف المجموعة:
محلول كبريتيد الهيدروجين H2Sفي وجود محلول كلوريد الأمونيوم NH4Cl + محلول هيدروكسيد الأمونيوم NH4OH
– الصورة الترسيبية:
كبريتيدات ذات ألوان مختلفة وهي كما يلي:
- كبريتيد الخارصين (راسب أبيض) ZnS
- كبريتيد المنجنيز (راسب لحمي) MnS
- كبريتيـد الكوبلت (راسب أسود) CoS
- كبريتيد النيكل (راسب أسود) Ni
– لرؤية التجربة الأساسية والتجارب التأكيدية والتجارب المميزة لهذة المجموعة : أضغط هنا
الكشف عن كاتيونات المجموعة الخامسة من الشقوق القاعدية
الخلفية النظرية
– تشمل هذه المجموعة على الكاتيونات كما يلي:
- كالسيوم (Ca2+) Calcium
- إسترانشيوم (Sr2+) Strontium
- باريوم (Ba2+) Barium
والتي تترسب على هيئة كربونات عند معاملة محاليلها بمحلول كربونات الأمونيوم (NH4)2CO3 في وجود محلول كلوريد الأمونيوم NH4Cl + محلول هيدروكسيد الأمونيوم NH4OH ، وتتميز كربونات هذه المجموعة بأنها لا تذوب في الماء.
– كاشف المجموعة:
محلول كربونات الأمونيوم (NH4)2CO3 في وجود محلول كلوريد الأمونيوم NH4Cl + محلول هيدروكسيد الأمونيوم NH4OH
– الصورة الترسيبية:
كربونات بيضاء اللون وهي كالآتي:
- كربونات الكالسيوم (راسب أبيض) CaCO3
- كربونـات الإسترانشيوم (راسب أبيض) SrCO3
- كربونات الباريوم (راسب أبيض) BaCO3
– لرؤية التجربة الأساسية والتجارب التأكيدية والتجارب المميزة لهذه المجموعة : أضغط هنا
الكشف عن كاتيونات المجموعة السادسة من الشقوق القاعدية
الخلفية النظرية
- أمونيوم (NH4+) Ammonium
- بوتاسيوم (K+) Potassium
- ماغنسيوم (Mg2+) Magnesium
- صوديوم (Na+) Sodium
تتصف هذه المجموعة بعد ترسب كاتيوناتها بواسطة أي من كواشف المجموعات السابقة، وليس هناك كاشف مشترك يعمل على ترسيب جميع كاتيونات هذه المجموعة، بل أن كل كاتيون يتم اختباره بصورة مفصلة.
– لرؤية التجربة الأساسية والتجارب التأكيدية والتجارب المميزة لهذة المجموعة : أضغط هنا
المخطط العملي للكشف عن الشقوق القاعدية
نظراً لكبر المخطط العملي وأنه لا يمكن وضعه هنا على هيئة صورة ، لذا يجب تحميله ثم طباعته ورقياً أو تكبيره عن طريق الجوال أو الكمبيوتر ، ولتحميل المخطط العملي للكشف عن الشقوق القاعدية .
طريقة التحميل
– إذا لم يتم توجيهك لصفحة التحميل أو أن الرابط لا يعمل، فقط قم بإبلاغنا في التعليقات عن ذلك وسنقوم خلال 24 ساعة بحل المشكلة.
– إذا أردت كتاباَ معيناً في أى فرع من فروع علم الكيمياء، فقم بالدخول إلى قسم اتصل بنا وأرسل لنا أيميل فيه صورة الكتاب أو اسمه ، وأن شاء الله تعالى نعمل على توفيره لك مجاناً أو مدفوعاً حسب رغبة المالك الأصلي للحفاظ على حقوق الطبع والنشر إذا أمكن ذلك.
– كما يمكنك تحميل العديد من الكتب الكيميائية والمحاضرات والدورات المتعلقة بالكيمياء وذلك بالذهاب إلى الصفحة الرئيسية قسم “كتب كيميائية ” أو عبر الرابط التالي: كتب كيميائية المراجع : – الدليل العملي لمقرر كيمياء عامة (1) . معتز جمال سفيان، الطبعة الثانية (2015) / كلية العلوم التطبيقية – قسم الكيمياء – جامعة تعز – اليمن









المغنيسيوم يشبه إلى حد كبير القلويات الارضيه المجموعه الخامسه لماذا وضع في المجموعه السادسه علل؟ هذا اسوال في الشقوق القاعديه نرجو التعاون ورد اسريع لمن كان عنده اجابه كتب الله اجركم
الكواشف المستخدمة للكشف عن ايون الحديديك لا يمكن استخدامها في الكشف عن ايون الحديدوز …..ما السبب