الكيمياء التحليلية تهتم بدراسة تركيب المواد وتحديد مكوناتها. تشمل التحليل الكيفي والكمي، وتُستخدم في المختبرات والصناعات لتحديد نقاء المواد واكتشاف العناصر والمركبات بدقة.
الكيمياء التحليلية
-
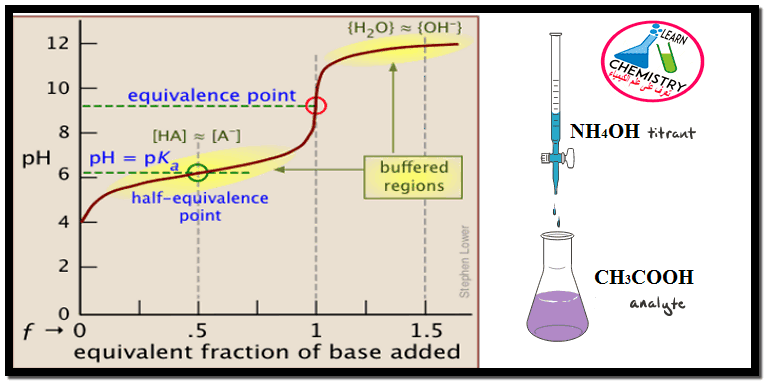
منحنى معايرة حمض ضعيف مع قاعدة ضعيفة
يمكن تمثيل منحنى معايرة حمض ضعيف مع قاعدة ضعيفة بدراسة معايرة 50 مل من محلول حمض الخليك 0.1N بواسطة محلول…
أكمل القراءة » -
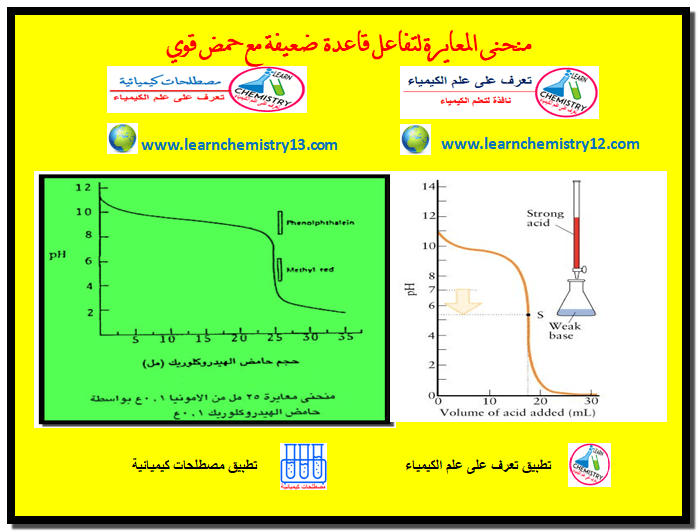
منحنى معايرة قاعدة ضعيفة مع حمض قوي
في هذا الموضوع سيتم استنتاج ورسم منحنى معايرة قاعدة ضعيفة مع حمض قوي Titration Curve of a weak base with…
أكمل القراءة » -
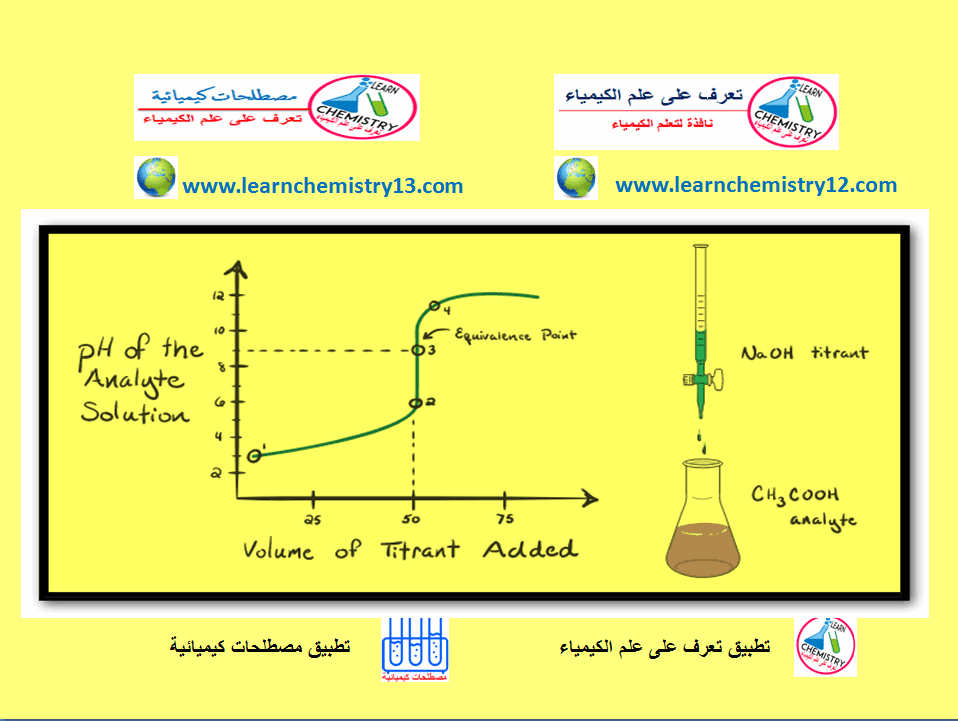
رسم منحنى المعايرة لتفاعل حمض ضعيف مع قاعدة قوية
منحنى المعايرة Titration Curve هو المنحنى الذي يمثل العلاقة بين حجم الحمض المتعادل (أو حجم القاعدة) والرقم الهيدروجيني للمحلول.
أكمل القراءة » -
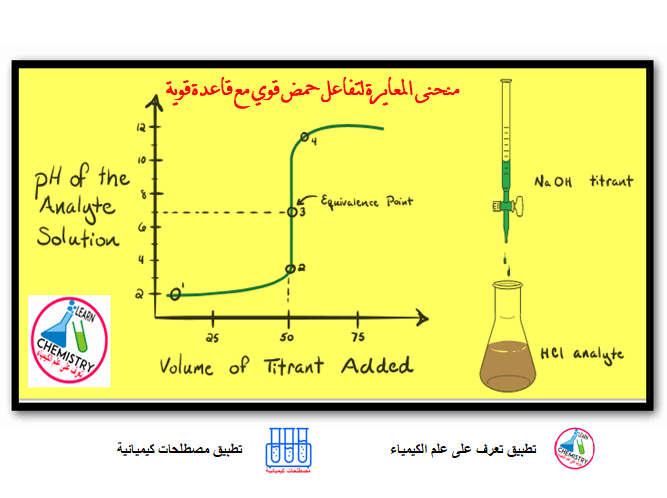
منحنى معايرة حمض قوي مع قاعدة قوية
منحنى معايرة حمض قوي مع قاعدة قوية هو المنحنى الذي يمثل العلاقة بين حجم الحمض القوي المتعادل والرقم الهيدروجيني للمحلول.
أكمل القراءة » -
حساب الرقم الهيدروجيني pH للمحاليل المنظمة
حساب الرقم الهيدروجيني pH للمحاليل المنظمة في حالة : (أ) محلول منظم من حمض ضعيف وأحد أملاحه - (ب) محلول…
أكمل القراءة » -
تأين الأملاح Disassociation of salts واشتقاق قوانين pH
سيتم مناقشة عن الاتزان في الأملاح - تأين الأملاح - اشتقاق قوانين pH للأملاح الناتجة من حمض قوي وقاعدة قوية،…
أكمل القراءة » -
تأين الأحماض والقواعد واشتقاق قوانين pH
سيتم مناقشة الأتزان وتأين الأحماض والقواعد Acid - base equilibrium وكيفية اشتقاق قوانين pH للأحماض والقواعد القوية والضعيفة بالتفصيل.
أكمل القراءة » -
تفكك الماء – اشتقاق القانون pH + pOH =14
أن كل أيونات الهيدروجين والهيدروكسيل الموجودة فى الماء النقي ناتجة من تفكك الماء ولهذا فإن تراكيزها تكون متساويةلذا يكون: pH…
أكمل القراءة » -
نظريات عمل الأدلة المستخدمة فى تفاعلات معايرات التعادل
نظريات عمل الأدلة المستخدمة فى تفاعلات معايرات التعادل: (1) النظرية الأيونية (2) النظرية الكروموفورية (3) النظرية الأيونية الكروموفورية.
أكمل القراءة » -
المدى الهيدروجيني للدليل المستخدم فى تفاعلات المعايرة
يعرف المدى الهيدروجيني للدليل بأنه المجال من الرقم الهيدروجيني الذي يتغير فيه لون الدليل، ولإختيار الدليل المناسب في تفاعلات التعادل…
أكمل القراءة »