موانع تآكل المعادن والسيطرة على التآكل
محتويات الموضوع
موانع تآكل المعادن Corrosion Inhibitors
– يمكن اعتبار مانع تآكل المعادن بأنه يعمل بشكل معاكس لفعل العامل المساعد الكيميائي. فهو يعرقل أو يوقف تفاعل التآكل.
– أن استخدام موانع التآكل هي إحدى الطرق لمعالجة عدد من مشاكل التآكل المختلفة.
– إن هذه الموانع هي مركبات كيميائية عضوية ولا عضوية.
السليكات والكرومات والفوسفات والبورات
– فمعظـم الموانع اللاعضوية مثل السليكات والكرومات والفوسفات والبورات تحد مـن عملية التآكل. وذلك بتأثيرها على القطب الموجب وأن استعمال بعضـها لا ينصح به في ظروف معينة. فمثلاً الاستخدام غير الصحيح للكرومـات قـد يؤدي إلى تعجيل التآكل بدلاً من إيقافه.
– فبوجود استقطاب الهيدروجين تؤدي إضافة الكرومات أو أية مؤكسد آخر على قلة الاستقطاب وبالتالي زيادة تيار التآكل الكهربائي. أيضاً إذا كان المانع بكميات غير كافية لتكوين غطاء واق متكامل فوق القطب الموجب فإن المناطق الصغيرة المتبقية سوف تتآكل بسرعة متزايدة مؤيدة بذلك إلى تنقـر المعدن.
نترات الصوديوم القاعدية
كما تستخدم نترات الصوديوم القاعدية لوحدها أو مع موانع لا عضوية أخرى كالفوسفات لحماية خطـوط الأنابيـب وناقلات المشتقات النفطيـة والكيميائية كذلك مادة بنزوات الصوديوم تستخدم لحمايته الفولاذ الطري.
الجير المطفأ
– أيضاً فإن الجير المطفأ 2(Ca(OH يعمل كمانع للتأكل بتأثيره علـى القطب السالب بواسطة ترسيب كربونات الصوديوم من المياه التي تحوى على العسرة المؤقتة أو ثاني أكسيد الكربون الذائب.
– فالدقائق الغروانية لكربونات الصوديوم تكون فيها شحنة موجبة تؤدي إلى انجذابها إلى مناطق القطـب السالب حيث ترسبها يوقف أو يقلل التآكل.
موانع تآكل المعادن العضوية
– إن موانع التآكل العضوية تعمل بطرق عديدة ومختلفـة. فـالمواد الغراونية العضوية تكون طبقات واقية نتيجة التصاقها بسطح المعدن.
– المواد الكيميائية ذات الفعالية السطحية (Surface-Active Chemicals) التـي تحتوي على مجاميع قطبية تعزز الانتشار والالتصـاق المناسـب بالسطح المعدني (وهي غير متأينة) ولكنها تكون غطاء على سطح المعدن.
– القواعـد العضوية مثل الأمينـات (Amines) والبريـدين (Pyridine) والكينولين (Quinoline) ومشتقاتها تكون أيونات موجبة تحتوي على مجاميع وجـذور ذات طبيعة طاردة للماء (Hydrophobic). وأن هذه الأيونات الموجبة تربط نفسها من خلال ذرة النيتروجين إلى المناطق السالبة لسطح المعدن.
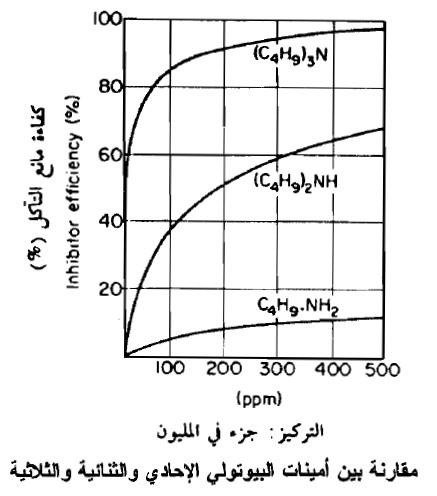
– ولقد وجد أن كفاءة هذه الموانع يعتمد على عدد ومعيـار الـجـذور الهيدروكربونية. فالأمينات الأميلي الأوليـة (C5H11NH2) هي أفضـل كمانعات للتآكل من الأمينات الاثيلي الأولية (C2H5NH2).
– فالزيادة في حماية المعدن التي يمكن الحصول عليها سبب زيادة عدد جذور الألكيل (Alkyl Radicals) موضحة في الشكل التالي. حيث أن أجزاء قليلة في المليون من الأمينات الثلاثية تكفي للحصول على حماية تامة.
– الأمينات ذات الأوزان الجزيئية العالية والمشتقة من الراتينج القلفونية (Rosin) كما موضح في الشكل التالي هي موانع جيدة للتأكل.
أملاح المركبات العضوية
– الأملاح التي تذوب في الزيوت النفطية مثل السترات ، والنافثينـات والمشتقات الأخرى تستخدم كموانع للتآكل في عملية تنظيف المعدن بمغطـس حامضي (Acid Picking).
– الملح المتكون نتيجة تفاعل أمين راتينج القلفونيـة (Rosin Amine) مع خامس كلور الفينول (Pentachlorophenol) عندما يدخل في تركيـب الغطاء المستخدم للأنابيب المدفونة يقاوم أو يمنع التآكل الحادث بسبب البكتريا في التربة.
المشتقات الأمينية
– المشتقات الأمينية الأخرى يمكن أن تفيد في استعمالات معينـة، فمرکب (2hydroxypropyl Amine Nitrite) هو مركب غيـر متأين يوصى باستخدامه لمنع تأكل أواني القصدير بواسطة أنواع الصابون السائل والمعقمات الفينولية ومعقمات زيت الصنوبر (Pine) والمحاليـل المركـزة للعوامـل التبليليــة أو الترطيبـة للأمونيــــوم الرباعيـة. (Quaternary Ammonium)
– بعض الموانع العضوية هي عوامل ذات فعالية سطحية وطبيعة أيونية سالبة تحتوي على مجاميع قطبية مثل الكبريتيـد وهيدروكبريتيـد والكحـول وبعض الحوامض فهي في بعض الأحوال تعمل كمانع للأكسدة فتمنع تكـوين البروكسيدات والـ (Peracids) المسببة للتأكل.
موانع تآكل المعادن للطور البخاري (Vapour Phase Inhibitors)
– موانع التآكل للطور البخاري هي مواد تتبخر بسرعة وتكـون طبقـة واقية أو مانعة للتأكل.
– فهذه الموانع تستعمل لحماية خطوط بخار الماء عنـد وجود ثاني أكسيد الكربون أو حماية الفولاذ والحديد من التآكل نتيجة وجـود الرطوبة وثاني أكسيد الكبريت.
– وبعض الأجزاء المعدنية يمكن حمايتها من التآكل الجوي وذلك بلفهـا بنوع من الورق المشبع بمانع التآكل للطور البخاري، فبدلاً من تغطية المواد المعدنية بطبقة من الزيت أو الدهن الشحمي (Grease) تلف بغطـاء مـشـبع بالمانع.
– فعند خزن الآلات الطائرات الاحتياطية يوضع في كل أسطوانة من الآلة بعض البلورات لمانع التآكل للطور البخاري وذلك عن طريـق فتحـة الإشعال بالشرر (Spacking Plug) فيها
– أما الأقسام الخارجية للآلات فتلف بورقة مغطاة بنوع من اللدائن ذات المسامية المخفضة. وتحتوي على مانع من موانع التأكل للطور البخاري التي استعملت وبنجاح.
السيطرة على تآكل المعادن
فيما يلي ملخص لبعض الأسس العامة للسيطرة على تآكل المعادن استخلصـت من البنود المذكورة سلفاً كما يلي:
الملاحظة الأولى
– إن اختيار المعدن يجب ألا يعتمد فقط على تكلفته وتركيبه. وإنما أيضاً على خواصه الكيميائية والوسط الذي يستعمل فيه.
– فلغرض تقليل التآكل إلى الحد الأدنى يجب تخليص المعدن من الجهود الميكانيكية الموجـودة فيه.
– وإذا كان المعدن نشطاً فيجب عزله مـن المعـادن ذات الطبيعـة السالبة. فعندما يتوجب تماس معدنين فإنه من الضـروري أن يكـون جهود أكسدتهم متقاربة أو متساوية قدر الإمكان.
– إن المساحة السطحية للمعدن الثمين الغير نشط يجب أن تكون أصغر من تلك للمعدن الموجب النشط. يمكن تقليل فرصة تنق المعدن وذلك بوضع واقية علـى كـلا المعدنين.
الملاحظة الثانية
– يجب عزل أو منع الرطوبة. فالأجزاء المعدنية المخزونة والمحفوظة في لدائن منخفضة المسامية ومعها جل الالومينا أو السليكا تبقى محمية من التآكل لسنين عديدة.
– وفي حالة وجود رطوبة أو محلول الكتروليتي فيجب استخدام مانع للتآكل.
الملاحظة الثالثة
– يجب السيطرة على حموضة أو قاعدية وسط التآكل حيث أن كل معدن يتميز بحد أدني للتآكل عند رقم هيدروجيني معين.
– فالحموضة الكليـة يمكن تقليلها بتكلفة قليلة جـداً. وذلك بإضـافة كربونات الكالسيوم (Limestone) أو الجير المطفأ 2(Ca(OH إلا أنه في المياه الحامضية التي تحوى على حامض الكبريتيك تكون عملية التعادل بطيئـة بسـبب الذوبان البطيء لكبريتات الكالسيوم .
– إن رمـاد الصـودا (Na2CO3) الأكثر غلاء يستخدم بشكل واسع. إذا لم تكن السيطرة علـى الـرقم الهيدروجيني ذا نفع فيمكن تقليل التآكل باستخدام أغطية واقية أو خاملة ومعادن غير نشيطة.
الملاحظة الرابعة
– عند تصميم الأجهزة المعدنية يجـب تجنـب التجميـدات الـحـادة أو الانحناءات أو صلات تراكب (Lap Joint) أو عوارض التي يمكن أن تؤدي إلى مناطق خاملة يتجمع فيها راسـب (Sediment) أو قشـور (Scale)
– إن مثل هذه الطريقة تتأثر بشكل أكبر بذلك النوع من التأكل التي تسببه الخلايا التركيزية .
المراجع: كتاب أسس الكيمياء الصناعية – الطبعة الأولى 2005 – أ.د. محمد مجدي واصل أستاذ الكيمياء الفيزيائية – كلية العلوم – جامعة الأزهر – مصر