الكيمياء العامة
الكيمياء العامة تُعد أساس فروع الكيمياء، تدرس المادة وخواصها وتغيراتها. تشمل الذرات، الجزيئات، التفاعلات، والمعادلات. تساعد في فهم الظواهر الطبيعية وتطبيقات العلوم في الحياة اليومية.
-
القصدير Tin – الخواص الفيزيائية والكيميائية للقصدير
ما هو عنصر القصدير Tin؟ – القصدير tin هو عنصر من عناصر الجدول الدوري: العدد الذري = 50 ، العدد…
أكمل القراءة » -
الإنديوم Indium – الخواص الفيزيائية والكيميائية للإنديوم
ما هو عنصر الإنديوم Indium؟ – الإنديوم Indium هو عنصر من عناصر الجدول الدوري: العدد الذري = 49 ، العدد…
أكمل القراءة » -
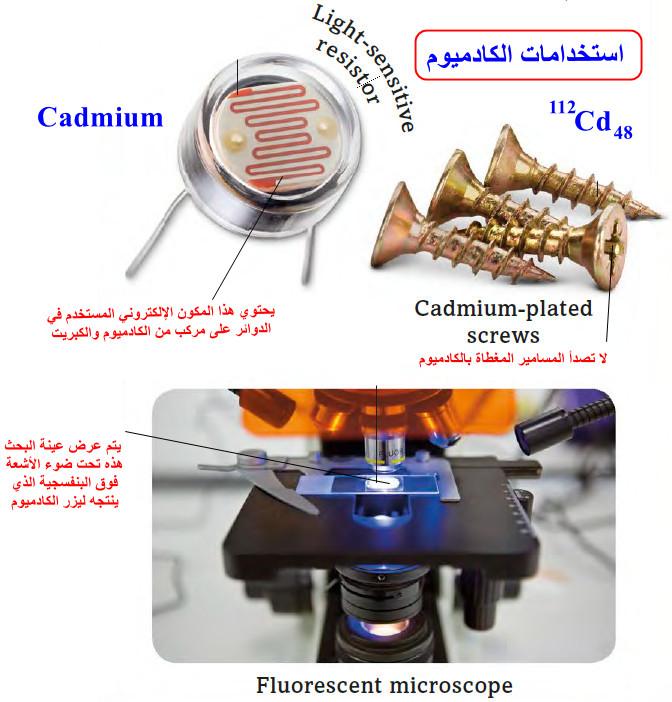
الكادميوم Cadmium – الخواص الفيزيائية والكيميائية للكادميوم
ما هو عنصر الكادميوم Cadmium؟ – الكادميوم Cadmium هو عنصر من عناصر الجدول الدوري: العدد الذري = 48 ، العدد…
أكمل القراءة » -
الفضة Silver – الخواص الفيزيائية والكيميائية للفضة
ما هو عنصر الفضة Silver؟ – الفضة Silver هو عنصر من عناصر الجدول الدوري: العدد الذري = 47 ، العدد…
أكمل القراءة » -
البلاديوم Palladium – الخواص الفيزيائية والكيميائية للبلاديوم
ما هو عنصر البلاديوم Palladium؟ – البلاديوم Palladium هو عنصر من عناصر الجدول الدوري: العدد الذري = 46 ، العدد…
أكمل القراءة » -
الراديوم Radium – الخواص الفيزيائية والكيميائية للراديوم
ما هو عنصر الراديوم Radium؟ – الراديوم Radium هو عنصر من عناصر الجدول الدوري: العدد الذري = 88 ، العدد…
أكمل القراءة » -
الروديوم Rhodium – الخواص الفيزيائية والكيميائية للروديوم
ما هو عنصر الروديوم Rhodium؟ – الروديوم Rhodium هو عنصر من عناصر الجدول الدوري: العدد الذري = 45 ، العدد…
أكمل القراءة » -
الروثينيوم Ruthenium – الخواص الفيزيائية والكيميائية له
ما هو عنصر الروثينيوم Ruthenium؟ – الروثينيوم Ruthenium هو عنصر من عناصر الجدول الدوري: العدد الذري = 44 ، العدد…
أكمل القراءة » -
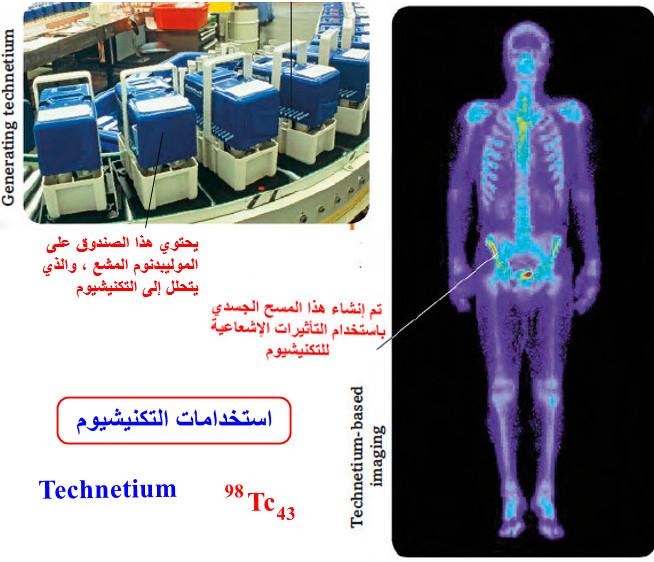
التكنيشيوم Technetium – الخواص الفيزيائية والكيميائية له
ما هو عنصر التكنيشيوم Technetium؟ – التكنيشيوم Technetium هو عنصر من عناصر الجدول الدوري: العدد الذري = 43 ، العدد…
أكمل القراءة » -
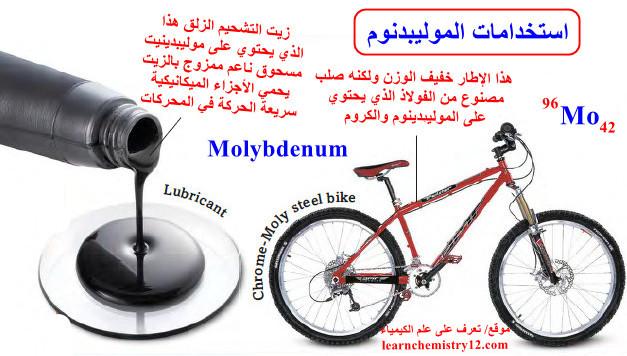
الموليبدنوم Molybdenum – الخواص الفيزيائية والكيميائية له
ما هو عنصر الموليبدنوم Molybdenum؟ – الموليبدنوم Molybdenum هو عنصر من عناصر الجدول الدوري: العدد الذري = 42 ، العدد…
أكمل القراءة »