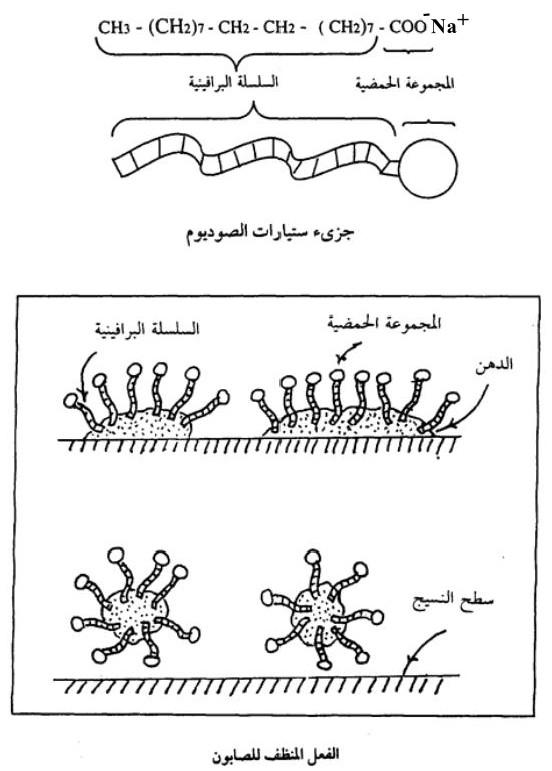
الفعل المنظف للصابون – كيف يقوم الصابون بعملية التنظيف؟
الفعل المنظف للصابون
– الفعل المنظف للصابون عملية معقدة إلى حد ما ولكنها تعتمد أساساً على بعض الخواص الطبيعية لجزيئات أملاح الأحماض الدهنية التي يتكون منها الصابون.
– إذا أخذنا جزىء إستيارات الصوديوم مثالاً لجزيئات الصابون، لوجدنا أن هذا الجزيء يتكون من سلسلة برافينية تتكون من ذرات الكربون المتصلة بالهدروجين، وتوجد بنهاية هذه السلسلة مجموعة الكربوكسيل الحمضية التي تكون الملح عند اتحادها بذرة صوديوم.
– تتصف السلاسل الهدروكربونية البرافينية عموما بأنها كارهة للماء ويتضح ذلك تماماً عندما نضع قطعة من الشمع البرافيني في الماء، ثم نخرجها منه، فإننا نجد أن قطرات الماء تتساقط منها تاركة سطحها غير مبتل على وجه التقريب وذلك لأنه لا يوجد في السلاسل البرافينية التى يتكون منها الشمع ما يشد جزيئات الماء أو يجذبها إليه .
– توصف هذه السلاسل البرافينية بأنها كارهة للماء، وذلك لأنها عندما توضع في وسط مائي، تحاول أن تبتعد عن جزيئات الماء المكونة لهذا الوسط.
– أما المجموعة الحمضية التى توجد فى طرف سلسلة جزىء الصابون، فهى مجموعة محبة للماء، ولها القدرة على جذب عدة جزيئات من الماء حولها، وخاصة عندما تكون على هيئة أيون سالب [–COO] كما في جزيئات الصابون .
– وعلى هذا الأساس فإنه عندما يوجد جزىء من ستيارات الصوديوم (الصابون) فى وسط مائي، فإن المجموعة الحمضية الموجودة بالجزىء سوف تنغمس في الماء، فهى محبة له على حين تبتعد السلسلة البرافينية على قدر الإمكان عن هذا الماء، فهي كارهة له.
– هذه هي الخواص الطبيعية الأساسية التي تتحكم في الفعل المنظف للصابون .
– الهدف من عمليات الغسيل في أغلب الأحوال، هو إزالة بعض الأوساخ التي قد تتعلق بسطح النسيج، وغالبا ما تتعلق هذه الشوائب ببعض بقع الزيت أو الدهون التي قد توجد على سطح النسيج ولهذا فإنه عند إزالة هذه الدهون من على سطح النسيج تأخذ معها أغلب الشوائب العالقة بها تاركة سطح النسيج نظيفاً كما كان.
– وعندما نضع قليلاً من الصابون فى الماء، فإن السلاسل البرافينية الجزيئاته تنغمس في بقع الدهن مبتعدة عن الماء على حين تتجه المجموعات الحمضية لهذه الجزيئات ناحية الماء وتنغمس فيه.
– وعند إمرار تيار من الماء فوق سطح النسيج، فإنه يحمل معه المجموعات الحمضية التي تحمل معها بقعة الدهن عن طريق السلاسل الهدروكربونية المنغمسة فيها، وبذلك تنفصل بقعة الدهن وما يعلق بها من شوائب، عن سطح النسيج يصبح نظيفا منها تماماً.
تأثير الماء اليسر والعسر على عمل الصابون
– لا يتم هذا الفعل المنظف للصابون إلا في حالة الماء اليسر، أي الماء الذي يخلو من أيونات الكالسيوم أو المغنسيوم.
– أما الماء الذي توجد به مثل هذه الأيونات، وهو يعرف باسم الماء العسر، فلا يصلح فيه الصابون لأنه يكون في هذه الحالة أملاح الكالسيوم والمغنسيوم للأحماض الدهنية المكونة للصابون، وهى أملاح لا تقبل الذوبان في الماء وتظهر بالماء على هيئة رواسب، وهي لا تساعد بذلك على التنظيف، لأن الفعل المنظف للصابون يتطلب وجود بعض الجزيئات الذائبة منه في الماء.
المراجع
– كتاب الصناعات الكيميائية – الجزء الثالث – البترول والكيمياويات، الصابون الممظفات الصناعية. ، المطاط – د/ أحمد مدحت عبد السلام – القاهرة – دار الفكر العربي – الطبعة الأولى 1997.
– أسس الكيمياء الصناعية – د/ محمد مجدى واصل – القاهرة – دار الفجر للنشر والتوزيع – الطبعة الأولى 2005.
– الكيمياء الصناعية – الجزء الثاني – تكنولوجيا الصناعات الكيميائية العضوية. – د/ طارق إسماعيل كاخيا – الطبعة الأولى.