الكيمياءالكيمياء العامةعناصر الجدول الدورى
عنصر البورون Boron

أولاً:
ما هو عنصر البورون؟
** البورون B
عنصر من عناصر الجدول الدوري العدد الذري=5 ، العدد الكتلي=
10
**
التوزيع الإلكتروني لعنصر البورون: 2P1
1S2
, 2S2
عنصر من عناصر الجدول الدوري العدد الذري=5 ، العدد الكتلي=
10
**
التوزيع الإلكتروني لعنصر البورون: 2P1
1S2
, 2S2
** البورون
عنصر
فلزي
ثلاثي
التكافؤ
عنصر
فلزي
ثلاثي
التكافؤ
** البورون عبارة عن جسم صلب يتمتع بقساوة عالية.
** يكون البورون على شكل:
(أ) بلوري: على شكل مسحوق ناعم أسود اللون قليل الفعالية في الشروط العادية، إذ يتمتع
البورون بثلاثة
أشكال متغايرة
البنية

البورون بثلاثة
أشكال متغايرة
البنية

(ب)
غير
بلوري: على
شكل
مسحوق
بني
اللون
له
فعالية
كبيرة
نظراً
لكبر
مساحة
سطحه الفعال.

غير
بلوري: على
شكل
مسحوق
بني
اللون
له
فعالية
كبيرة
نظراً
لكبر
مساحة
سطحه الفعال.

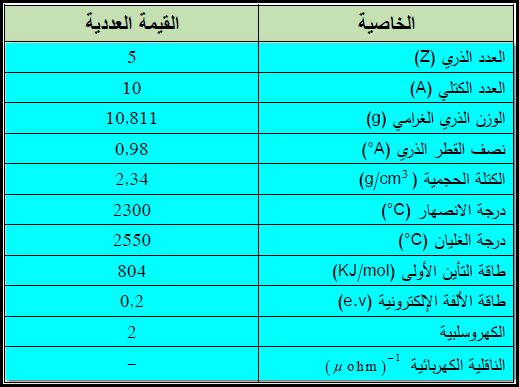
** الجدول التالي يوضح بعض الخواص العامة لعنصر البورون:
ثانياً:
اكتشافه ووجوده في الطبيعة
** عزل البورون
من
قبل Gay-Lussac وThenard في
فرنسا،
ومن
قبل Davy في بريطانيا سنة 1808م.
من
قبل Gay-Lussac وThenard في
فرنسا،
ومن
قبل Davy في بريطانيا سنة 1808م.
** أصل
اسم
البورون
من
العربية
البوراق بمعنى أبيض اللون لامع، الذي يدل على مصدره Borax وهو معدن خام
على
شكل
بلورات
لامعة.
اسم
البورون
من
العربية
البوراق بمعنى أبيض اللون لامع، الذي يدل على مصدره Borax وهو معدن خام
على
شكل
بلورات
لامعة.
** يوجد
عنصر
البورون
في
الطبيعة
بشكل
حر،
وإنما
يوجد
بشكل
بورات
في
المنابع
الحارة.
عنصر
البورون
في
الطبيعة
بشكل
حر،
وإنما
يوجد
بشكل
بورات
في
المنابع
الحارة.
** يشكل البورون 0.005 من القشرة الأرضية .
** أهم خامات البورون:
البوراكس: Na2B4O7 .10H2O
الكيرنيت: Na2B4O7 .4H2O
الكوليمانيت:
Ca2B6O11
.5H2O
Ca2B6O11
.5H2O
الأشاريت: MgHBO3
حامض البوريك:
H3BO3
H3BO3
ثالثاً:
طرق تحضير البورون
يحضر البورون بعدة طرق:
(أ) البورون اللابلوري:
يحضر بمعالجة البوراكس مثلا بحمض كلور الماء ثم معالجة الناتج حرارياً لاستحصال ثلاثي أكسيد البورون الذي يختزل
أخيراً بالماغنسيوم وذلك وفق المعادلات:
أخيراً بالماغنسيوم وذلك وفق المعادلات:
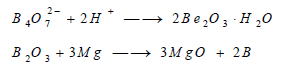
(ب) البورون البلوري:
**يحضر البورون البلوري أما بإختزال أكسيد البورون بواسطة الألمونيوم بالحرارة وفي وجود هيدروكسيد الصوديوم
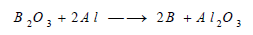
**أو بإختزال ثلاثي بروميد البورون بواسطة الهيدروجين في درجة حرارة عالية
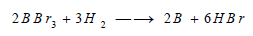
رابعاً:
الخواص الكيميائية لعنصر البورون
(1) تفاعل البورون مع الأكسجين
يتفاعل مع أكسجين الهواء في درجة حرارة تناهز 700Co مشكلا ثلاثي أوكسي ثنائي البورون وفق التفاعل التالي:
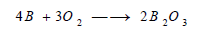
(2) تفاعل البورون مع الماء
يتفاعل البورون مع الماء في درجة الحرارة العالية وفق المعادلة:
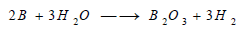
(3) تفاعل البورون مع الأحماض
يتفاعل البورون مع الأحماض المركزة والمؤكسدة في وجود التسخين ليشكل حمض البوريك
H3BO3 ولا يتفاعل مع الأحماض الممدة حيث لا يستطيع طرد الهيدروجين منها:
H3BO3 ولا يتفاعل مع الأحماض الممدة حيث لا يستطيع طرد الهيدروجين منها:
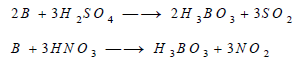
(4) تفاعل البورون مع القواعد
لا يتفاعل مع القواعد المركزة دون درجة
500Co ولكن فوق هذه الدرجة يشكل –H2BO3 والهيدروجين:

500Co ولكن فوق هذه الدرجة يشكل –H2BO3 والهيدروجين:
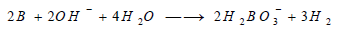
(5) تفاعل البورون مع المعادن
يتفاعل
مع
بعض
المعادن
مباشرة
بالتسخين
ليعطي
بوريدات
المعادن
مثل
بوريد
الصوديوم
مع
بعض
المعادن
مباشرة
بالتسخين
ليعطي
بوريدات
المعادن
مثل
بوريد
الصوديوم
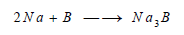
(6) تفاعل البورون مع الكبريت
يتفاعل
مع
الكبريت
ليعطي
كبريت
البورون:

مع
الكبريت
ليعطي
كبريت
البورون:
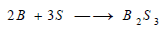
(7)تفاعل البورون مع النيتروجين
يتأثر البورون بالآزوت في وجود التسخين ليعطي نتريد البورون
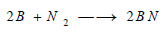
(8)تفاعل البورون مع الهالوجينات
يتفاعل البورون مع الهالوجينات بالحرارة
خامساً:
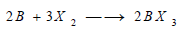
خامساً:
استخدامات عنصر البورون
(1) يستخدم
البورون
بشكل
كبير
في
عمليات
التركيب
العضوي.
البورون
بشكل
كبير
في
عمليات
التركيب
العضوي.
(2) يدخل البورون
في
صناعة
زجاج البوروسيليكات.
في
صناعة
زجاج البوروسيليكات.
(3) يدخل البورون في إنتاج الألياف الزجاجية العازلة ومواد التبيض .
(4) يستعمل البورون كمواد حافظة للأخشاب.
(5) يستعمل
البورون
في
السيطرة
والتحكم
في
المفاعلات
النووية
كدرع
واق
من
الإشعاع
وكذلك
للكشف
عن النيوترونات.
البورون
في
السيطرة
والتحكم
في
المفاعلات
النووية
كدرع
واق
من
الإشعاع
وكذلك
للكشف
عن النيوترونات.
(6) يستخدم البورون في مجالات طبية، وفي علاج الروماتيزم وآلام المفاصل.
(7)
حمض
البوريك
مركب
مهم
يستخدم في
صناعة
النسيج.
حمض
البوريك
مركب
مهم
يستخدم في
صناعة
النسيج.
المراجع: دراسة كيميائية تحليلية مفصلة لعناصر الجدول الدوري / الأستاذ الدكتور حسن بوزيّان أستاذ بقسم الكيمياء بالمدرسة العليا للأساتذة / الجزء الأول / أبريل 2017 / الجزائر