أسئلة وإجاباتالكيمياءالكيمياء العامة
مسائل محلولة على رتبة التفاعل Solved Problems On Reaction Order

(أضغط على الموضوع الذي تريده)
5- تفاعلات الرتبة االثالثة Third order reaction
6- طرق تعيين رتبة التفاعل Determining of Order reaction
6- طرق تعيين رتبة التفاعل Determining of Order reaction
7- مسائل محلولة على رتبة التفاعل Solved Problems On Order reaction
والآن نبدأ بحل المسائل وعددها (17) مسألة وإذا كان لديك أى استفسار عن هذة المسائل أترك لنا تعليق وسوف نرد عليك في أسرع وقت ممكن.
مثال (1)
إذا علم ان ثابت التحلل المشع
للراديوم هو 1.25 × 10-4 عندما كان الزمن مقاساً بالدقائق. ماهو الكسر من المادة الأصلية
الذي يتبقى بعد 5.33 يوماً؟
للراديوم هو 1.25 × 10-4 عندما كان الزمن مقاساً بالدقائق. ماهو الكسر من المادة الأصلية
الذي يتبقى بعد 5.33 يوماً؟

مثال (2)
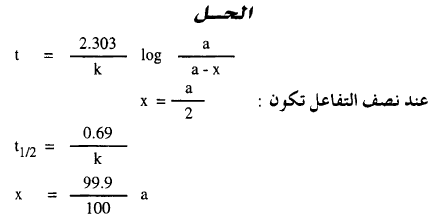
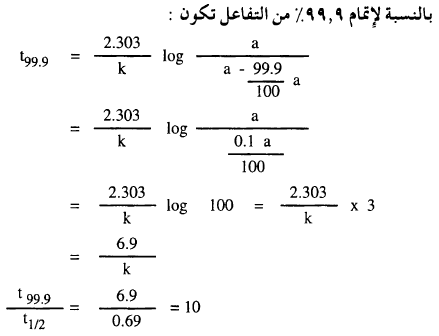
أثبت أن الزمن اللازم لإتمام 99.9 % من أي تفاعل من الرتبة
الأولى يساوي 10 أضعاف الزمن اللازم لإتمام نصف التفاعل؟
الأولى يساوي 10 أضعاف الزمن اللازم لإتمام نصف التفاعل؟
مثال (3)
إذا علمت أن فترة نصف العمر
للراديوم هي 3.85 يوماً. أوجد النسبة التي تتبقى بعد 40 يوماً؟

مثال (4)
أخذت 2 مل من محلول خلات الميثيل في
حمض الهيدروكلوريك المخفف في فترات زمنية مختلفة ثم عويرت بواسطة محلول هيدروكسيد
الباريوم. من النتائج التالية احسب ثابت السرعة للتحلل المائي الحامضي لخلات
الميثيل؟
حمض الهيدروكلوريك المخفف في فترات زمنية مختلفة ثم عويرت بواسطة محلول هيدروكسيد
الباريوم. من النتائج التالية احسب ثابت السرعة للتحلل المائي الحامضي لخلات
الميثيل؟

مثال (5)
إذا سخن حامض المالونيك فإنه يتحلل
إلى حامض الخليك وثاني أكسيد الكربون وقد عينت سرعة التحلل عند درجة حرارة 136 مo بقياس الزيادة فى الضغط
الناتجة في وعاء مغلق – من النتائج التالية أحسب سرعة التفاعل؟
إلى حامض الخليك وثاني أكسيد الكربون وقد عينت سرعة التحلل عند درجة حرارة 136 مo بقياس الزيادة فى الضغط
الناتجة في وعاء مغلق – من النتائج التالية أحسب سرعة التفاعل؟
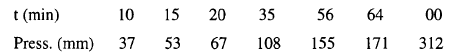
وأوجد أيضاً الزمن
اللازم لاستهلاك نصف كمية حامض المالونيك؟
اللازم لاستهلاك نصف كمية حامض المالونيك؟

مثال (6)
فى تحلل خامس أكسيد النيتروجين في
محلول رابع كلوريد الكربون عند درجة حرارة 40مo عينت سرعة التفاعل بقياس كمية التحلل معبراً عنها بواسطة حجم
الأكسجين الناتج في فترات زمنية مختلفة كمايلى:
محلول رابع كلوريد الكربون عند درجة حرارة 40مo عينت سرعة التفاعل بقياس كمية التحلل معبراً عنها بواسطة حجم
الأكسجين الناتج في فترات زمنية مختلفة كمايلى:
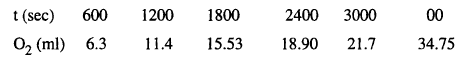
أثبت أن التفاعل من الرتبة الأولى. عين
ثابت السرعة واذكر الوحدات؟ ماهو الزمن اللازم لإغلال التركيز إلى نصف قيمته
الأصلية؟
ثابت السرعة واذكر الوحدات؟ ماهو الزمن اللازم لإغلال التركيز إلى نصف قيمته
الأصلية؟

مثال (7)
في التحلل الغازي للإسيتالدهيد
اتبع التفاعل بقياس الزيادة في الضغط P في وعاء مغلق. وكانت النتائج كما يلي:
اتبع التفاعل بقياس الزيادة في الضغط P في وعاء مغلق. وكانت النتائج كما يلي:
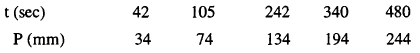
فإذا كان الضغط الأولى داخل الوعاء يساوي 363 مم زئبق ، اثبت أن
التفاعل من الرتبة الثانية؟
التفاعل من الرتبة الثانية؟

مثال (8)
في تحلل فوق أكسيد الهيدروجين
بواسطة ثاني أكسيد المنجنيز، كانت حجوم برمنجانات البوتاسيوم المكافئة لعينة ثابتة
من المخلوط بعد أزمنة مختلفة من بدء التفاعل كما يلي:
بواسطة ثاني أكسيد المنجنيز، كانت حجوم برمنجانات البوتاسيوم المكافئة لعينة ثابتة
من المخلوط بعد أزمنة مختلفة من بدء التفاعل كما يلي:
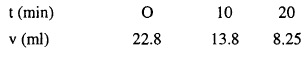
أوجد رتبة التفاعل؟

مثال (9)
فى تحلل السكروز إلى جلوكوز وفركتوز
بواسطة حمض المخفف ، كانت زوايا الدوران عند الأزمنة المختلفة كما يلي:
بواسطة حمض المخفف ، كانت زوايا الدوران عند الأزمنة المختلفة كما يلي:
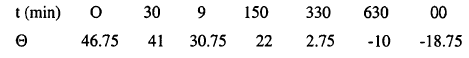
أوجد سرعة التفاعل وفترة نصف العمر؟

مثال (10)
عند تحلل غاز معين ، كانت النسبة
المئوية للتحلل عند الأزمنة المختلفة كمايلى:
المئوية للتحلل عند الأزمنة المختلفة كمايلى:
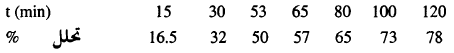
أوجد رتبة التفاعل؟

مثال (11)
إذا سخن فوق أكسيد النيتروجين
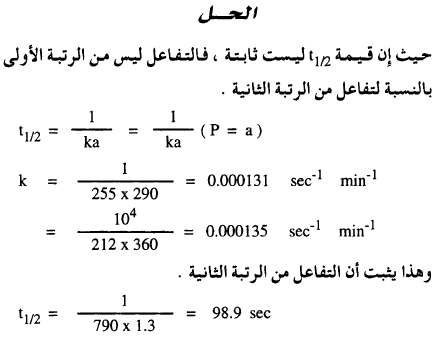
فإنه يتحلل. وعند ضغوط أولية مختلفة كانت فترات نصف العمر المقابلة كما يلي:
فإنه يتحلل. وعند ضغوط أولية مختلفة كانت فترات نصف العمر المقابلة كما يلي:
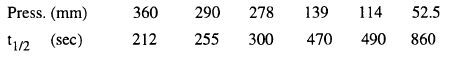
ما هي رتبة التفاعل؟

مثال (12)
في تحلل خامس أكسيد النيتروجين
عند درجة حرارة 760 م نحصل على النتائج التالية لفترات نصف العمر مع الضغط الأولى :
عند درجة حرارة 760 م نحصل على النتائج التالية لفترات نصف العمر مع الضغط الأولى :
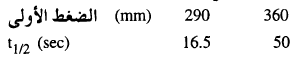
احسب رتبة التفاعل وفترة نصف العمر؟
مثال (13)
عند تفاعل كميات جزيئية متساوية
من البروم وحامض الفيوماريك في محلول مائي كانت سرعة التفاعل dc/dt تساوي 0.0106 وحدة عندما كان تركيز
المواد المتفاعلة يساوي 8.37 بنفس الوحدات ، وعندما قل التركيز إلى 3.66 وحدة أصبحت سرعة التفاعل 0.0022 بنفس الوحدات. ما هي رتبة التفاعل؟
من البروم وحامض الفيوماريك في محلول مائي كانت سرعة التفاعل dc/dt تساوي 0.0106 وحدة عندما كان تركيز
المواد المتفاعلة يساوي 8.37 بنفس الوحدات ، وعندما قل التركيز إلى 3.66 وحدة أصبحت سرعة التفاعل 0.0022 بنفس الوحدات. ما هي رتبة التفاعل؟

مثال (14)
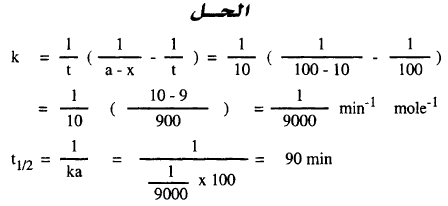
لوحظ في تفاعل معين ثنائي
الجزيئية فيه (a = b = 1 mole/L) أنه يلزم 10 دقائق لكي يتم 10% من التفاعل. كم من الوقت يلزم لكي يتم 5% من التفاعل؟
الجزيئية فيه (a = b = 1 mole/L) أنه يلزم 10 دقائق لكي يتم 10% من التفاعل. كم من الوقت يلزم لكي يتم 5% من التفاعل؟
مثال (15)
خلطت كمية من مادة A مع كمية مكافئة لها من
مادة B وبعد 100 ثانية تفاعلت نصف كمية
المادة A الأصلية. ما هو مقدار
المادة المتفاعلة من A في 200 ثانية إذا كان التفاعل
بالنسبة لها:
(أ) من الرتبة الأولى؟
ب) من الرتبة الثانية؟


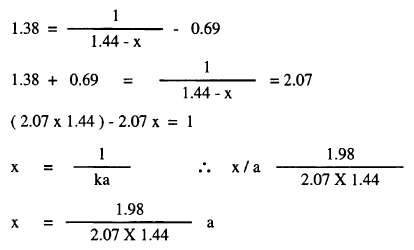
مثال (16)
بتحلل الأرزين بالتسخين إلى
الزرنيخ الصلب والهيدروجين يمكن تتبع سرعة التفاعل بقياس الضغط عند ثبوت الحجم عند
درجة 310 مo كما يلي:
الزرنيخ الصلب والهيدروجين يمكن تتبع سرعة التفاعل بقياس الضغط عند ثبوت الحجم عند
درجة 310 مo كما يلي:
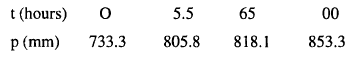
أوجد رتبة التفاعل؟

مثال (17)
عينت سرعة التفاعل:
بمعايرة 10 مل من مخلوط التفاعل عند 25مo بواسطة 0.01 محلول يود وكانت النتائج
كالآتي:
كالآتي:
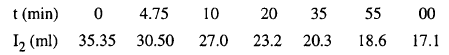
ما هي السرعة النوعية للتفاعل (ثابت
السرعة)؟
السرعة)؟

إقرأ هذة الموضوعات المهمة : (أضغط على الموضوع الذي تريده)
المراجع :
– الكيمياء الحركية والكهربية.محمد مجدي عبد الله واصل ، الطبعة لأولى (1425هـ – 2004م) / دار النشر للجامعات – القاهرة – جمهورية مصر العربية





سؤال كيف اثبت ان التفاعل من مرتبه الأولى بيانا ارجوالرد
مع جزيل الشكر
ممتع جداً جداً ومفيد