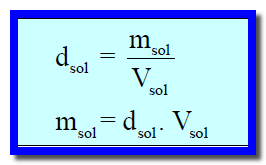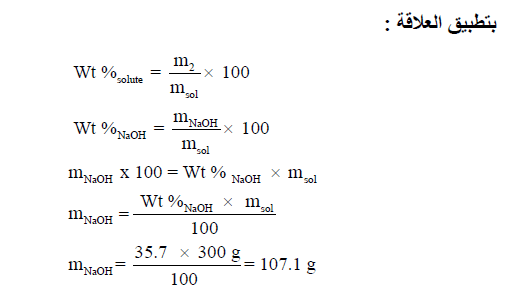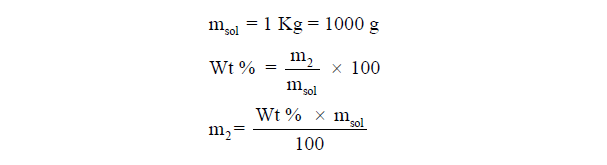النسبة المئوية الوزنية للمذاب Weight Percentage + مسائل محلولة

النسبة المئوية الوزنية للمذاب Weight Percentage
النسبة المئوية الوزنية للمذاب هي كتلة المادة المذابة مقاسه بالجرامات الموجودة في مائة جرام من المحلول.
أو
عدد الجرامات من المذاب في 100 g من المحلول.
– ويمكن صياغتها رياضياً كما يلى:
حيث:
كتلة المذيب (msolvent) بوحدة الجرام = m1
كتلة المذاب (msolute) بوحدة الجرام = m2
msol: كتلة المحلول بوحدة الجرام
Wt%m2: النسبة المئوية الوزنية للمذاب (solute)
Wt%m1 : النسبة المئوية الوزنية للمذيب (solvent)
وكتلة المحلول (msol) عبارة عن مجموع كتلتي المذاب (m2) والمذيب (m1):
msol = m1 + m2
ويمكن حساب كتلة المحلول من كثافة المحلول إذا عرف حجم المحلول ، باستخدام العلاقة التالية:
dsol : كثافة المحلول بوحدة (g/L) أو بوحدة (g/ml)
msol : كتلة المحلول بوحدة الجرام (g)
Vsol : حجم المحلول بالوحدات الآتية :
مسائل محلولة النسبة المئوية الوزنية
مثال (1): احسب النسبة المئویة الوزنیة لمادة كلورید الصودیوم (NaCl) (ملح الطعام) حينما يذاب منها (43 g) في (100 g) من الماء ؟
الحل :
مثال (2): حضر محلول بإذابة 1.25 g من الأيثانول C2H5OH في 116 g من الماء H2O
احسب:
1- النسبة المئوية الوزنية للإيثانول.
2- النسبة الوزنية للماء
الحل:
مثال (3): احسب كتلة هيدروكسيد الصوديوم (NaOH) الموجود فى ((300 g من محلول تركيزه (35.7% NaOH)؟
الحل:
مثال (4): يراد عمل محلول مائي من السكروز ذي تركيز قدره 24% وزناً . فكم جراماً من السكروز والماء يجب استخدامها للحصول على كيلو جرام من المحلول؟
الحل :
مثال (5): أحسب عدد مولات HCl الموجودة في 5 cm3 من حمض الكلور المركز الذي كثافته (1.19g/cm3) ويحتوي على 37.23% بالوزن . علماً بأن الأوزان الذرية (H = 1, Cl = 35.5) ؟
الحل :
مثال (6): حمض الكبريت المركز 1.84g/ml يحتوي على 98% وزناً . أحسب حجم حمض الكبريت المركز الذي يحتوي على 40 g من H2SO4 النقي؟
الحل :
أولاً/ نحسب كتلة المحلول msol
تمارين محلولة مباشرة
تمرين (7): ما حجم حمض النيتريك المخفف كثافته 1.11 g/cm3 حيث أن النسبة المئــوية الوزنية لـــ HNO3 هي 19% يحتوي على 10 g من HNO3؟
الجواب النهائي : Vsol = VHNO3 = 47.414 cm3
تمرين (8): كم جراماً من الماء والملح تلزم لتكوين 70 g من محلول نسبته 17.9% وزناً ؟
الجواب النهائي : ( 12.53 g , 57.47 g )
تمرين (9): كم عدد جرامات 5% بالوزن من محلول كلوريد الصوديوم NaCl للحصول على 3.2gNaCl ؟
الجواب النهائي : 64 g
المراجع : النسبة المئوية الوزنية للمذاب Weight Percentage – الفصل الأول / طرق التعبير عن التركيز من كتاب أسس الكيمياءالعامة والفيزيائية للمؤلف / عمر بن عبدالله الهزازي أستاذ قسم الكيمياء كلية العلوم -جامعة أم القري.