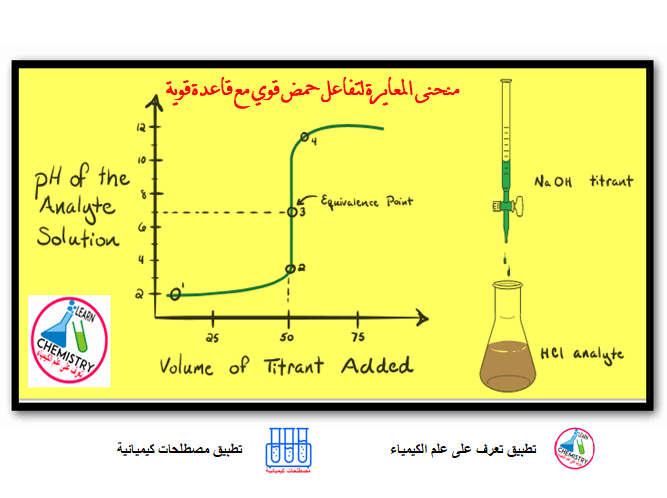
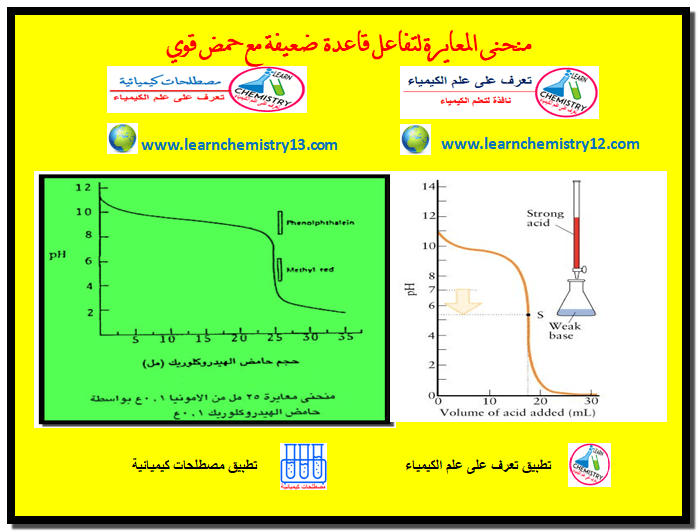
تعيين عيارية وقوة HCl , NaCl في مخلوط منهما باستخدام AgNO3

الأساس النظري
الهدف من التجربة
الأدوات والمواد المطلوبة
خطوات العمل
(1) نظف أدوات التجربة جیداً بالماء المقطر حتى تصبح جاهزة للعمل.
(2) نظف السحاحة قبل ملئها بقلیل من محلول هیدروكسید الصودیوم القیاسي للتخلص من بقایا الماء المقطر ثم املأ السحاحة مع مراعاة عدم وجود فقاعات هواء وامتلأ الجزء ما تحت الصنبور.
(3) خد ماصة 25 مل من محلول قطرات دلیل الفینول نفثالین او دلیل المیثیل البرتقالي .
(4) عایر محلول الخلیط بتنقیط محلول هیدروكسید الصودیوم القیاسي قطرة قطرة مع الرج واستمر في عملیة المعایرة حتى الوصول إلي نقطة نهایة التفاعل أي حتى یتحول لون المحلول من عدیم اللون الى الأحمر في حالة دلیل الفینول نفثالین او من الأحمر إلي الأصفر في حالة دلیل المیثیل البرتقالي وسجل الحجم المستهلك من هیدروكسید الصودیوم ولیكن (V) مل
(5) كرر الخطوات ( 4,3 ) وخد متوسط ثلاثة حجوم (V1) الذي یكافئ حمض الهیدروكلوریك.
(6) خد 25 مل جدیدة من الخلیط في دورق المعایرة ثم أضف إلي الدورق حجم هیدروكسید الصودیوم الذى یكافئ حمض الهیدروكلوریك (V1) ثم أضف قطرات من دلیل كرومات البوتاسیوم.
(7) بعد تنظیف السحاحة من محلول هیدروكسید الصودیوم جیدا تملأ السحاحة بمحلول نترات الفضة القیاسي ویفضل أستخدام سحاحة أخرى نظیفة.
(8) ابدأ عملیة المعايرة بتنقیط محلول نترات الفضة القیاسي قطرة قطرة حتى الوصول نقطة نهایة التفاعل أي حتى ظهور راسب احمر ثابت.
(9) كرر الخطوات ( 8,7 ) وخد متوسط ثلاثة حجوم من محلول نترات الفضة الذى یكافئ كلورید الصودیوم NaCl ولیكن (V2)
الحسابات
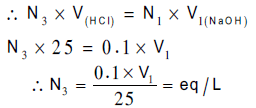
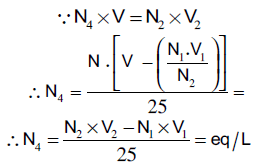
تعليمات السلامة داخل المختبر الكيميائي
يجب عليك قبل بدء التجربة مراعاة الآتي:
(1) يجب مراعاة نظافة المختبر والأدوات المستخدمة به .
(2) يجب عدم إلقاء المواد الكيماوية بالأحواض إلا بعد تخفيفها ، ولا يجوز نهائيا إلقاء قطع أو قشور الصوديوم في الأحواض
(3) يجب أن تكون الأرضيات وكذلك أسطح الطاولات من مواد مقاومة للحريق والمواد الكيماوية وسهلة التنظيف .
(4) يجب غسل الأواني التي بها بقايا مواد سريعة الاشتعال بعد انتهاء العمل بها .
(5) يجب عدم تخزين الكيماويات أو عينات المواد المراد حفظها داخل المختبر إلا بأقل قدر ممكن ولحاجة العمل فقط .
(6) يجب عدم حفظ السوائل السريعة التبخر إلا في الثلاجات ويجب الانتباه عند تغطية زجاجات الكيماويات .
(7) يجب وضع إناء مملوء بالرمل تحت القناني التي لا يوجد سبيل آخر لحمايتها ، واعلم أن استخدام الرمال والتراب لامتصاص الأحماض المنسكبة على الأرض من الوسائل الآمنة من وجهة نظر السلامة .
(8) عند تسخين مواد سريعة الاشتعال يجب استخدام حمام مائي .
(9) لا تحاول أن تدخل بقوة أنبوبة في سدادة فلين أو مطاط ، بلل الزجاج بالماء أو الزيت أولاً لان ذلك يسهل ألي حد كبير هذه العملية .
ويجب أيضاً:
(10) يجب تداول المواد الخطرة حسب الأسس العلمية ، وكمثال عند تخفيف حمض الكبريتيك فأن الحمض يضاف للماء ولا يضاف الماء إليه .
(11) يجب عدم استخدام المواد الخطرة كالفوسفور إلا تحت الإشراف الفعلي لمسئول المختبر ، ومراعاة حفظ الفوسفور الأبيض والأصفر تحت سطح الماء لمنع اشتعالها تلقائيا حيث إنها تشتعل بمجرد تعرضها للهواء
(12) يجب أن يكون بكل مختبر أكثر من مخرج ويفضل أن تكون الأبواب من النوع المفصلي التي تفتح للداخل والخارج
(13) يجب أن يتأكد محضر المختبر من فصل الكهرباء وإغلاق الغاز والماء عند انتهاء العمل بالمختبر يوميا ما لم يكن هناك أجهزة تلزمها الكهرباء باستمرار مثل الثلاجات أو أجهزة تكييف الهواء لظروف معينة .
(14) يجب على محضر المختبر إجراء التفتيش الدوري على توصيلات الغاز والمياه والمجاري والكهرباء للتأكد من سلامتها والإبلاغ عن أي خلل بها فور اكتشافه .
(15) يجب على محضر المختبر التأكد من توفير التهوية المناسبة والإضاءة المناسبة بالمختبر .
(16) يجب التأكد من أن غرفة الغازات (غرفة التجارب) محكمة الغلق لمنع تسرب الغازات الضارة منها أثناء إجراء التجارب الخطرة وان تكون مزودة بمروحة سحب مناسبة.
المراجع: كتاب تجارب في الكيمياء التحليلية (التحليل الكمي الحجمى والوزني) / مسعود فرج أبو سته / كلية العلوم – جامعة سبها.