أسئلة وإجاباتالكيمياءالكيمياء العامة
قانون جاي لوساك للغازات + مسائل محلولة (Gay-Lussac’s Law (P-T relationship

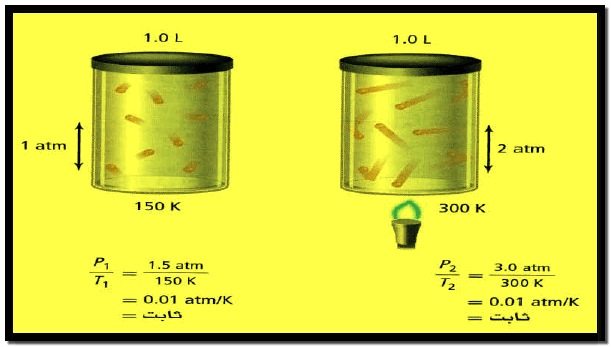
إذا سخن حجم معین من غاز في إناء مغلق ثابت الحجم(صلب مثلاً) فإن الحجم في هذه الحالة لا یتمدد، ولكن سوف تتحرك جزیئاته أكثر مما كانت علیه في الحالة السابقة ویزداد التردد وشدة الضربات مع الجدار أو مع جزيء آخر (violent Collisions) ویعني ذلك أن الضغط سوف یزداد ویعبر عن تلك بالعلاقة بین الضغط ودرجة الحرارة المطلقة عند ثبوت الحجم.
نص قانون جاي لوساك
” یتناسب ضغط (P) كتلة معینة من غاز تناسباً طردیاً مع درجة حرارتھا المطلقة
(T)عند ثبوت الحجم “.
(T)عند ثبوت الحجم “.
The pressure of a fixed amount of gas in a vessel of
constant volume is proportional to the absolute temperature
constant volume is proportional to the absolute temperature

الصيغة الرياضية للقانون

حيث K ثابت الغاز بالنسبة لحجم معین منه ویتغیر بتغیر الحجم عند درجات حرارة مختلفة وعموماً یمكن كتابتھا على الصورة :
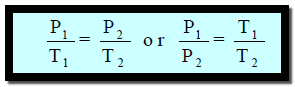
وهذه العلاقة مفیدة في حساب ضغط الغاز عند تسخینه في أواني مغلقة ثابتة الحجم، فنلاحظ مثلاً أن بعض العبوات المغلقة (مثل البخاخات)
یكتب علیھا) لا تخزن فوق 50Co ) وذلك لأنھا عندما تسخن العبوة یزداد ضغط الغاز بالداخل وقد یؤدي ذلك إلى انفجار العبوة.
یكتب علیھا) لا تخزن فوق 50Co ) وذلك لأنھا عندما تسخن العبوة یزداد ضغط الغاز بالداخل وقد یؤدي ذلك إلى انفجار العبوة.
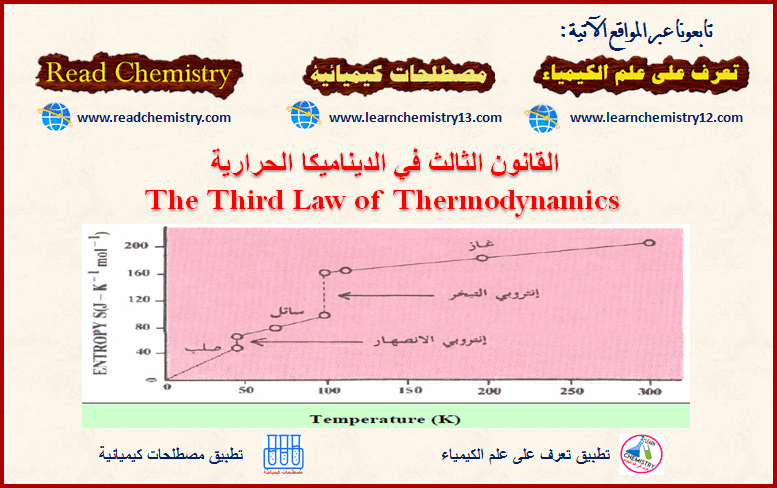
العلاقة البيانية
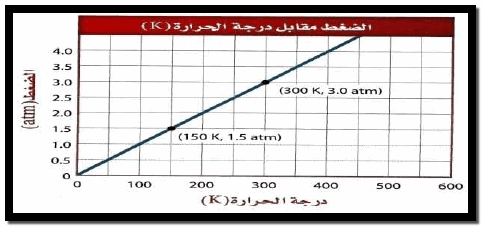
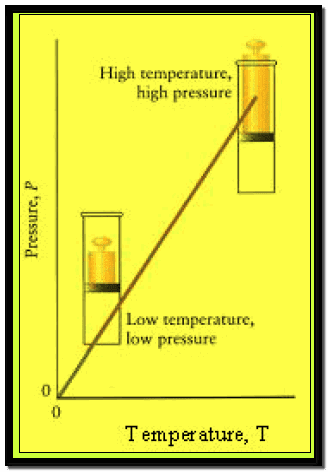
وبرسم العلاقة بین الضغط (P) مقابل درجة الحرارة المطلقة(T) عند ثبوت الحجم نحصل على خط مستقیم وكل خط في المنحنى له میل معین ویكون المیل أقل عندما یكون الحجم أكبر.
مسائل محلولة
الحل:
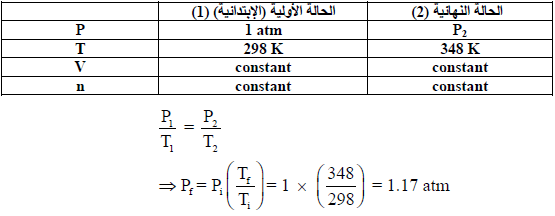
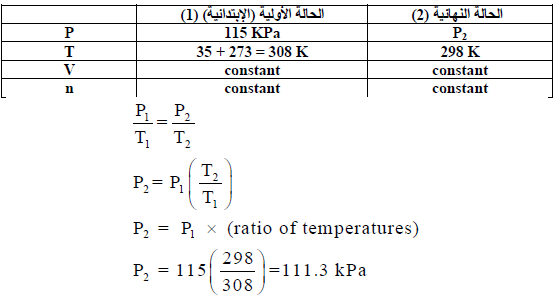
مثال (2): ما ضغط الغاز الذي كان أصلاً 115 KPa ، إذا ما خفضت درجة
الحرارة من 35Co إلى 25Co مع
بقاء الحجم ثابتاً؟
الحرارة من 35Co إلى 25Co مع
بقاء الحجم ثابتاً؟
الحل:
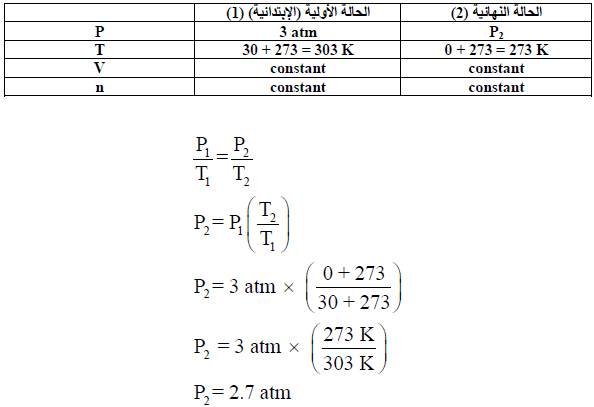
مثال (3): وضعت عينة من غاز في إناء عند 30Co وكان الضغط 3 atm ، فاحسب كم سيكون الضغط لهذه الكمية عند 0Co؟
الحل:
مثال (3): وضعت عينة من غاز في إناء عند 30Co وكان الضغط 3 atm ، فاحسب كم سيكون الضغط لهذه الكمية عند 0Co؟
الحل:

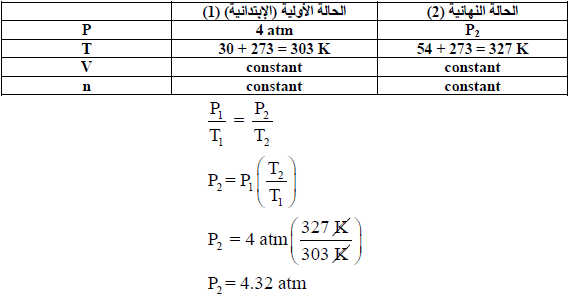
مثال (4): إطار
سيارة يحتوي على هواء ضغطه 4 atm عند 30Co وبعد سير السيارة ارتفعت درجة حرارة الإطار إلى 54Co، فكم سيكون ضغط الهواء داخل الإطار ( بإفتراض ثبات الحجم)؟
سيارة يحتوي على هواء ضغطه 4 atm عند 30Co وبعد سير السيارة ارتفعت درجة حرارة الإطار إلى 54Co، فكم سيكون ضغط الهواء داخل الإطار ( بإفتراض ثبات الحجم)؟
مثال (5): في
إناء مغلق، ما درجة الحرارة اللازمة لتسخین غاز 5Co عند لكي
یتضاعف الضغط ؟
إناء مغلق، ما درجة الحرارة اللازمة لتسخین غاز 5Co عند لكي
یتضاعف الضغط ؟

المراجع
– أسس الكيمياء العامة والفيزيائية- الجزء الأول.عمر بن عبد الله الهزازي ، قسم الكيمياء- كلية العلوم – جامعة أم القرى – المملكة العربية السعودية