الكيمياءعناصر الجدول الدورى
عنصر الكربون Carbon

أولاً:
ما هو عنصر الكربون؟
** الكربون
عنصر من عناصر الجدول الدوري العدد الذري = 6 ، العدد الكتلي
= 12
عنصر من عناصر الجدول الدوري العدد الذري = 6 ، العدد الكتلي
= 12
**
التوزيع الإلكتروني لعنصر الكربون: 2P2
1S2
, 2S2
التوزيع الإلكتروني لعنصر الكربون: 2P2
1S2
, 2S2
** الكربون
عنصر
مميز
لأسباب
عديدة:
عنصر
مميز
لأسباب
عديدة:
(أ) تتضمن أشكاله العديدة مادة من أنعم المواد) الجرافيت)
ومادة من
أقسى
المواد
(الماس)
ومادة من
أقسى
المواد
(الماس)

(ب) لهقابلية
كبيرة
للترابط مع الذرات الأخرى الصغيرة، بما فيها الكربون نفسه وحجمه الصغير يجعله يستطيع تكوين روابط عديدة. ونظراً لذلك فإن الكربون يعرف أنه يكون ما يقرب من 10 ملايين مركب، أي معظم المركبات الكيميائية تقريبا.
كبيرة
للترابط مع الذرات الأخرى الصغيرة، بما فيها الكربون نفسه وحجمه الصغير يجعله يستطيع تكوين روابط عديدة. ونظراً لذلك فإن الكربون يعرف أنه يكون ما يقرب من 10 ملايين مركب، أي معظم المركبات الكيميائية تقريبا.
** مركبات
الكربون
هي الأساس
للحياة
على
الأرض
كما
أن
دورة
كربون – نيتروجين هي السبب في إصدار بع الطاقة الصادرة عن الشمس والنجوم الأخرى.
الكربون
هي الأساس
للحياة
على
الأرض
كما
أن
دورة
كربون – نيتروجين هي السبب في إصدار بع الطاقة الصادرة عن الشمس والنجوم الأخرى.
** الجدول التالي يوضح بعض الخواص العامة لعنصر الكربون:
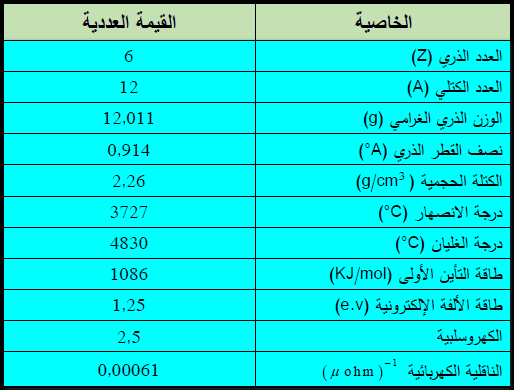
ثانياً:
اكتشافه ووجوده في الطبيعة
** الكربون
تعني
باللغة
اللاتينية Cardo بمعنى Charbon الذي يدل على مصدر الفحم.
تعني
باللغة
اللاتينية Cardo بمعنى Charbon الذي يدل على مصدر الفحم.
**
تم
اكتشاف الكربون قبل
الميلاد
وكان
معروفا
عند
القدماء
الذين
حصلوا
عليه
بحرق
المواد
العضوية
بمعزل
عن
الأكسجين لتصنيع
الفحم
كما
أن
الماس
يعتبر
منذ
القدم
من
المواد
النادرة
والتي
تم
اكتشافها
كمنتج
ثانوي
أثناء تجارب
الشعاع
الجزئي
في
الثمانيات
من
القرن
العشرين.
تم
اكتشاف الكربون قبل
الميلاد
وكان
معروفا
عند
القدماء
الذين
حصلوا
عليه
بحرق
المواد
العضوية
بمعزل
عن
الأكسجين لتصنيع
الفحم
كما
أن
الماس
يعتبر
منذ
القدم
من
المواد
النادرة
والتي
تم
اكتشافها
كمنتج
ثانوي
أثناء تجارب
الشعاع
الجزئي
في
الثمانيات
من
القرن
العشرين.
**
يشكل
الكربون
حوالي
0.08%
من
وزن
القشرة
الأرضية.
يشكل
الكربون
حوالي
0.08%
من
وزن
القشرة
الأرضية.
** يدخل الكربون
في
تركيب
الغلاف
الجوي
بنسبة 0.03%
حجماً يشكل CO2
في
تركيب
الغلاف
الجوي
بنسبة 0.03%
حجماً يشكل CO2
**
الكربون
عنصر
هام
يدخل في
تركيب
النسيج
الحيواني
والنباتي
ويعتبر
العنصر الأساسي
الذي
تتكون
منه
البقايا
الجيولوجية
مثل
البترول
والفحم
الحجري.
الكربون
عنصر
هام
يدخل في
تركيب
النسيج
الحيواني
والنباتي
ويعتبر
العنصر الأساسي
الذي
تتكون
منه
البقايا
الجيولوجية
مثل
البترول
والفحم
الحجري.
**
أهم خامات الكربون:
أهم خامات الكربون:
(1) يوجد على شكل كربونات معدنية
أهمها الحجر الكلسي CaCO3
– أحجار الدولوميت CuCO3.MgCO3
– السيدريت FeCO3
– والوزريت BaCO3
– والملاغيت 2CuCO3.Cu(OH)
أهمها الحجر الكلسي CaCO3
– أحجار الدولوميت CuCO3.MgCO3
– السيدريت FeCO3
– والوزريت BaCO3
– والملاغيت 2CuCO3.Cu(OH)
(2) يمكن للكربون أن يوجد في الطبيعة بشكل حر مثل الماس والجرافيت.
(3) يوجد بالإضافة إلى ذلك عدة أشكال مسامية من الكربون مثل فحم الكوك وفحم الخشب والفحم الحجري وغير ذلك من الفحوم التي تشابه الجرافيت في صفاته.
ثالثاً:
الخواص الكيميائية لعنصر الكربون
يعتبر الكربون عنصراً قليل الفعالية في درجات
الحرارة العادية، لكنه يتفاعل مع العديد من العناصر في الدرجات العالية لينتج عددا هائلا من المركبات حيث إنّ معظم هذه المركبات تصنف على أنها مركبات عضوية.
الحرارة العادية، لكنه يتفاعل مع العديد من العناصر في الدرجات العالية لينتج عددا هائلا من المركبات حيث إنّ معظم هذه المركبات تصنف على أنها مركبات عضوية.
(1) تفاعل الكربون
مع الأكسجين
يحترق
الكربون بالحرارة وفي جو من الأكسجين ليعطي غاز أحادي أكسيد الكربون أو غاز ثنائي أكسيد الكربون وذلك حسب كمية الأكسجين المستعملة:
الكربون بالحرارة وفي جو من الأكسجين ليعطي غاز أحادي أكسيد الكربون أو غاز ثنائي أكسيد الكربون وذلك حسب كمية الأكسجين المستعملة:
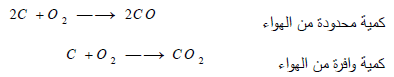
(2) تفاعل
الكربون مع أشباه المعادن
(أ)
التفاعل مع الكبريت
التفاعل مع الكبريت
يتفاعل الكربون مع الكبريت ليشكل ثنائي كبريتيد الكربون CS2 وهو سائل سام سريع الاشتعال حسب التفاعل التالي:
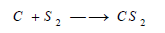
(ب)
التفاعل مع الهالوجينات
التفاعل مع الهالوجينات
يمكن أن يشكل الكربون مركبات هالوجينية بصورة مباشرة ولكنه يمكن أن يشكل رباعي فلوريد الكربون بالتفاعل المباشر بين الفلور والكربون بالحرارة العالية:
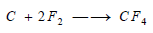
(جـ)
التفاعل مع الهيدروجين
التفاعل مع الهيدروجين
يتحد الكربون مع الهيدروجين في درجات الحرارة العالية معطياً غاز الميثان حسب التفاعل التالي:
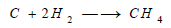
(د)
التفاعل مع النيتروجين
التفاعل مع النيتروجين
يشكل الكربون مع النيتروجين مركبات عديدة أبسطها هو غاز السيانوجين C2N2
(3) الخواص
الاختزالية للكربون
لما كان الكربون ذا علاقة شديدة بالأكسجين فهو يسعى إلى انتزاعه من الأجسام وبالتالي يعد جسما مرجعا قوياً
(أ)
أختزال الكربون للأكاسيد المعدنية
أختزال الكربون للأكاسيد المعدنية
يختزل
الكربون الأكاسيد المعدنية وينطلق غازCO ،
CO2 وذلك حسب موقع المعدن في السلسلة الكهروكيميائية وحسب درجة الحرارة وحسب شدة العلاقة بين المعدن والأكسجين:
الكربون الأكاسيد المعدنية وينطلق غازCO ،
CO2 وذلك حسب موقع المعدن في السلسلة الكهروكيميائية وحسب درجة الحرارة وحسب شدة العلاقة بين المعدن والأكسجين:
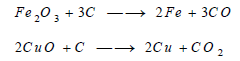
(ب)
أختزال الكربون للأحماض المؤكسدة
أختزال الكربون للأحماض المؤكسدة
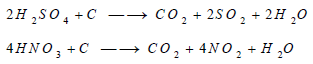
(جـ)
أختزال الكربون لبخار الماء
أختزال الكربون لبخار الماء
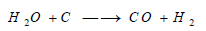
المراجع: دراسة كيميائية تحليلية مفصلة لعناصر الجدول الدوري / الأستاذ الدكتور حسن بوزيّان أستاذ بقسم الكيمياء بالمدرسة العليا للأساتذة / الجزء الأول / أبريل 2017 / الجزائر






