معلومات هامة جداً عن الكالسيوم Calcium
ما هو عنصر الكالسيوم Calcium؟
– الكالسيوم Ca هو عنصر من عناصر الجدول الدوري: العدد الذري = 20 ، العدد الكتلي = 40
– يرمز له بالرمز 40Ca20
– التوزيع الإلكتروني له : 1S2 , 2S2 2P6 , 3S2 3P6 , 4S2
– عبارة عن معدن أبيض فضي، يزول هذا اللون بالتعرض للهواء نتيجة تأكسده.
– عنصر طري نسبياً.
– كما يتمتع بناقلية جيدة التيار الكهربائي وللحرارة.
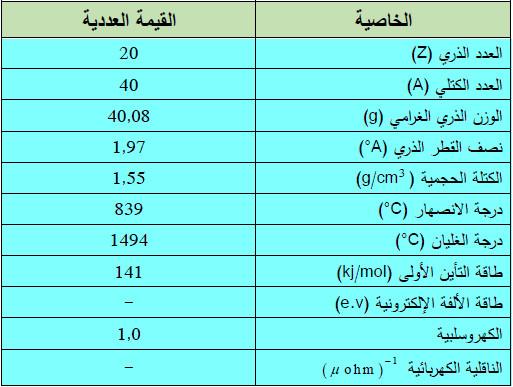
– الجدول التالي يوضح بعض الخواص العامة لهذا العنصر:
اكتشافه ووجوده في الطبيعة Discovery of Calcium
– اكتشف Ca عام 1808م على يد (ديفي Davy) في بريطانيا، كما اشتق اسمه من اللاتينية Calx بمعنى الجير.
– يعتبر هذا المعدن من أوسع العناصر الأساسية انتشاراً في القشرة الأرضية، فهو يؤلف حوالي 3.7% من وزنها.
– وهو لا يوجد يشكل حر في الطبيعة وذلك لشدة فعاليته، ولكن فلزاته واسعة الانتشار في اليابسة ومياه البحر.
– وأهم فلزاته تكون بشكل كربونات مثل الحجر الكلسي والرخام والطباشير، كما يوجد على شكل كبريتات كالجبس CaSO4.2H2O والفوسفات 2(Ca3(PO4، والفلورسبار CaF2 والأنهدريت CaSO4
تحضير الكالسيوم Preparation of Calcium
– يتم تحضير Ca بعدة طرق أهمها:
(1) اختزال كلوريد الكالسيــوم لمعدن الصوديوم
CaCl2 + 2Na → Ca + 2NaCl
(2) اختزال أكاسيد الكالسيــوم بواسطة الألمنيوم
تفاعلات الكالسيوم Chemical properties of Calcium
(1) التفاعل مع الأكسجين
عند تسخين Ca في جو من الأكسجين يتشكل أكسيد الكالسيوم كما هو مبين في التفاعل التالي:
(2) التفاعل مع الماء
يتفاعل Ca بسهولة وينطلق غاز الهيدروجين كما هو مبين في التفاعل التالي:
(3) التفاعل مع الهيدروجين
يتفاعل Ca بالتسخين مع الهيدروجين ويتشكل هيدريد الكالسيوم وهو مركب ثابت في الظروف الطبيعية.
(4) التفاعل مع أشباه المعادن
(أ) التفاعل مع النيتروجين
يتفاعل Ca مع النيتروجين بالتسخين إلى درجات مناسبة ويتشكل مركب نتريد الكالسيوم ذو الصيغةCa3N2 ، وهو مركب يتميأ بسرعة في الماء ويتشكل هيدروكسيد الكالسيوم وينطلق غاز النشادر كما هو مبين فى التفاعل التالي:
(ب) التفاعل مع الكربون
يتفاعل Ca بالتسخين مع الكربون ويتشكل كربيد الكالسيوم ذو الصيغة CaC2 ويتصف هذا المركب بأنه يتحلمه بالماء ويتشكل هيدروكسيد الكالسيوم وينطلق غاز الأستيلين كما هو مبين فى التفاعل التالي:
(جـ) التفاعل مع الفوسفور
يتفاعل Ca مع الفوسفور بالحرارة ويتشكل فوسفيد الكالسيوم Ca3P2، والذي يتميأ بسرعة بالماء ويتشكل هيدروكسيد الكالسيـوم وينطلق غاز الفوسفين كما هو مبين فى التفاعل التالي:
(د) التفاعل مع الهالوجينات
يتفاعل Ca مع الهالوجينات جميعها ويتشكل هاليد الكالسيوم CaX2
(5) التفاعل مع الأحماض
يتفاعل Ca مع الاحماض المعدنية وينطلق غاز الهيدروجين كما يلي:
أما حمض الكبريت الكثيف والساخن فيتفاعل معه وينطلق غاز ثنائي أكسيد الكبريت:
(6) التفاعل مع النشادر
يتفاعل Ca مع النشادر السائل ويتشكل أميد الكالسيــوم بوجود وسيط مناسب كما يلي:
أما مع غاز النشادر وبدرجة حرارة عالية فيتفاعل مشكلاً نتريد الكالسيــوم كما بالمعادلة الآتية:
(7) تشكيل المعقدات الكيميائية
يمكن للـ Ca أن يشكل العديد من المعقدات الكيميائية منهـا
وللشاردة الموجبة في هذه المعقدات شكل رباعي الوجوه مع أربعة روابط تناسقية بين ذرات الأكسجين وشاردة 2+Ca.
استخدامات الكالسيوم Uses of Calcium
– يستعمل Ca كعامل مختزل وخاصة عند تحضير المعادن النادرة مثل الثوريوم والزركونيوم.
– يستعمل هيدروكسيد الكالسيوم في تحضير النشادر.
– يلعب Ca دوراً هاماً في صناعة السكر.
– استخدامه لتلف جثث بعض الحيوانات.
– يستعمل في صناعة كربيد الكالسيوم المستعمل لتحضير الأسيتيلين:
– كما يستعمل في البناء حيث يخلط مع الرمل والماء.
– تستخدم كربونات الكالسيــوم في صناعة الزجاج وفي صناعة الاسمنت.
– أما كلوريد الكالسيــوم فيستخدم كمادة مجففة للغازات ماعدا النشادر.
المراجع: دراسة كيميائية تحليلية مفصلة لعناصر الجدول الدوري / الأستاذ الدكتور حسن بوزيّان أستاذ بقسم الكيمياء بالمدرسة العليا للأساتذة / الجزء الأول / أبريل 2017 / الجزائر.