الكيمياء العضوية
الأميدات Amides (التسمية – التحضير – الخواص الفيزيائية و الكيميائية)

تعريف الأميدات Definition of Amides
– الأميدات Amides هي النوع الرابع من مشتقات الأحماض الكربوكسيلية وفيها استبدلت بمجموعة الهيدروكسيل الخاصة بالأحماض مجموعة أمين.
– تعتبر الأميدات من مشتقات الأحماض الكربوكسيلية وذلك لأنه عند التحلل المائي للأميدات فأنها تعطي أحماضاً كربوكسيلية.
– المجموعة الوظيفية هي مجموعة Acyl group ولها الصيغة (-R-CO) مرتبطة بذرة نيتروجين كما يلي:
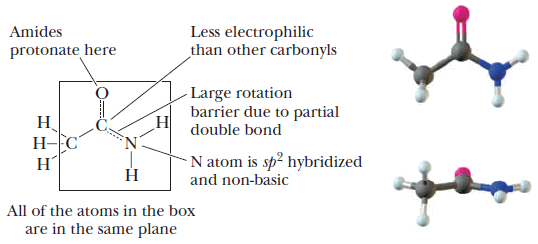
– كما يمكن أن تكون الأميدات أحادية أو ثنائية التفرع على ذرة النيتروجين.

– ومن ضمن مشتقات الأحماض تعتبر الأميدات أقلها فاعلية less reactive
تسمية الأميدات midesNomenclature of a
تشتق أسماء الأميدات من الأسماء النظامية للأحماض الكربوكسيلية باستبدال المقطع oic acid بكلمة amide أو باستبدال المقطع ic acid من الأسماء الشائعة للأحماض الكربوكسيلية بكلمة أميد . amide
أمثلة:
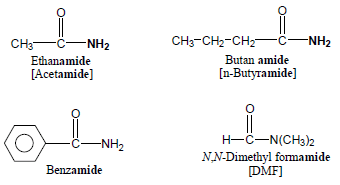
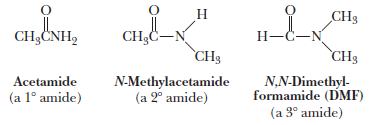
أما في الأميدات التي تتصل فيها مجموعة الكربونيل بمركب حلقى يستبدل المقطع ylic acid بكلمة أميد amide
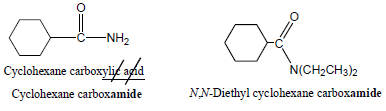
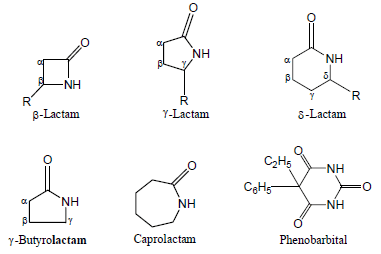
الأميدات الحلقية Lactams
عند وجود أمين على أحدي ذرات كربون β أو γ أو δ في جزئ الحمض الكربوكسيلي يحدث نزع جزئ ماء داخل الجزئ ويتكون أميد حلقي بنفس الطريقة التي تكونت بها الأسترات الحلقية.
أمثلة:
أمثلة:
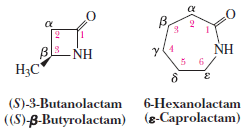
تحضير بعض الأميدات الهامةPreparation of some important Amides
(1) الأسيتاميد Acetamide
تحضر الاميدات بإحدى الطرق التالية ، فمثلاً يمكن تحضير الأسيتاميد بالطرق الآتية:
(أ) بتسخين خلات الامونيوم في وجود حمض الخليك:
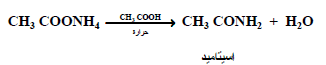
(ب) من تفاعل الامونيا مع كلوريدات الأحماض أو الانهيدريدات أو الاسترات:
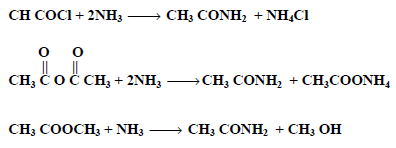
(2) كابرولاكتام Caprolactam
ويمكن تحضيرها بالطرق الآتية:
(أ) من الألكانات الحلقية:
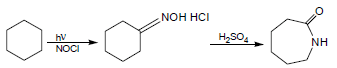
(ب) من الكيتونات الحلقية:
عند تفاعل Cyclohexanone مع NH2OH ومعالجة الناتج بحمض الكبريتيك تحدث عملية إعادة ترتيب تعرف Beckmann rearrangment فينتج كابرولاكتام ويستعمل في تحضير Nylon 6
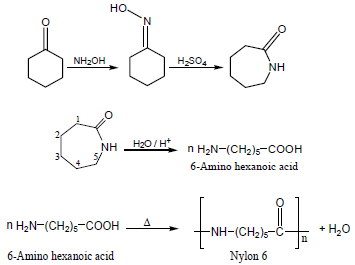
(3) فينوبربيتال Phenobarbital
يستعمل في الطب كمسكن للآلام
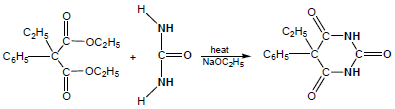
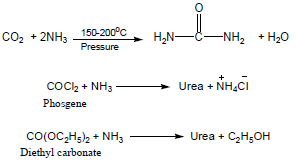
(4) اليوريا Urea
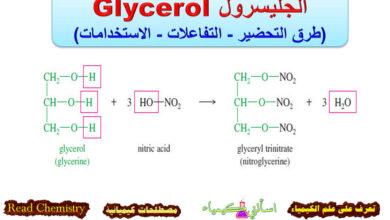
– تعتبر اليوريا من أهم أنواع الأميدات وتصنع بتفاعل الأمونيا مع ثاني اكسيد الكربون مع التسخين والضغط وتستخدم كسماد للأراضي الزراعية وفي صناعة بعض الأدوية وتدخل في صناعة بعض أنواع اللدائن وتحضر بعدة طرق منها ما يلي :-
– يعرف التركيب الذي يحتوي على كل من الشحنة الموجبة والسالبة على نفس الجزئ بالأيونات الأمفوتيرية أو آيونات زويتر Zwitter ions
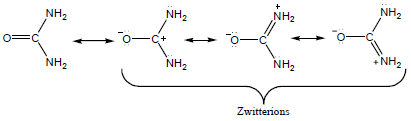
– تتفاعل اليوريا مع حمض النيتروز وينتج النيتروجين.
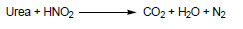
الخواص الفيزيائية للأميدات Physical properties of Amides
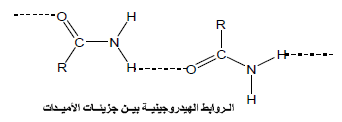
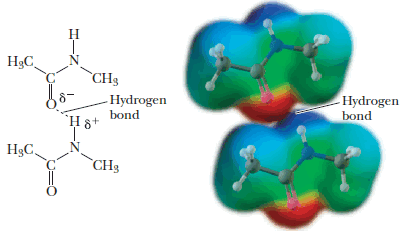
– الأميدات مركبات قطبية تعمل من خلالها ظاهرة الرابطة الهيدروجينية ولذا فإن معظم الأميدات تكون مواد صلبة لها درجات انصهار مرتفعة كما أنها تذوب إلى حد معين في الماء أكثر من مثيلاتها من الإسترات.
– وبالرغم من أن الأميدات تحتوي على مجموعة أمين ، فليست لها صفة قاعدية وذلك لوجود مجموعة الكربونيل الحمضية التي تعادل كل منها تأثير الأخرى ، لذا تعتبر الأميدات مواد أمفوتيرية تسلك كقواعد أو أحماض ضعيفة.
– للأميدات الأولية والثانوية درجات غليان مرتفعة وذلك بسبب مقدرتها على تكوين روابط هيدروجينية بين جزيئاتها أما الأميدات الثالثية لها درجات غليان أقل لعدم مقدرتها على تكوين روابط هيدروجينية بين جزيئاتها.
الخواص الكيميائية للأميدات Chemical properties of Amides
ومن ضمن مشتقات الأحماض تعتبر الأميدات أقلها فاعلية less reactive
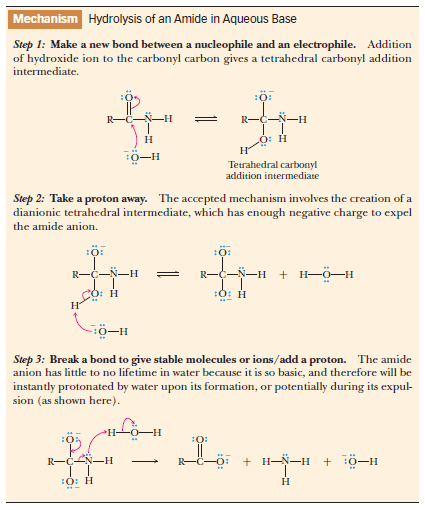
(1) التحلل المائي للأميدات Hydrolysis of Amides
تحلل الأميدات في الوسطين الحمضي والقاعدي إلا أنها تحتاج لظروف خاصة بسبب قلة نشاطها. حيث يمكنها التحلل مائياً بغليها مع حمض أما قاعدة مخففة وفي حالة استخدام حمض يكون الناتج في صورة حمض أما في حالة استخدام القواعد فيتكون ملح الحمض:
(أ) التحلل في الوسط الحمضي:
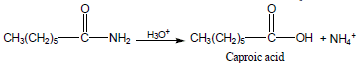
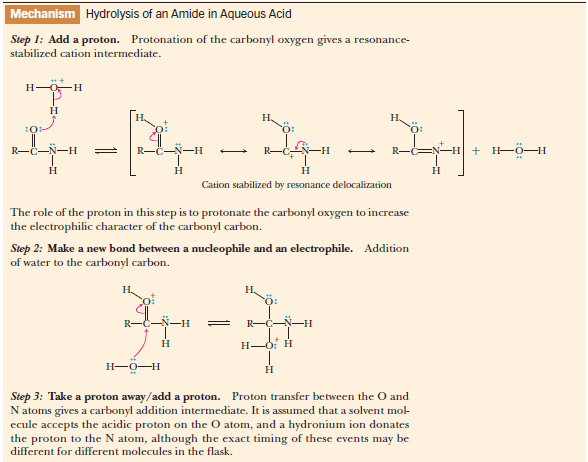
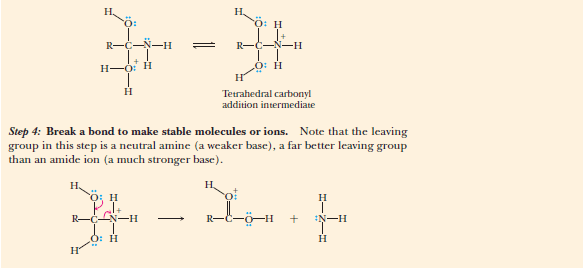
(ب) التحلل في الوسط القاعدي:
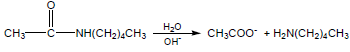
(2) أختزال الإسترات Reduction of Amides
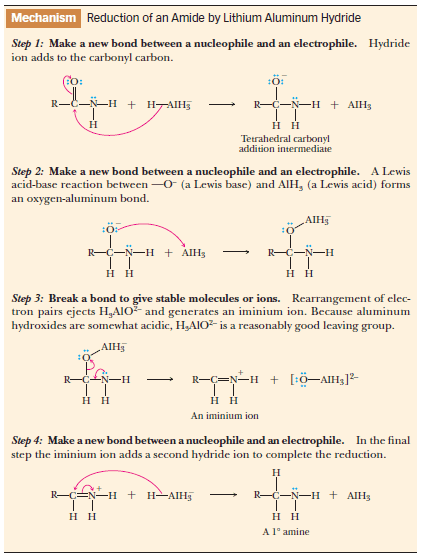
كما تختزل الاميدات بواسطة هيدريد ليثيوم الومنيوم إلى الأمينات المقابلة والمشتملة على نفس عدد ذرات الكربون
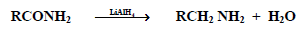
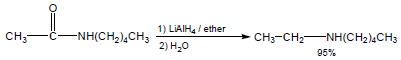
(3)تفاعل نزع الماء Dehydration of Amides
– كما يمكن أن تحول الأميدات الأولية إلى nitriles عن طريق نزع جزئ ماء باستخدام الكواشف التالية:
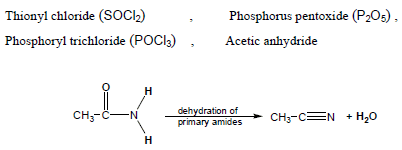
– تستخدم مركبات Nitriles في تحضير المواد العضوية مثل الأسترات والأميدات والكيتونات وغيرها كما يستخدم Acetonitrile كمذيب قطبي غير بروتوني وذلك لأن له ثابت عزل كهربي يساوي 38 تقريباً.
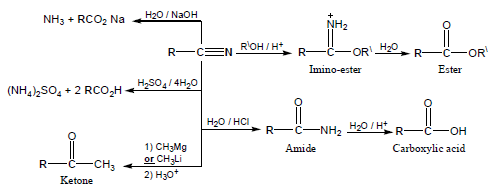
(4) تفاعل نزع مجموعة الكربونيل
هو تفاعل لتحضير الأمينات
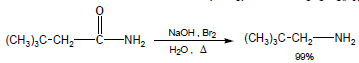
(5) تفاعل الأميدات مع حمض النيتروز Reaction between Amides and Nitrous acids
كما تتفاعل الأميدات غير المتفرعة مع حمض النيتروز ليتكون حمض كربوكسيلي وتصاعد غاز النيتروجين:
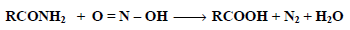
(6) تفاعل هوفمان للأميدات Hofmann rearrangement
عند تفاعل الأميدات غير المتفرعة مع البروم في وجود هيدروكسيد الصوديوم يتكون أمين أولي يقل عن الاميد بذرة كربون واحدة.
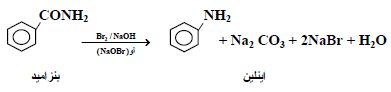
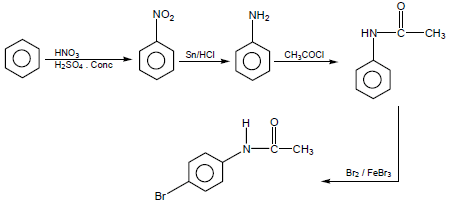
تمرين: كيف تقوم بتحويل:
Benzene→N-(p-Bromo phenyl)acetamide
الحل:
المراجع :
– أسس الكيمياء العضوية . وائل غالب محمد – وليد محمد السعيطي ، الطبعة الأولى (2008) / دار الكتب الوطنية – بنغازي – لبيبا
– أساسيات الكيمياء العضوية. محمد مجدي واصل ، جامعة الأزهر – جمهورية مصر العربية
Organic chemistry / William H. Brown , Christopher S. Foote , Brent L. Iverson , Eric V. Anslyn , Bruce M. Novak . ( sixth edition) . United States
– أساسيات الكيمياء العضوية. محمد مجدي واصل ، جامعة الأزهر – جمهورية مصر العربية
Organic chemistry / William H. Brown , Christopher S. Foote , Brent L. Iverson , Eric V. Anslyn , Bruce M. Novak . ( sixth edition) . United States

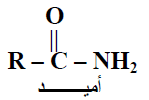




من حمض الاستيك كيف تحصل على الاسيتاميد؟