الأنيلين Aniline – تجربة تحضير الأنيلين فى المعمل
محتويات الموضوع
تجربة تحضير الأنيلين فى المعمل Preparation of Aniline
يمكن تحضير الأنيلين فى المعمل بطريقتين كما يلي:
(1) اختزال النيتروبنزين Reduction of Nitrobenzene
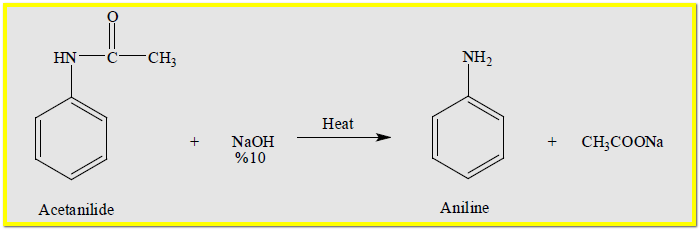
(2) التحلل المائي للاسيتانيليد Hydrolysis of Acetanilide
الطريقة الأولي لتحضير الأنيلين فى المعمل
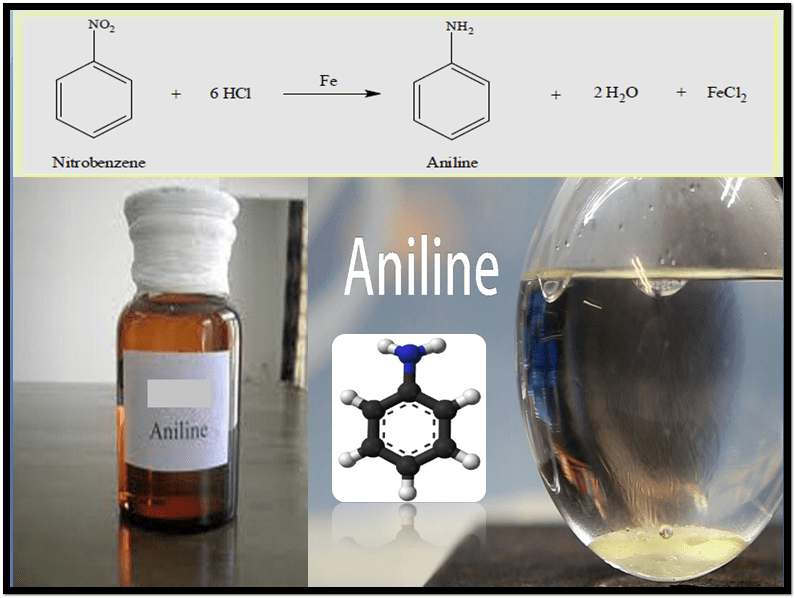
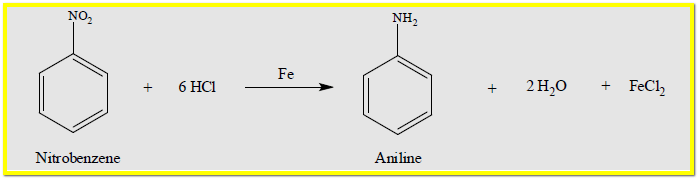
في هذه الطريقة يتم تحضير الأنيلين بواسطة اختزال النيتروبنزين Reduction of Nitrobenzene بوجود حمض المركز HCl وأحد الفلزات Fe , Sn , Zn
أولاً/ الجزء النظري
– يحضر الأنيلين عن طريق اختزال النيتروبنزين بوجود حمض المركز HCl وأحد الفلزات وهي الحديد Fe أو القصدير Sn أو الخارصين Zn
– حيث يتم اختزال النيتروبنزين عن طريق تحويل العنصر الفلزي إلى أيونات وتحرير الالكترونات التي تضاف الى مجموعة النيترو –NO2 فتتحول إلى جذر حر ايوني.
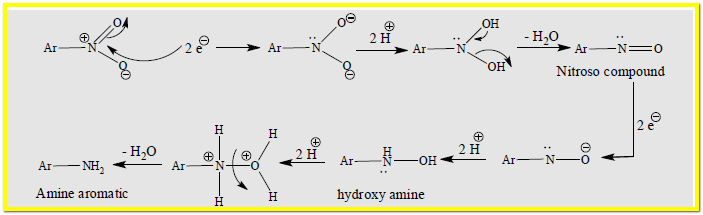
– يمكن تمثيل خطوات الأختزال كما بالمعادلة الآتية:
– من ميكانيكية التفاعل يمكن أن ندرك أن عملية تحضير الانيلين تتم بخطوتين وهي كما يلي:
(1) إضافة إلكترون
(2) إضافة البروتون
– إن اختزال مجموعة النيترو هي من التفاعلات المعقدة وتمر بعدة مراحل كما يتم فصل المواد الوسطية تحت ظروف معينة ولكنها في النهاية تؤدي إلى الاختزال التام لمجموعة النيترو وتحويلها إلى مجموعة الامين –NH2
– يعتبر الانيلين من قواعد لويس لأنه يحتوي مزدوج الكتروني على النتروجين وترتبط ذرة النتروجين مباشرة بالحلقة .
– إن الانيلين من المواد السامة جداً وهو سائل عديم اللون ولكنه يتأكسد مباشرة بالهواء الجوي ويصبح مادة سوداء اللون مائلة إلى الاحمرار وغير قطبية تكون روابط هيدروجينية فيما بينها ولهذا لها درجات غليان عالية ولكنها أقل درجة غليان من الكحولات والأحماض الكربوكسلية .
ثانياً/ الأدوات والمواد الكيميائية المطلوبة
الأجهزة والأدوات
– يتم توفير الأدوات الآتية كما يلي:
- دورق دائري 500ml
- مكثف عاكس
- ورق ترشيح
- قمع فصل
- بيكر سعة 250ml
المواد الكيميائية المطلوبة
– يتم توفير المواد الكيميائية الآتية كما يلي:
- برادة حديد أو صفائح الزنك أو القصدير
- أسيتون
- نتروبنزين
- حمض HCl المركز
- هيدروكسيد الصوديوم
- كلوريد الصوديوم
- أيثر
ثالثاً/ خطوات العمل Procedure
(1) ضع 30g من برادة الحديد او القصدير في بيكر وأضف إليها 15 ml من الأسيتون للتنظيف، رج الخليط لبضع دقائق.
(2) انقل الأسيتون إلى دورق أخر وجفف البرادة بواسطة أوراق ترشيح أو باستعمال فرن واطئ الحرارة.
(3) أضف البرادة الجافة إلى دورق دائري سعة 500 ml وأضف إليها 15 ml من النتروبنزين.
(4) ثبت مكثفا عاكسا على الدورق دون أن تمرر الماء فيه.
(5) انقل 75 ml من حامض HCl المركز وصب حوالي 15 ml في كل مرة من هذا الحامض خلال المكثف ثم رج الدورق .يصب المزيج ساخنا ثم يصبح التفاعل شديدا وعندما يغلي المحلول بشدة اخفض شدة التفاعل بغمر الدورق في الماء البارد.
(6) بعد إضافة كل الحامض وبعد انتهاء التفاعل السريع .سخن المزيج على حمام مائي لمدة (60-30) دقيقة أي حتى تختفي رائحة النيتروبنزين.
(7) برد مزيج التفاعل إلى درجة حرارة المختبر. وأضف تدريجيا محلولا مكونا من 50 g هيدروكسيد الصوديوم في 75ml من الماء .ما فائدةNaOH ؟
(8) اربط الدورق إلى جهاز تقطير البخاري.
(9) أضف إلى مزيج الانيلين والماء الناتج من التقطير البخاري 25 g من كلوريد الصوديوم NaCl في قمع فصل.
(10) أضف 25 ml من الايثر. رج ثم افصل وكرر عملية الفصل.
(11) بخر الايثر ثم قطر الانيلين باستخدام اللهب المباشر أو الحمام الهوائي وأجمع المتقطر بين (184 – 180) Co
الطريقة الثانية لتحضير الأنيلين فى المعمل
في هذه الطريقة يتم تحضير الأنيلين بواسطة التحلل المائي للاسيتانيليد Hydrolysis of Acetanilide
أولاً/ الجزء النظري
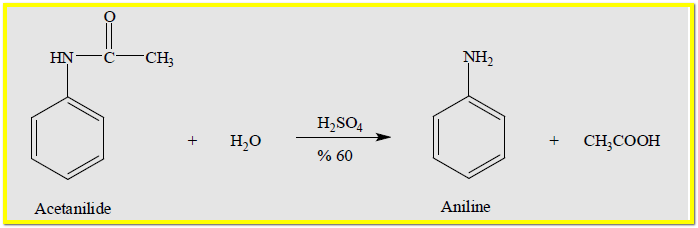
– يتحلل الاسيتانيليد فى الماء بوجود H2SO4 60% ليعطي الانيلين وحمض الخليك كما بالمعادلة الآتية:
– كما يمكن أن يتحلل الاسيتانيليد في الوسط القاعدي كما في المعادلة التالية:
ثانياً/ الأدوات والمواد الكيميائية المطلوبة
– يتم توفير الأدوات والمواد الآتية كما يلي:
- أنبوبة اختبار
- مصدر تسخين
- الاسيتانيليد
- هيدروكسيد الصوديوم
- ورقة عباد الشمس الحمراء.
ثالثاً/ خطوات العمل Procedure
(1) ضع 0.5g من الاسيتانيليد في أنبوبة أختبار.
(2) أضف 4ml من هيدروكسيد الصوديوم 10% إلى الأنبوبة.
(3) سخن المزيج إلى درجة الغليان.
(4) لاحظ رائحة الغاز المتحرر وافحص الغاز بوضع قطعة من ورقة عباد الشمس الحمراء الرطبة ولاحظ تغير لون الورقة.
تعليمات السلامة داخل المختبر الكيميائي
يجب عليك قبل بدء التجربة مراعاة التعلميات الآتية كما يلي:
(1) يجب مراعاة نظافة المختبر والأدوات المستخدمة به.
(2) يجب عدم إلقاء المواد الكيماوية بالأحواض إلا بعد تخفيفها. ولا يجوز نهائيا إلقاء قطع أو قشور الصوديوم في الأحواض.
(3) كما يجب أن تكون الأرضيات وكذلك أسطح الطاولات من مواد مقاومة للحريق والمواد الكيماوية وسهلة التنظيف.
(4) يجب غسل الأواني التي بها بقايا مواد سريعة الاشتعال بعد انتهاء العمل بها.
(5) يجب عدم تخزين الكيماويات أو عينات المواد المراد حفظها داخل المختبر إلا بأقل قدر ممكن ولحاجة العمل فقط.
(6) كما يجب عدم حفظ السوائل السريعة التبخر إلا في الثلاجات. ويجب الانتباه عند تغطية زجاجات الكيماويات.
(7) يجب وضع إناء مملوء بالرمل تحت القناني التي لا يوجد سبيل آخر لحمايتها. واعلم أن استخدام الرمال والتراب لامتصاص الأحماض المنسكبة على الأرض من الوسائل الآمنة من وجهة نظر السلام.
(8) عند تسخين مواد سريعة الاشتعال يجب استخدام حمام مائي.
(9) لا تحاول أن تدخل بقوة أنبوبة في سدادة فلين أو مطاط. بلل الزجاج بالماء أو الزيت أولاً لان ذلك يسهل ألي حد كبير هذه العملية.
أحتياطات أخرى
(10) يجب تداول المواد الخطرة حسب الأسس العلمية. وكمثال عند تخفيف حمض الكبريتيك فأن الحمض يضاف للماء ولا يضاف الماء إليه.
(11) يجب عدم استخدام المواد الخطرة كالفوسفور إلا تحت الإشراف الفعلي لمسئول المختبر. ومراعاة حفظ الفوسفور الأبيض والأصفر تحت سطح الماء لمنع اشتعالها تلقائياً حيث إنها تشتعل بمجرد تعرضها للهواء.
(12) كما يجب أن يكون بكل مختبر أكثر من مخرج. ويفضل أن تكون الأبواب من النوع المفصلي التي تفتح للداخل والخارج.
(13) يجب أن يتأكد محضر المختبر من فصل الكهرباء وإغلاق الغاز والماء عند انتهاء العمل بالمختبر يومياً ما لم يكن هناك أجهزة تلزمها الكهرباء باستمرار مثل الثلاجات أو أجهزة تكييف الهواء لظروف معينة.
(14) يجب على محضر المختبر إجراء التفتيش الدوري على توصيلات الغاز والمياه والمجاري والكهرباء للتأكد من سلامتها والإبلاغ عن أي خلل بها فور اكتشافه.
(15) كما يجب على محضر المختبر التأكد من توفير التهوية المناسبة والإضاءة المناسبة بالمختبر.
(16) يجب التأكد من أن غرفة الغازات (غرفة التجارب) محكمة الغلق لمنع تسرب الغازات الضارة منها أثناء إجراء التجارب الخطرة وأن تكون مزودة بمروحة سحب مناسب.
المراجع: تجارب فى الكيمياء العضوية. أسعد هاشم عنيد – حيدر مصطفي كمال – نهي سلمان صالح – أحمد حسون مجيد ، الطبعة لأولى (2015م) / جامعة الكوفة – كلية العلوم – العراق