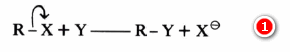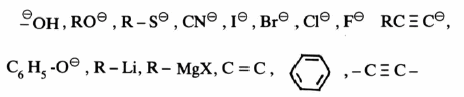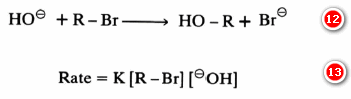تفاعلات الاستبدال النيكليوفيلية SN1 ، SN2
تفاعلات الاستبدال النيكليوفيلية على ذرة الكربون المشبعة
Nucleophilic Substitution at a Saturated Carbon Atom
– تعتبر تفاعلات الاستبدال النيكليوفيلية في المركبات الأليفاتية من أبسط وأهم أصناف التفاعلات العضوية ، ويرجع ذلك إلى أهمية هذه التفاعلات في الصناعة والتحضيرات المعملية.
– لقد حازت تفاعلات الاستبدال النيكليوفيلي هذه على قسط كبير من الاهتمام والدراسة التفصيلية. ونخص بالذكر أعمال انقـولـد Ingold ومدرسته في هذا الشأن.
كيف تحدث تفاعلات الاستبدال النيكليوفيلية (ميكانيكية التفاعل)
– تفاعلات الاستبدال النيكليوفيلية هي تلك التفاعلات التي يهاجم فيها العامل النيكليوفيلي Nucleophile ، (وهو الذي يحمل زوجاً من الإلكترونات الحرة أو شحنة سالبة) ذرة الكربون المشبعة (Substrate) ، ويقوم الزوج الإلكتروني بتكوين الرابطة الجديدة، وعندئذ تغادر المجموعة الخارجة (Leaving group) حاملة زوجها الإلكتروني.
– مثال:
– يجب التنويه هنا إلى أن التفاعلات النيكليوفيلية تفاعلات قطبية حيث:
(1) تقوم المجموعة الخارجة (X-) ذات الكهروسالبية العالية بجذب الإلكترونين المكونين للرابطة بين ذرة الكربون والمجموعة X
(2) تصبح هذه المجموعة الخارجة حاملة لشحنة جزئية سالبة (-δ) بينما تحمـل ذرة الكـربـون شحنـة جزئية موجبة (+δ) مما يسهل على العامل النيكليوفيلي الهجوم على ذرة الكربون وهذا يسبب خروج المجموعة X ـ وهي تحمل زوج إلكترونات الرابطة.
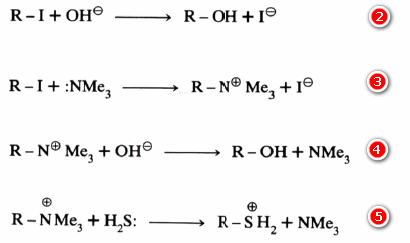
– يلاحظ في المعادلة السابقة أن العامل النيكليوفيلي قد يكون متعادل الشحنة أو يكون سالب الشحنة. كما أن المادة المتفاعلة تكون متعادلة أو موجبة الشحنة. وعليه يمكن تقسيم التفاعلات النيكليوفيلية إلى أربعة أنواع التالي: معادلة (2 حتى 5)
يتضح من المعادلات السابقة أن العامل النيكليوفيلي يجب أن يحمل زوج إلكتروني حر وعليه يمكن القول إن جميع العوامل النيكليوفيلية عبارة عن قواعد لويس (Lewis bases)
– يمكن للمذيب أن يلعب دور العامل النيكليوفيلي وفي هذه الحالة يسمى هذا التفاعل بالتحلل (Solvolysis).
أهم العوامل النيكليوفيلية Nucleophile
– وتجدر الإشارة هنا إلى أن أهم العوامل النيكليوفيلية التي ستقابلنا خلال دراسة تفاعلات الاستبدال النيكليوفيلية هي :
– إن أهم المركبات العضوية المشبعة التي تهاجم بواسطة العامل النيكليوفيلي هي: هاليدات الألكيل وهي أكثـرهـا انتشاراً في تفاعلات الاستبدال هذه، والكحولات ، ومركبات النيتروجين ومركبات الكبريت وغيرها.
أنواع تفاعلات الاستبدال النيكليوفيلية
– لقد استطاع انقولد وآخرون بعد دراسة مستفيضة على أمثلة مختلفة من تفاعلات الاستبدال الاستنتاج بأن هناك ميكانيكيتين لهذه التفـاعـلات يشترك في أولاهما المادة المتفاعلة في الخطوة البطيئة المحددة لسرعة التفاعل وهما:
(1) تفاعل استبدال نيكليوفيلي أحادي الجزيئية Substitution nucleophilic unimolecular ويتم اختصارها إلى (SN1)
(2) تفاعل استبدال نيكليوفيلي ثنائي الجزيئية Substitution nucleophilic Bimolecular ويتم اختصارها إلى (SN2). وفيها يشترك في الخطوة المحددة لسرعة التفاعل كل من المادة المتفاعلة والعامل النيكليوفيلي.
وفى بعض الأحيان وذلك حسب الدراسة الحركية قد تتم الميكانيكيتين معاً. أو قد يبدأ التفاعل بإحدى الميكانيكيتين وينتهي بالأخرى.
تفاعلات الاستبدال النيكليوفيلية أحادية الجزيئية SN1
– في تفاعلات SN1 لا تشترك في الخطوة المحددة لسرعة التفاعل سوى المادة المتفاعلة فقط.
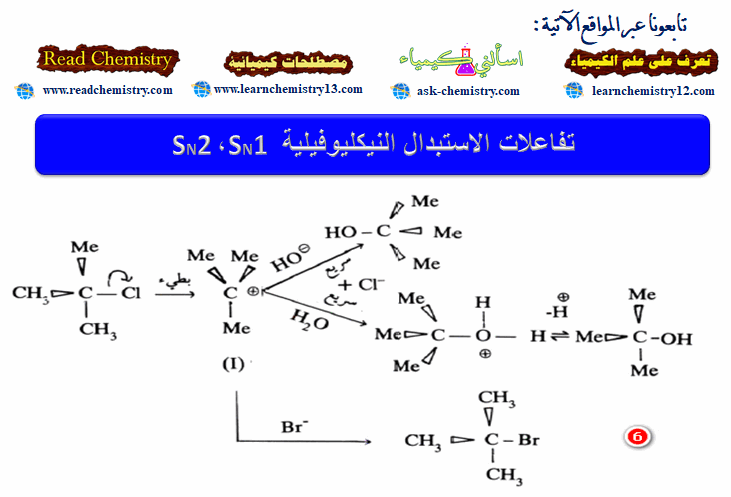
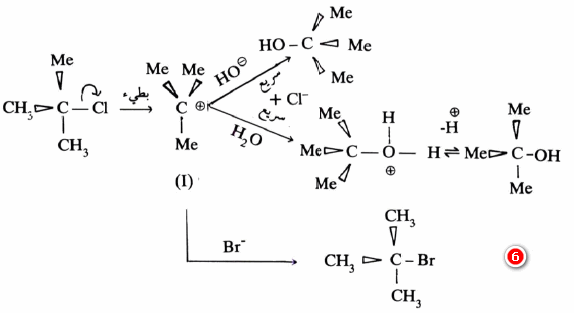
– مثال: التحلل المائي لمركب butylchloride في وجود قاعدة (معادلة 6)
– لقد وجد أن سرعة التفاعل لا تعتمد على تركيز أيون القاعدة –OH. ويمكن تفسير ذلك على أساس أن هاليد الألكيل يحصل له تأين بطيء. إذ تنفصل ذرة الهاليد المراد استبدالها انفصالاً أيونياً وينتج عن هذا التأين تكون أيون الكربونيوم Carbonium.
وبما أن مزيج التفاعل يحتوي على أيونين متعاكسي الشحنة ومتقاربين في بادئ الأمر. إلا أنها لا يلبثا أن يتباعدا بسبب وجود جزيئات المذيب التي تكون هالة تعمل على فصل الأيونين عن بعضها. كما هو في حالة تكون أيون الكربونيوم في المعادلة السابقة.
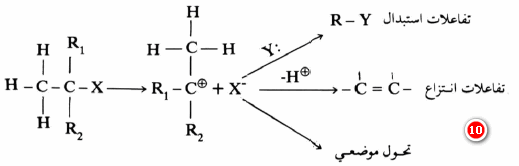
– يتضح أن عملية التهجين الأصلية على ذرة الكربون المركزية (sp3) قد تحولت إلى تهجين من نوع جديد (Planar-sp2 ) زواياه 120° وهو أكثر استقرارا.ً وذلك لأن مجاميع المثيل الثلاث تكون متباعدة أكثر ما يمكن عن بعضها البعض. وعليه فإن عملية مهاجمة العامل النيكليوفيلي (OH, H2O– ) يمكن أن يتم من الأمام أو الخلف. هذا مع الأخذ في الاعتبار أن التزاحم الفراغي للمجاميع والعوامل الأخرى تؤثر في تكـون أيون الكـربـونيوم. وفي حالة صعوبة تكون أيون الكربونيوم فإن ميكانيكية التفاعل قد تتغير من SN1 إلى SN2.
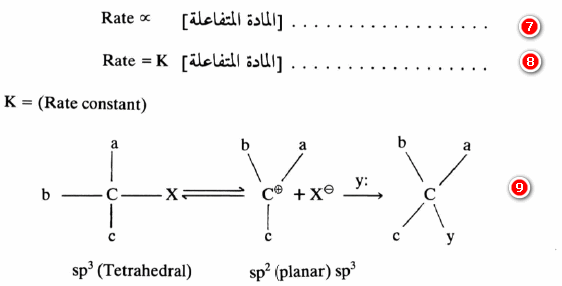
-ويمكن التعبير عن سرعة تفاعلات الاستبدال SN1 بالمعادلات التالية:
وهذا يعني أن تفاعلات الاستبدال SN1 تخضع في الحالة المثالية لقوانين السرعة الحركية من الدرجة الأولى كما هو واضح من معادلة (8).
تكون أيون الكربونيوم في تفاعلات الاستبدال النيكليوفيلية SN1
– يمكن إثبات تكون أيون الكربونيوم كحالة وسطية بإضافة أيون هالوجين مغاير لأيون الهالوجين الأصلي (المجموعة الخارجة).
– ففي التفاعل السابق (معادلة 6) أمكن الاستدلال على تكـون ناتجين أحدهما كحول والآخر هاليد الألكيل. وهذه النتيجة دليل قاطع على أن تكون أيون الكربونيوم يتم أولاً كحالة وسطية قبل مهاجمته بالعامل النيكليوفيلي.
– وقد وجد أن أيون الكربونيوم قليل الثبات وذلك لأن طاقته عالية كما أن هالة المذيب قد تعيق أحياناً مهاجمة العامل النيكليوفيلي له .
– وعندما يتكون أيون الكربونيوم كحالة وسطية فإن هذا يؤدي إلى خليط من النواتج حسب الكربونيوم المعادلة:
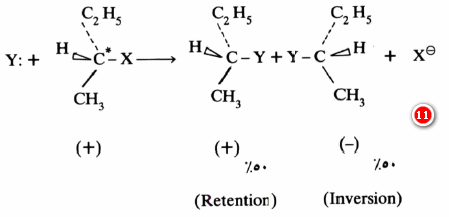
– عنـد دراسة التركيب الفراغي لنواتج تفاعلات SN1 والتي تكون فيها المادة المتفاعلة فعالة ضوئياً يتضح لنا أهمية تكون أيون الكربونيوم حيث يتم مهاجمته من جهتين متعاكستين وبنسبة واحدة تقريباً، وعليه عند البدء بمركب فعال ضوئيا (+) أو (-) فإن الناتج يكون خليطا من (+)، (-) ويكون غير فعال ضوئياً ويسمى خليط راسيمي Racemic mixture).
يدل هذا على أن 50% يـكـون هـجـوم العـامـل النيكليوفيلي من جهة المجمـوعـة التي تم استبدالها. ويقال إن المركب احتفظ بترتيبه الفراغي الأصلي (Retention) . كما وأن هناك هجوماً نيكليوفيلي من الجهة المعاكسة للمجمـوعـة المراد استبدالها بنسبة 50% ويقال إنه حصل انقلاب للشكل الفراغي الأصلي (Inversion) ويتضح ذلك من المثال التالي:
مميزات تفاعلات الاستبدال النيكليوفيلية أحادية الجزيئية SN1
(1) تخضع لقوانين السرعة الحركية من الدرجة الأولى.
يدل ذلك على أن وجود العامل النيكليوفيلي أو القاعدة في المحلول، بتراكيز مختلفة لا يؤثر على سرعة التفاعل. حيث إنه لا يشترك في الخطوة البطيئة المحددة لسرعة التفاعل.
(2) يتكون أيون الكربونيوم ببطء فيتحول التهجين من sp3 للمادة المتفاعلة إلى sp2 لأيون الكربونيوم.
(3) عند استخدام مادة فعالة ضوئياً فإن الناتج يكون خليطاً راسيمياً Racemic Mixture
(4) للوسط أثر كبير على تفاعلات SN1
(5) تخضع الرابطة بين المجموعة المراد استبدالها وذرة الكربون المركزية لعدة تغيرات في تفاعلات SN1 أهمها تحول الرابطة التساهمية إلى رابطة مستقطبة ثم تنفصل جزئياً (أيونات متقاربة) ثم يحيط بكل أيون هالة من المذيب مما يؤدي إلى تباعدها عن بعضها البعض.
(6) تتم مهاجمة العامل النيكليوفيلي لأيون الكربونيوم بعد تكونه مباشرة وبسرعة.
(7) تحدث تفاعلات جانبية مثل تفاعلات الانتزاع والتحول الموضعي Elimination and rearrangement reactions
تفاعلات الاستبدال النيكليوفيلية ثنائية الجزيئية SN2
في تفاعلات الاستبدال النيكليوفيلية أحادية الجزيئية SN1 نجد أن تركيز المادة المتفاعلة هو المحدد لدرجة التفاعل ومرفوع لأس واحد بمعنى أنه تفاعل من الدرجة الأولى.
– أما في حال تفاعلات الاستبدال النيكليوفيلي ثنائية الجزيئية SN2 فقد اتضح من خلال الدراسات الحركية لبعض التفاعلات العضوية بأنه تفاعل من الدرجة الثانية.
فعلى سبيل المثال تحلل مثيل البروم في وسط مائي قاعدي (معادلة 12) يتبع قانون التفاعل الموضح في معادلة (13):
حيث يتضح أن كلا من المادتين المتفاعلتين اشتركا في تحديد سرعة التفاعل وعليه يوصف مثل هذا النوع من التفاعلات بأنه تفاعل من الدرجة الثانية SN2 .
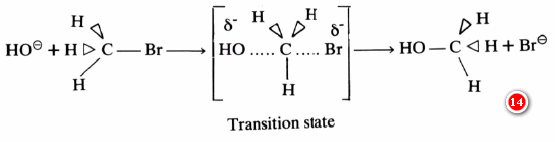
– وقد اقترح العالم Ingold أن الحالة الوسطية والتي يقوم العامل النيكليوفيلي فيها بمهاجمة المادة المتفاعلة تبدأ بارتباط العامل النيكليوفيلي جزئياً إلى ذرة الكربون المركزية التي تحمل المجموعة المغادرة (Br) ، وفي الوقت نفسه تظل ذرة البروم المغادرة متصلة جزئياً بذرة الكربون المركزية (ويوضح ذلك بنقط في حالة الروابط الجزئية) (Partial bonding)
وعليه فإن جزءا من الطاقة اللازمة لكسر الرابطة C….Br يتم الحصول عليه من الطاقة الناتجة عن تكون الرابطة الجزئية HO….C . وقد بينت الحسابات أن مهاجمة أيون الهيدروكسيل تكون على خط الوسط من الجهة المعاكسة للمجموعة المغادرة بحيث نحصل على أقل طاقة ممكنة للوضع الناشئ. ويمكن التعبير عن ذلك بالمعادلة التالية:
وتجدر الإشارة هنا إلى أنه في الحالة الانتقالية تكون مجموعة الهيدروكسيل وذرات الهيدروجين الثلاث وذرة الكربون المركزية والمجموعة المغادرة في مستوى واحد.
– وتكون المسافة بين الذرة المركزية وكل من المجموعة المغادرة والعامل النيكليوفيلي متساوية تقريباً.
– كما أن الشحنة السالبة تتوزع في الحالة الانتقالية بين مجموعة الهيدروكسيل والبروم. وتمتاز هذه الحالة بعدم الاستقرار وبطاقة تنشيط عالية. مما يؤدي انفصال المجموعة المغادرة (–Br ) نهائيا عن المادة المتفاعلة وفي الوقت نفسه ترتبط المجموعة –HO برابطة تساهمية ونحصل على الناتج المستقر.
مميزات تفاعلات الاستبدال النيكليوفيلي ثنائي الجزيئية SN2
ويمكن تلخيص أهم خصائص تفاعلات الاستبدال SN2 فيما يلي:
(1) يمكن تمثيل معدل سرعة التفاعل بالمعادلة التالية:
أي أن سرعة التفاعل في أبطأ خطوة له تتحدد بتركيز كل من المادة المتفاعلة والعامل النيكليوفيلي.
(2) لا يتكون أيون الكربونيوم كحالة وسطية، بل تنشأ حالة انتقالية على النمط نفسه في تهجين sp2. وتكون ذرة الكربون المركزية وذرات الهيدروجين الثلاث (أو المجاميع الألكيلية) في مستـوى واحـد وتكون مجموعتا –Br ، – HO مرتبطتين جزئياً وبعيدتين ما أمكن.
(3) يحدث في تفـاعـلات SN2 انقلاب للوضع الفراغي للجزيء.
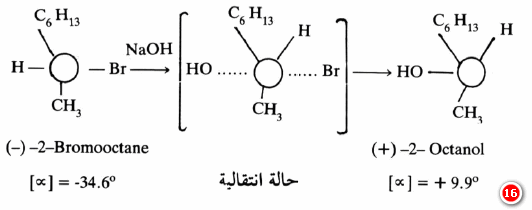
وذلك لأن العامل النيكليوفيلي يهاجم الجزيء من الجهة المعاكسة للمجموعة المغادرة وهذا يشبه المظلة عندما تنقلب بسبب الريح. ويبرهن ذلك عملياً باستخدام مادة فعالة ضوئيا تدير الضوء المستقطب إلى اليمين (+) مثلاً. فيكون الناتج ۱۰۰٪ مرکب فعال ضوئياً ويدير مستوى الضوء إلى اليسار (-) والعكس صحيح فيها لو استخدمت مادة فعالة تدير الـضـوء المـسـتـقـطب إلى اليسـار (-) ويسمى هذا بانقلاب فالـدن (Walden inversion) للشكل الفراغي ويتضح ذلك من المثال التالي :
(5) نظراً للوضع الفراغي الجديد (sp2) في الحالة الانتقالية ، فإن انتروبي التنشيط (Entropy of activation) في تفاعلات SN2 يأخذ قيمة سالبة. «وضع تزاحمي عالي» على خلافsp2 وتكون أيون الكربونيوم الموجب في تفاعلات SN1
المراجع: كتاب ميكانيكية التفاعلات العضوية ، تأليف/ د.سالم بن شويهان ، د. إبراهيم بن محمود النجار ، د. حمد بن عبدالله اللحيدان ، الرياض – جامعة الملك سعود – الطبعة الثانية 2003م