تكاثف بيركن Perkin Condensation فى المعمل
محتويات الموضوع
تجربة تكاثف بيركن Perkin Condensation في المعمل
– في هذه التجربة سيتم تحضير حمض السيناميك Preparation of Cinnamic acid كمثال على تفاعل تكاثف بيركن Perkin Condensation وسيتم مناقشة التجربة نظرياً وعملياً بالتفصيل.

أولاً/ الجزء النظري لتجربة تكاثف بيركن Perkin Condensation
– تكاثف الألدهيدات الأروماتية مع انهيدريدات الأحماض بوجود ملح القلوي للحمض الكربوكسيلي نفسه والذي يعمل كقاعدة، حيث يعطي الأحماض الكربوكسيلية غير المشبعة في الموقع ألفا وبيتا، ويعرف هذا التفاعل بتفاعل بيركن Perkin Condensation
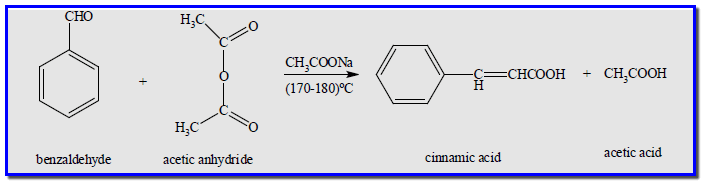
– حمض السيناميك يحضر بواسطة تفاعل بيركن، حيث يسخن البنزالديهيد مع أنهيدريد حمض الخليك بوجود خلات الصوديوم كما بالمعادلة الآتية:
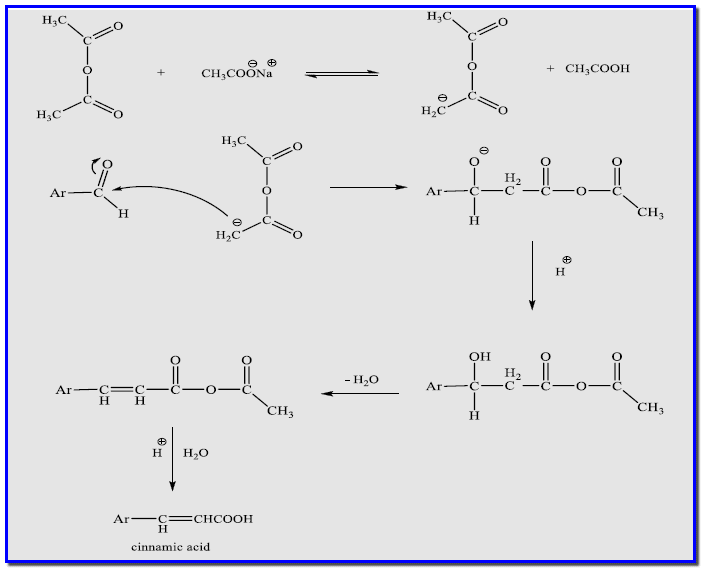
– يمكن تمثيل ميكانيكية التفاعل كما يلي:
ملاحظات هامة على تجربة تكاثف بيركن
(1) عند زيادة التسخين و وجود أثار البريدين تزداد نسبة الناتج كما في بعض الحالات عند استعمال ملح البوتاسيوم بدلاً من ملح الصوديوم للحمض الكربوكسيلي.
(2) من الممكن استعمال قلويات أخرى )الأمينات المختلفة مثل triethylamine (Et)3N أو الأملاح اللاعضوية مثل كربونات البوتاسيوم(
(3) إن ايزومراتCis ، Trans ممكن أن تتكون حول الآصرة المزدوجة في حمض السيناميك تفاعل بيركن يعطي فقط شكل الترانس trans المستقر درجة انصهاره 133Co أما شكل Cis درجة انصهاره 68Co فأنه يتكون ولكن غير مستقر وبسهولة يتحول إلى شكل trans
ثانياً/ الجزء العملي لتجربة تكاثف بيركن Perkin Condensation
الأدوات والمواد الكيميائية المطلوبة
الأجهزة والأدوات
– يتم توفير الأدوات الآتية كما يلي:
- دورق دائري
- مكثف هوائي
- حمام رملي
- جهاز تقطير
- جهاز ترشيح
المواد الكيميائية المطلوبة
– يتم توفير المواد الكيميائية الآتية كما يلي:
- بنزالدهيد
- انهيدريد الخليك
- خلات الصوديوم أو البوتاسيوم
- أنبوبة كلوريد الكالسيوم
- بيكربونات الكالسيوم بيكربونات الصوديوم
- حمض HCl المركز
- ماء بارد
خطوات التجربة
(1) ضع 1.5ml من البنزالديهيد و 2.5ml من انهيدريد الخليك مع 1g من خلات الصوديوم أو البوتاسيوم المصهورة حديثاً والمستخدمة جيداُ في دورق دائري مزود بمكثف هوائي يحمل أنبوبة كلوريد الكالسيوم ) أنبوبة واقية من الرطوبة(
(2) امزج محتويات الدورق جيداً وسخن مزيج التفاعل على حمام رملي عند درجة 160Co لمدة ساعة ثم عند (180-170)Co لمدة ثلاث ساعات.
(3) صب المزيج وهو ساخن (100-80) درجة مئوية في حوالي 20ml من الماء في دورق دائري لاستخدامه في التقطير البخاري.
(4) اغمر دورق التفاعل في كمية قليلة من الماء الساخن ثم أضف مع الرج الشديد محلولاً مشبعاً من بيكربونات الصوديوم حتى تتحول ورقة عباد الشمس من الأحمر إلى الأزرق.
(5) قطر المحلول بالبخار حتى يتقطر جميع بنزالدهيد غير المتفاعل وتحصل على متقطر رائق.
(6) برد المحلول المتبقي ورشح تحت الضغط المخلخل للتخلص من النواتج الثانوية الراتنجية ثم حمض الراشح بإضافة حمض HCl المركز ببطء مع الرج الشديد حتى ينقطع تحرر غاز ثاني أكسيد الكربون.
(7) عندما يبرد المحلول رشح حمض السيناميك بالترشيح تحت ضغط مخلخل، ثم اغسل بالماء البارد وجففه جيداً.
(8) أعد بلورته بواسطة ماء ساخن أو بواسطة مزيج من ثلاث حجوم من الماء وحجم واحد من الكحول.
تعليمات السلامة داخل المختبر الكيميائي
يجب عليك قبل بدء التجربة مراعاة التعلميات الآتية كما يلي:
(1) يجب مراعاة نظافة المختبر والأدوات المستخدمة به.
(2) يجب عدم إلقاء المواد الكيماوية بالأحواض إلا بعد تخفيفها. ولا يجوز نهائيا إلقاء قطع أو قشور الصوديوم في الأحواض.
(3) كما يجب أن تكون الأرضيات وكذلك أسطح الطاولات من مواد مقاومة للحريق والمواد الكيماوية وسهلة التنظيف.
(4) يجب غسل الأواني التي بها بقايا مواد سريعة الاشتعال بعد انتهاء العمل بها.
(5) يجب عدم تخزين الكيماويات أو عينات المواد المراد حفظها داخل المختبر إلا بأقل قدر ممكن ولحاجة العمل فقط.
(6) كما يجب عدم حفظ السوائل السريعة التبخر إلا في الثلاجات. ويجب الانتباه عند تغطية زجاجات الكيماويات.
(7) يجب وضع إناء مملوء بالرمل تحت القناني التي لا يوجد سبيل آخر لحمايتها. واعلم أن استخدام الرمال والتراب لامتصاص الأحماض المنسكبة على الأرض من الوسائل الآمنة من وجهة نظر السلام.
(8) عند تسخين مواد سريعة الاشتعال يجب استخدام حمام مائي.
(9) لا تحاول أن تدخل بقوة أنبوبة في سدادة فلين أو مطاط. بلل الزجاج بالماء أو الزيت أولاً لان ذلك يسهل ألي حد كبير هذه العملية.
أحتياطات أخرى
(10) يجب تداول المواد الخطرة حسب الأسس العلمية. وكمثال عند تخفيف حمض الكبريتيك فأن الحمض يضاف للماء ولا يضاف الماء إليه.
(11) يجب عدم استخدام المواد الخطرة كالفوسفور إلا تحت الإشراف الفعلي لمسئول المختبر. ومراعاة حفظ الفوسفور الأبيض والأصفر تحت سطح الماء لمنع اشتعالها تلقائياً حيث إنها تشتعل بمجرد تعرضها للهواء.
(12) كما يجب أن يكون بكل مختبر أكثر من مخرج. ويفضل أن تكون الأبواب من النوع المفصلي التي تفتح للداخل والخارج.
(13) يجب أن يتأكد محضر المختبر من فصل الكهرباء وإغلاق الغاز والماء عند انتهاء العمل بالمختبر يومياً ما لم يكن هناك أجهزة تلزمها الكهرباء باستمرار مثل الثلاجات أو أجهزة تكييف الهواء لظروف معينة.
(14) يجب على محضر المختبر إجراء التفتيش الدوري على توصيلات الغاز والمياه والمجاري والكهرباء للتأكد من سلامتها والإبلاغ عن أي خلل بها فور اكتشافه.
(15) كما يجب على محضر المختبر التأكد من توفير التهوية المناسبة والإضاءة المناسبة بالمختبر.
(16) يجب التأكد من أن غرفة الغازات (غرفة التجارب) محكمة الغلق لمنع تسرب الغازات الضارة منها أثناء إجراء التجارب الخطرة وأن تكون مزودة بمروحة سحب مناسب.
المراجع: تجارب فى الكيمياء العضوية. أسعد هاشم عنيد – حيدر مصطفي كمال – نهي سلمان صالح – أحمد حسون مجيد ، الطبعة لأولى (2015م) / جامعة الكوفة – كلية العلوم – العراق




ما سبب اظافة حامض HCL؟؟؟؟؟؟؟؟؟؟؟؟؟؟؟؟؟؟؟
ماسبب تجفيف الاجهزه قبل البدء بتجربه بيركن