الكيمياء العضوية
تحضير الأحماض الكربوكسيلية Preparation of Carboxylic acids
فيما يلى سنسرد جميع طرق تحضير الأحماض الكربوكسيلية Carboxylic acids مع تحضير أهم تلك الاحماض الشائع استخدامها وهي :
(1) أكسدة الكحولات الأولية Oxidation of primary alcohols
(2) أكسدة ألكيل بنزين Oxidation of alkyl benzene
(3) أكسدة الألكينات Oxidation of Alkenes
(4) من أملاح الأحماض Acids salts
(5) تميؤ الأسترات Hydrolysis of esters
(6) التحلل المائي لكلوريدات الأحماض Hydrolysis of Acid Chlorides
(7) أكسدة كلوريدات الأحماض Oxidation of Acid Chlorides
(8) كربنة متفاعلات جرينارد Carbonation of Grignard reagent
(9) إماهة النيتريلات Hydrolysis of Nitriles
(10) أكسدة الكيتونات Oxidation of Ketones
(11) تميؤ الزيوت والدهون
(12) تحضير أهم الأحماض الكربوكسيلية الهامة
(1) أكسدة الكحولات الأولية Oxidation of primary alcohols
تتأكسد الكحولات الأولية على خطوتين حيث تعطي ألدهيدات أولاً ثم تتأكسد إلى أحماض كربوكسيلية Carboxylic acids.
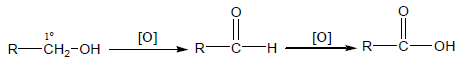
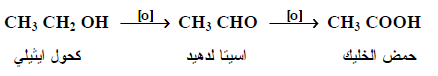
(2) أكسدة ألكيل بنزين Oxidation of alkyl benzene
يمكن أن تؤكسد مجموعة الألكيل في البنزين إلى مجموعة كربوكسيل باستخدام برمنجانات البوتاسيوم في وسط قاعدي.


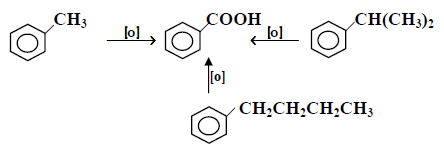
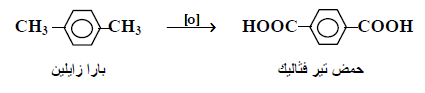
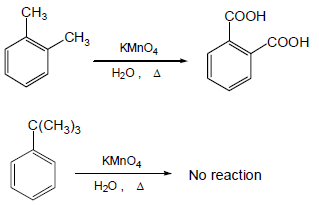
في المعادلة الأخيرة لم يحدث تفاعل لأن عملية الأكسدة تتم في ذرة الكربون المرتبطة بالحلقة مباشرة Benzylic carbon شرط وجود ذرة هيدروجين بنزيلية وهذا غير متوفر في مجموعة t-Butyle
(3) أكسدة الألكينات AlkenesOxidation of
– الألكينات ثنائية أو ثلاثية التفرع يمكن أن تتأكسد باستخدام كرومات البوتاسيوم أو الأوزون ، لتعطي أحماض كربوكسيلية Carboxylic acids.
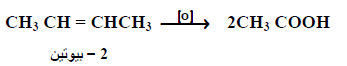
– بينما يعطي في حالة 2- ميثيل2- بنتين عند الأكسدة أسيتون وحمض بروبانويك.
– بينما أكسدة سايكلوهكسين تنتج عن كسر الرابطة المزدوجة لتعطي ناتج واحد فقط وهو حمض اديبيك.
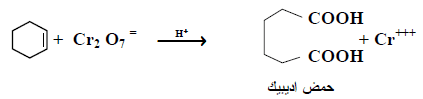
(4) من أملاح الأحماض Acids salts
يمكن تحضير الأحماض الكربوكسيلية البسيطة بإضافة حمض الكبريتيك إلى الملح لحمض ، ثم يقطر المخلوط ، وتحضر الأحماض الكبيرة بإضافة حمض الكبريتيك إلى محلول مائي للملح ثم يستخلص الحمض بمذيب عضوي مثل ايثيل ايثر أو مذيب آخر.
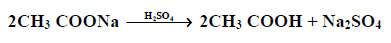
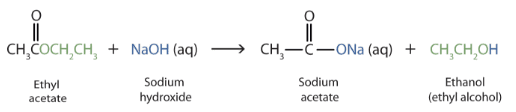
(5) تميؤ الأسترات estersHydrolysis of
عند غليان استر معين في محلول مائي لهيدروكسيد الصوديوم يتكون ملح صوديومي لحمض ونجد أنه عند معالجته بحمض HCl مخفف يعطي الحمض الكربوكسيلي.
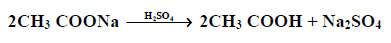
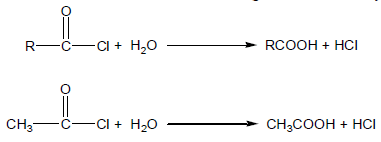
(6) التحلل المائي لكلوريدات الأحماض Hydrolysis of Acid Chlorides
تتحلل كلوريدات الأحماض مائياً وتنتج أحماض كربوكسيلية Carboxylic acids.
(7) أكسدة كلوريدات الأحماض Oxidation of Acid Chlorides
تتأكسد كلوريدات الأحماض لتعطي أحماض كربوكسيلية.
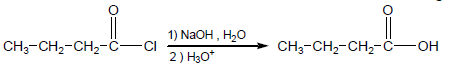
(8) كربنة متفاعلات جرينارد Carbonation of Grignard reagent
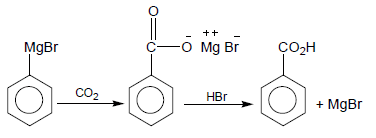
(9) إماهة النيتريلات Hydrolysis of Nitriles
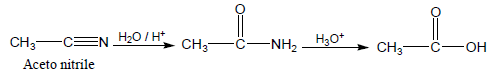
(10) أكسدة الكيتونات Oxidation of Ketones
– إن أكسدة الكيتونات البسيطة تعتبر عملية صعبة حيث يتأكسد الأسيتون ببطء شديد عن تفاعله مع KMnO4 أو بوجود H2CrO4على الساخن ولكن بالنسبة للسلاسل الطويلة غير المتماثلة تكون عملية الأكسدة قوية وجيدة وتعطي خليط من الأحماض الكربوكسيلية كما يلي:
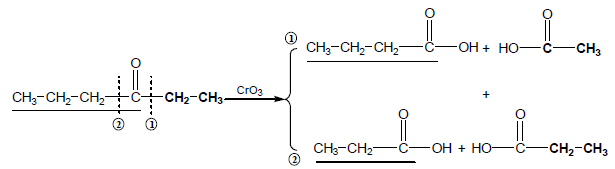
– أما الكيتونات الأروماتية من نوع alkyl aryl ketone والتي تحتوي على α-hydrogen تتأكسد بحيث تنشطر الرابطة بين مجموعة الألكيل والكربونيل وتنتج أحماض كربوكسيلية.
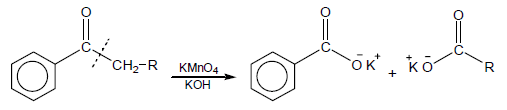
– كما يمكن الحصول على الأحماض الكربوكسيلية من إماهة ناتج تفاعل الكيتونات مع Hypochlorites ويستخدم هذا التفاعل فى الحصول على الكلوروفورم.
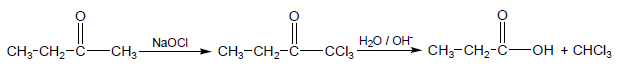
(11) تميؤ الزيوت والدهون
يمكن تميؤ الزيوت والدهون بواسطة هيدروكسيد الصوديوم لتعطي أحماض كربوكسيلية ذات سلاسل طويلة .
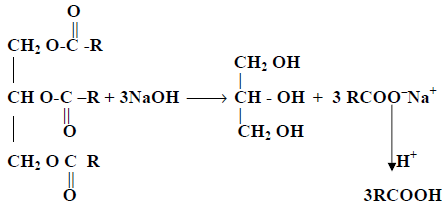
(12) تحضير أهم الأحماض الكربوكسيلية الهامة
(1) تحضير حمض الفورميك Methanoic acid
الطريقة القديمة: تقطير النمل الأحمر بعد معالجته ببخار الماء .
الطريقة الحديثة: يحضر في المعمل بتقطير حمض الأكساليك مع الجلسرين
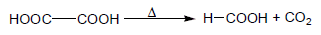
ويحضر في الصناعة عن طريق تفاعل هيدروآسيد الصوديوم مع غاز أول أآسيد الكربون ومعالجة الملح الناتج بحمض الكبريتيك أو عن طريق الإماهة المحفزة Catalytic hydration لغاز أول أكسيد الكربون ويستخدم حمض الفورميك في حفظ اللحوم وحماية الجلود من التفسخ.
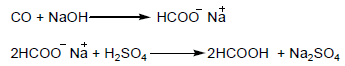
(2) تحضير حمض الخليك Ethanoic acid
الطرق القديمة: وكانت تتم بطريقتين:
(أ) التقطير الإتلافي للخشب .
(ب) الأكسدة الجرثومية للسوائل الكحولية : تخمر السوائل الكحولية في وفرة من الهواء وبفعل الخميرة الهوائية يتأكسد الإيثانول إلى حمض الخليك .
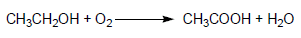
الطريقة الحديثة: عن طريق إماهة الأستلين إلى أسيتالدهيد ثم أكسدتها إلى حمض الخليك ويستعمل كمذيب عضوي للمواد المراد أكسدتها لأنه لا يتأثر بالعوامل المؤكسدة ويستخدم في صناعة مبيد الأعشاب Herbicide 2,4-D
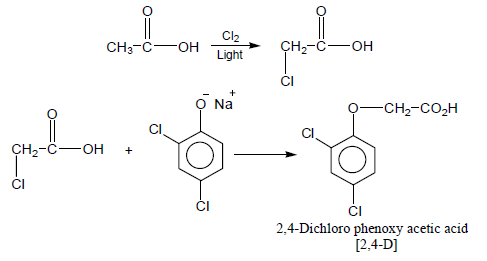
ملاحظة: يطلق على حمض الخليك ذو التركيز 100% اسم حمض الخليك الثلجي لأنه يتجمد عند درجات الحرارة المنخفضة على شكل بلورات عديمة اللون تشبه الثلج.
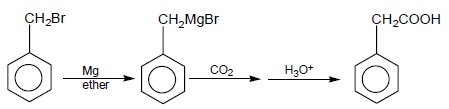
تمرين: كيف تحصل على Phenyl acetic acid من Benzyl bromide؟
المراجع :
– أسس الكيمياء العضوية . وائل غالب محمد – وليد محمد السعيطي ، الطبعة الأولى (2008) / دار الكتب الوطنية – بنغازي – لبيبا
– أساسيات الكيمياء العضوية. محمد مجدي واصل ، جامعة الأزهر – جمهورية مصر العربية


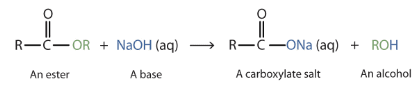



موقع جيد جداً ومفيد حقيقة استفدنا منه كثيراً في أبحاث مادة الكيمياء شكراً جزيلاً لأصحاب المحتوي