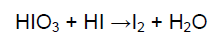الخواص الكيميائية للألكانات Chemical properties of Alkanes
الخواص الكيميائية للألكانات Chemical properties of Alkanes
– فى هذا الموضوع سيتم مناقشة الخواص الكيميائية للألكانات Chemical properties of Alkanes (تفاعلات الألكانات) وهي كما يلي:
- تفاعل الاحتراق Combustion reaction
- تفاعل التكسير Cracking reaction
- تفاعل الهلجنة Halogenation reaction
- هلجنة الألكانات العليا Halogenation of higher Alkanes
- الفريونات Freons
- تفاعلات الألكانات الحلقية Reactions of cycloalkanes
الألكانات مركبات خاملة كيميائياً نظراً للأسباب الآتية كما يلي:
(1) قوة الروابط C-C ، C-H التى لا تنكسر إلا عند درجات الحرارة العالية.
(2) ونظراً لتقارب ذرتي الكربون والهيدروجين فى قيم الكهروسالبية يجعل روابط C-H ذات قطبية منخفضة جداً وبناءاً عليه لا تتأثر الألكانات بالقواعد.
(3) ولعدم وجود إلكترونات حرة فى جزيئاتها فهي لا تتأثر بالأحماض المعدنية المركزة فى الظروف العادية.
(4) لا تتأثر بالعوامل المؤكسدة لذلك تستخدم الألكانات كمذيبات فى تفاعلات المجموعات الوظيفية الأخرى.
(5) تمتاز معظم تفاعلات الألكانات بهجوم متفاعل يحتوي على إلكترونات غير رابطة مثل الأكسجين والكلور على الألكان.

هو تفاعل الألكانات مع الأكسجين ويعتبر من أهم تفاعلاتها نظراً لأستخدمها كوقود حيث أن جميع الألكانات قابلة للاشتعال.
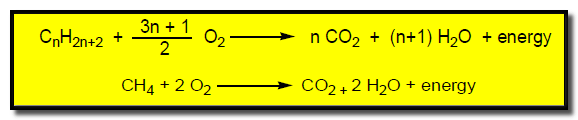
(a) الاحتراق الكامل:
يتم في وفرة من الأكسجين ويعطي غاز ثاني أكسيد الكربون وبخار ماء وتنطلق طاقة تسمي طاقة الاحتراق.
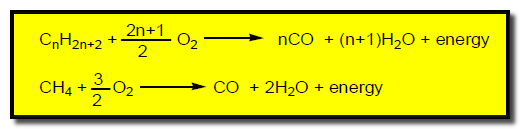
(b) الاحتراق الغير الكامل:
يتم في نقص الأكسجين ويعطي أول ثاني أكسيد الكربون وبخار ماء وطاقة كما بالتفاعل التالي:
ملاحظات هامة:
– إذا كان النقص كبيراً في الأكسجين يتم الحصول على الكربون فى صورة سناج (أسود الكربون Carbon black) وهو نقي ويستخدم في صناعة الحبر والطلاء.
– يفضل الحصول على الطاقة من الأحتراق الكامل للألكان لأن كمية الطاقة المنبعثة من الاحتراق غير الكامل تكون أقل بكثير من تلك المنبعثة من الأحتراق الكامل بالإضافة لانبعاث غاز CO
(2) الخواص الكيميائية للألكانات: تفاعل التكسير Cracking reaction
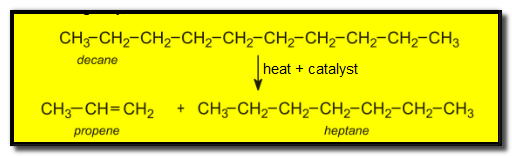
– هو عملية التكسير الحراري للألكانات التي تحتوي على 12 ذرة كربون أو أكثر في وجود عامل حفاز عند درجات حرارة عالية حيث تتكسر هذه السلسلة الكبيرة إلى ألكانات صغيرة وإلكينات وأحياناً غاز الهيدروجين.
– ولا تستخدم الألكينات الناتجة من هذه العملية كوقود وإنما ترسل كمواد خام لتصنيع البلاستيك.
(3) الخواص الكيميائية للألكانات: تفاعل الهلجنة Halogenation reaction
– هو عبارة عن استبدال ذرات الهيدروجين في الألكان بذرات هالوجين.
– وتختلف سرعة التفاعل من هالوجين لأخر حيث يتفاعل الفلور بشدة محدثاً انفجار بسبب شدة نشاطه لذلك يخلط الألكان والفلور بغاز خامل مثل الهيليوم ليقلل من شدة التفاعل.
– كما يجب أن يتم التفاعل في وعاء خاص مبطن بحبيبات النحاس التى تعمل على امتصاص الحرارة الناتجة من التفاعل.
– يتفاعل كل من الكلور والبروم مع الألكان فى درجة حرارة الغرفة تفاعل متسلسل Chain reaction في وجود الأشعة البنفسجية Ultraviolet UV ويعطي خليط من النواتج حيث يتكون فى كل خطوة منتج يعمل كمتفاعل فى الخطوة التى تليها.
– ويمتاز هذا التفاعل بالاستبدال المتكرر لأن جميع ذرات الهيدروجين في الألكان قادرة على التفاعل.
– لا يتفاعل اليود تحت الظروف العادية لذا يستخدم عامل مؤكسد مثل حمض الأيوديك Iodic acid HIO3 الذي يعمل علي تحويل يوديد الهيدروجين المتكون إلى يود وبالتالي يدفع التفاعل في إتجاة تكوين يوديد المثيل.
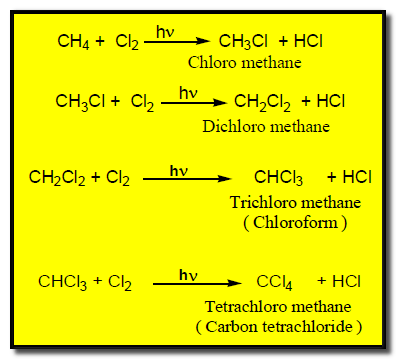
مثال: كلورة الميثان Chlorination of methane كما بالتفاعلات الأتية كما يلي:
ملاحظة : يمكن التحكم في النواتج عن طريق التحكم في نسب المتفاعلات فعند استخدام زيادة من الميثان يتم الحصول على نسبة عالية من كلوروميثان وعند استخدام زيادة من الكلور يتم الحصول علي رباعي كلوروميثان بنسبة عالية.
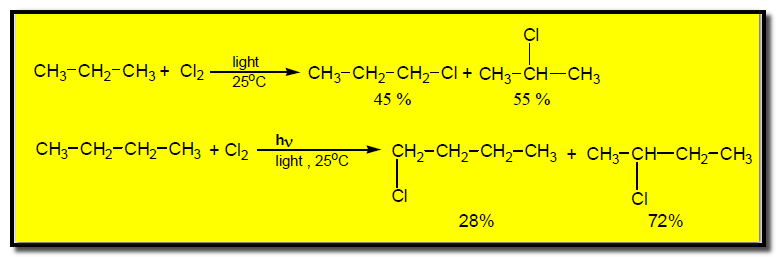
(4) هلجنة الألكانات العليا Halogenation of higher Alkanes
– أن الهلجنة الأحادية للألكانات العليا تؤدي إلى تكوين خليط من النواتج يتوقف عددها على عدد أنواع الهيدروجين بها.
– عند كلورة ألكان يحتوي على خليط من هيدروجين أولي وثانوي تكون جميع ذرات الهيدروجين فى كل نوع متكافئة فأن الكلورة تتبع ثبات الجذر الحر free radical.
– عند الكلورة الأحادية للألكانات التى تحتوي على خليط من أنواع مختلفة من الهيدروجين تتكون نواتج لا تتبع ثبات الجذر الحر.
– وتفسير ذلك هو أن الكلور يتميز تفاعله بالسرعة والشدة حيث يتفاعل على أساس طاقات تفكك الروابط .
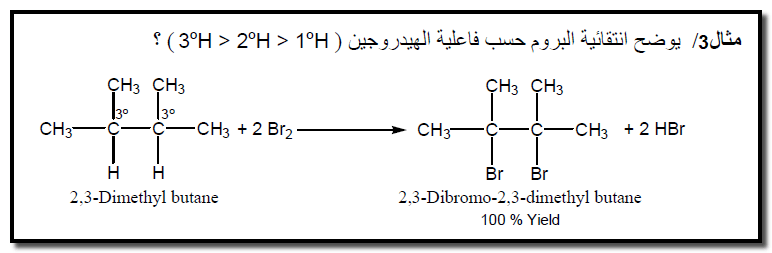
– ونظراً لأن الفارق فى مقدار هذه الطاقات ليس كبيرا جداً فأن الكلور لا يستطيع التمييز بين أنواع الهيدروجين الثلاثة لذا يكون غير انتقائي Non-selective على العكس من البروم الذي يكون تفاعله ابطأ وأكثر انتقائية Selectivity من حيث التمييز بين أنواع الهيدروجين على الرغم من انه أقل فاعلية من الكلور.
– قيم الفاعلية النسبية عند الكلورة:


(5) الفريونات Freons
– عبارة عن غازات أو سوائل ذات درجات غليان منخفضة تعرف بمركبات Chloro fluoro carbons CFC
– ولها استعمالات واسعة فى الصناعة حيث تستخدم كمواد دافعة في علب الرش وتستعمل فى المبردات والمجمدات ومكيفات الهواء.
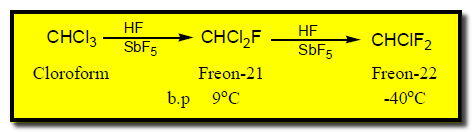
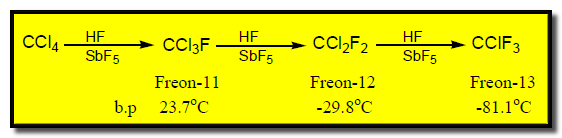
– كل مركبات CFC غير سريعة الاشتعال ولها بعض الكفاءة في إطفاء الحرائق ولكن المركبات الأكثر أستعمالاً لهذا الغرض هى التي تحتوي على البروم مثل CBrF3 ، CBrClF2 .
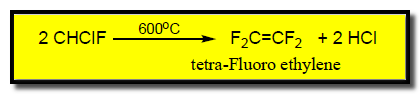
– يستخدم فريون 22 فى تحضير فلورو إيثلين المستخدم فى تحضير التفلون كما بالتفاعل التالي:
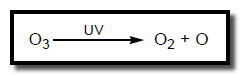
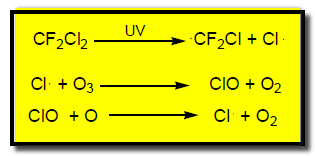
– تعمل أشعة UV على تكوين ذرات الكلور بالجذور الحرة من الفريونات فتتخذ ذرات الكلور مع الأوزون لينتج كلور أحادي الأكسيد وجزئ أكسجين مما يؤدى على تناقص طبقة الأوزون.
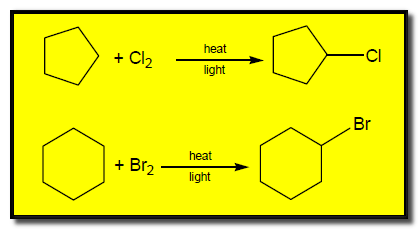
(6) تفاعلات الألكانات الحلقية Reactions of cycloalkanes
(a) الهلجنة Halogenation
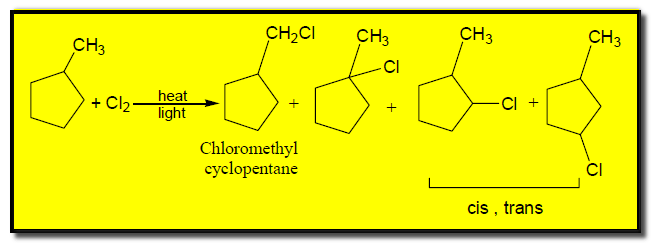
– عند هلجنة ألكان حلقي مستبدل ينتج خليط من النواتج كما يلي:
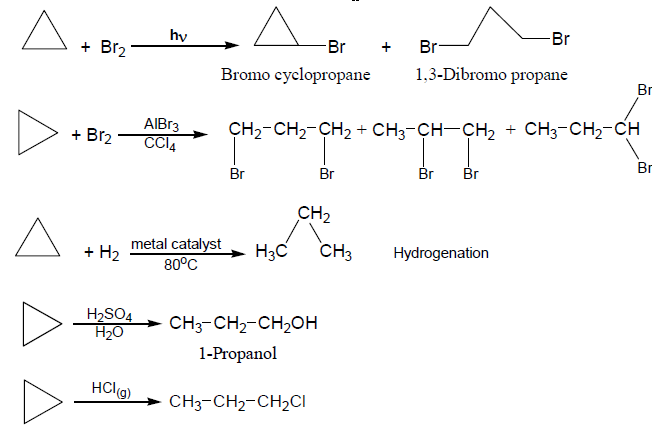
(b) تفاعلات فتح الحلقة Ring-opening
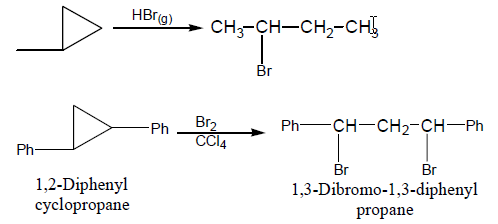
يتم فتح الحلقة بالانشطار غير المتجانس لرابطة سيجما حيث تفتح حلقة البروبان بسهولة الإجهاد العالي فى الحلقة الذي يضعف الرابطة C-C كما بالتفاعل التالي:
المراجع : الخواص الكيميائية للألكانات – الفصل الثاني ” الهيدروكربونات ” من كتاب أسس الكيمياء العضوية. Foundations of Organic Chemistry” للمؤلفين وائل غالب محمد – وليد محمد السعيطي”