النيكل Nickel – الخواص الكيميائية والفيزيائية لعنصر النيكل
ما هو عنصر النيكل Nickel؟
– النيكل Nickel عنصر من عناصر الجدول الدوري: العدد الذري = 28 ، العدد الكتلي = 59
– يرمز لعنصر النيكل له بالرمز: 59Ni28
– التوزيع الإلكتروني له: Ar]18 4s2 3d8]
– النيكـل معدن قاس أبيض اللون مائل إلى الفضي.
– ينتمي إلى الفلزات الانتقالية.
– وهو معدن قابل للطرق والسحب.
– ويعتبر عنصراً نشط كيميائياً بشكله الحر فيتفاعل مع أكسجين الهواء ببطء في درجات الحرارة والضغط العادية مشكلاً طبقة عازلة من الأكاسيد، ولهذا السبب يستعمل النيكـل غالباً في عمليات الطلي المعدني وفي صناعة الأجهزة المخبرية.
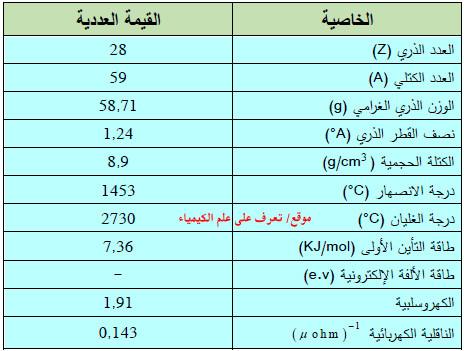
– الجدول التالي يوضح الخواص العامة لعنصر النيكـل كما يلي:
اكتشافه ووجوده في الطبيعة Discovery of Nickel
– عزل من قبل العالم السويدي (أكسيل كلونستد) سنة 1750م الذي أفلح في استخلاص فلز النيكل ولكن بصورة غير عالية النقاوة من خام الجرسدورفايت.
– اشتق اسمه من اللغة السويدية وكلمة Kopparrnickel بمعنى نحاس غير حقيقي.
– يعتبر معدن النيكل العنصر الثاني والعشرين من حيث الوفرة في القشرة الأرضية.
– كما يعد المعدن السابع بالنسبة لوفرة العناصر الانتقالية.
– ويوجد معدن النيكـل في خام جارنيرايت وخام نيكل – فيراس – ليمونايت الموجودة في كوبا وكذلك خام بنتلاندايت الذي يحتوي فقط على 15% من Ni ويوجد هذا الخام في كندا وروسيا وجنوب أفريقيا.
تحضير عنصر النيكل Preparation of Nickel
– يتم الحصول على معدن النيكل من خام الكبريتيد الذي يتم تركيزه في البداية بعملية الطفو، ثم الفصل المغناطيسي وينتج عن ذلك ما يسمى (الخام المركز) الذي يضاف إليه السليكا.
– ثم يتعرض لعملية التحميص والانصهار بغرض خفض التركيز حيث يتحول كبريتيد الحديد إلى أكسيد حديد ثم إلى سليكات حديد يتم التخلص منها على هيئة خبث، ثم يترك الخام ليبرد لعدة أيام حتى يتصلب هذا الخام.
– وبعد ذلك يتم تسخينه مع NaHSO4 وفحم الكوك فينتج مصهور الملح Na2S والذي يذيب كبريتيد النحاس في الطبقة العليا بينما يظل مصهور كبريتيد النيكـل طبقة سفلى سوداء اللون.
– وبعد تبريد الطبقتين يمكن فصل الطبقة السفلى وتحويل كبريتيد النيكل بالتحميص إلى أكسيد النيكـل.
– وتستخدم طريقة التحليل الكهربائي في الحصول على النيكـل حيث يوضع أنود النيكل غير النقي في مواجهة كاثود من النيكل النقي، ويوضع بين القطبين محلول مائي والكتروليت من NiCl2 وNiSO4 ويحدث أثناء التحليل الكهربائي ذوبان للنيكـل من الأنود ثم ترسبه على الكاثود بنسبة نقاء تصل إلى 99.9%
الخواص الكيميائية لعنصر النيكل Chemical properties of Nickel
(1) التفاعل مع الأكسجين
– يتفاعل النيكل مع أكسجين الهواء ببطء عند درجة الحرارة والضغط الماديين، مشكلاً طبقة عازلة من الأكاسيد وفق التفاعل الآتي كما يلي:
2Ni + O2 → 2NiO
(2) التفاعل مع الهالوجينات
يتفاعل النيكـل مع الهالوجينات حسب التفاعل الآتي كما يلي:
Ni + X2 → 2NiX2
(3) التفاعل مع الماء
– يتفاعل النيكـل مع الماء ليشكل أكسيد النيكـل وانطلاق غاز الهدروجين حسب التفاعل الآتي كما يلي:
Ni + H2O → NiO + H2
(4) التفاعل مع الأحماض
– يتفاعل النيكـل مع الأحماض المعدنية مثل HCl وانطلاق غاز الهيدروجين حسب التفاعل الآتي كما يلي:
Ni + 2HCl → NiCl2 + H2
(5) التفاعل مع الكبريت والكربون
– يتفاعل النيكـل مع كل من الكبريت والكربون حسب التفاعلين التاليين كما يلي:
Ni + S → NiS
3Ni + C → Ni3C
(6) التفاعل مع السيليكون
– يتفاعل النيكـل مع السليكون حسب التفاعل الآتي كما يلي:
2Ni + Si → Ni2Si
(7) التفاعل مع النشادر
– يتفاعل النيكـل مع النشادر وينشأ عن ذلك انطلاقاً غاز الهيدروجين حسب التفاعل الآتي كما يلي:
4Ni + 2NH3 → Ni4N2 + 3H2
استخدامات النيكل Uses of Nickel
– يبلغ الإنتاج العالمي من معدن النيكل حوالي 750 ألف طن سنوياً، يستخدم بعضها في إنتاج السبائك المعدنية، وصناعة الصلب النيكـلي الذي كان يستخدم في طلاء الدروع لقوة صلابته.
– أما الفولاذ الصامد فهو يحتوي على نسبة تصل إلى %8 من النيكـل، ويستخدم في صناعة المغناطيس الدائم.
– ومن السبائك المشهورة أيضاً فضة النيكـل أو الفضة الألمانية، وتغطى هذه السبيكة بطبقة من الفضة بالطلاء الكهربي وتستخدم في صناعة أدوات المائدة مثل الملاعق وغيرها.
تأثير النيكل على جسم الإنسان
– يعد النيكل خطر على الصحة فقط في حالة دخوله إلى الجسم، فهو يصنف من المواد المسبية للسرطان عند الإنسان.
– التعرض المزمن للنيكـل هو أحد عوامل الخطر للإصابة بسرطان الرئة.
– كما يعد من أكثر المعادن المسببة للحساسية ويمثل %12 من السكان مصابون بالحساسية نتيجة استخدامهم المفرط للنيكـل.
– بالإضافة إلى ذلك فأن الإشعاعية المحتملة للنيكـل فقد تبين أن النيكل يسبب نقصاً في وزن الأعضاء ووزن الجسم.
المراجع:
- دراسة كيميائية تحليلية مفصلة لعناصر الجدول الدوري / الأستاذ الدكتور حسن بوزيّان أستاذ بقسم الكيمياء بالمدرسة العليا للأساتذة / الجزء الأول / أبريل 2017 / الجزائر.
- العناصر الانتقالية – كتاب الصف الثالث الثانوي – جمهورية مصر العربية 2021