الكيمياء الفيزيائية
الكيمياء الفيزيائية تدمج بين الكيمياء والفيزياء، تدرس سلوك المواد على المستوى الجزيئي والذري. تركز على الطاقة، الديناميكا الحرارية، الحركية الكيميائية، وتفسير الظواهر الكيميائية نظريًا وتجريبيًا.
-
اختبار على الطاقة والتغيرات الكيميائية
اختبار على الطاقة والتغيرات الكيميائية في هذا الموضوع نقدم لك أختبار على الطاقة والتغيرات الكيميائية. وهو أختبار بسيط لقياس…
أكمل القراءة » -
تحميل كتاب أسس الكيمياء التناسقية pdf
استكمالاً لقائمة الكتب الكيميائية الرائعة والمختلفة الذي يقوم موقعنا بشرحها للأعضاء الكرام. نقدم لكم في هذا الموضوع مرجع غاية في…
أكمل القراءة » -
التسامي في المواد الصلبة Sublimation of Solids
التسامي Sublimation – عملية التسامي هو تحول المادة مباشرة من الحالة الصلبة إلى الحالة الغازية دون المرور بالحالة السائلة. –…
أكمل القراءة » -
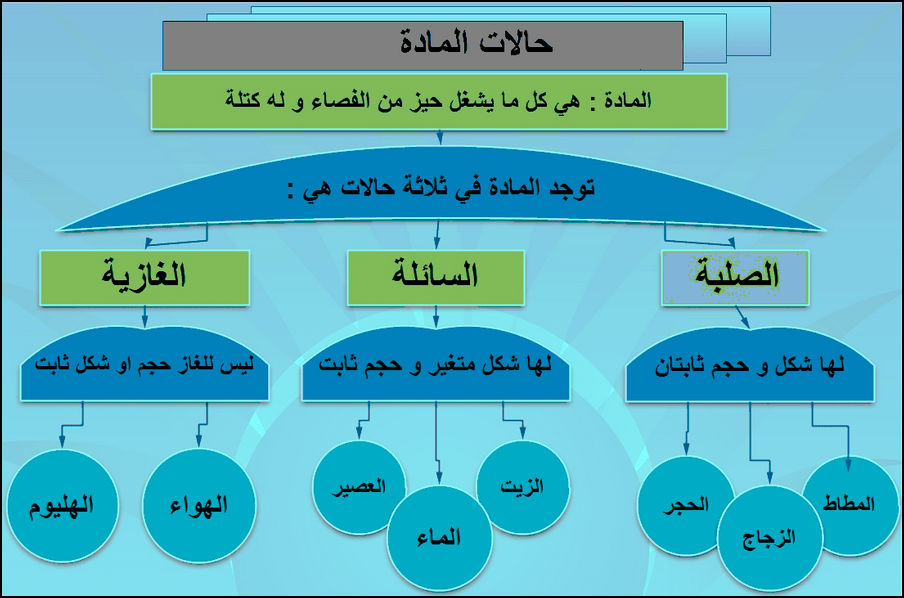
خواص السوائل وخواص المواد الصلبة liquids and solids properties
(1) الحالة السائلة The Liquid State –الحالة السائلة ھي الحالة الوسط بین الحالتین : الصلبة والغازیة حیث یمكن الحصول علیھا…
أكمل القراءة » -
اللزوجة Viscosity – موضوع شامل ومفصل
تعريف اللزوجة Viscosity – اللزوجة: ھي مقاومة السائل للإنسیاب (مقیاس لسرعة سریان السائل بتأثیر قوى معینة) حیث تبدي جمیع السوائل…
أكمل القراءة » -
ما هو الباراكور Parachor
فى هذا الموضوع سوف نستعرض ما هو المقصود بمصطلح الباراكور وأهم تطبيقاته علاوة على ذلك مسائل محلولة توضيحية. الباراكور Parachor…
أكمل القراءة » -
طرق قياس التوتر السطحي Measurement of Surface Tension
– توجد طرق متعدد لقياس التوتر السطحي لسائل ومنها: (1) طریقة ارتفاع السائل في الأنبوبة الشعریة Capillary Rise Method …
أكمل القراءة » -
التوتر السطحي – ظاهرة البلل – الخاصية الشعرية
في هذا الموضوع سوف نستعرض العلاقة بين التوتر السطحي وظاهرة البلل والخاصية الشعرية ثم نتناول بعض المسائل المحلولة على القوانين…
أكمل القراءة » -
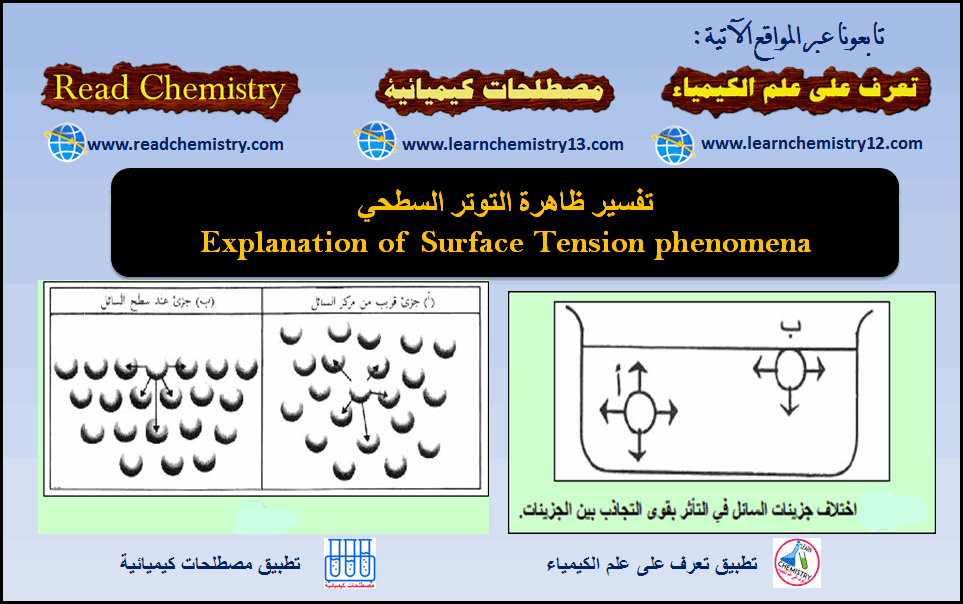
تفسير ظاهرة التوتر السطحي Surface Tension
– عند وضع إبرة معدنیة في إناء به كمیة من الماء، نلاحظ أنھا لا تطفو فوق سطح الماء ولكنھا…
أكمل القراءة » -
معادلة كلاوزيويس – كلابيرون Calusius – Clapeyron Equation
أولاً: معادلة كلاوزيويس – كلابيرون Calusius – Clapeyron Equation – العلاقة بین الضغط البخاري ودرجة الحرارة لكل من الماء والكحول…
أكمل القراءة »