تسمية المركبات الحلقية الغير متجانسة Heterocyclic Compounds
تصنيف المركبات العضوية الحلقية
– تقسم المركبات العضوية الحلقية عادة إلى:
(1) مركبات حلقية متجانسة Homocyclic compounds
– هي المركبات العضوية الحلقية التي تكون جميع الذرات المكونة للحلقة ذات نوع واحد.
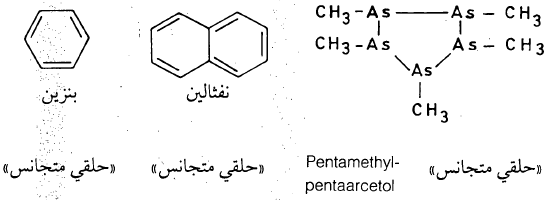
– قد تكون هذه المركبات أليفاتية مثل: السيكلوهكسان (Cyclohexane) والسيكلوبنتان (Cyclopentane). وقد تكون أروماتية مثل البنزين والنفثالين ومشتقاتها.
– ويلاحظ أنه في نواة البنزين تكون جميع الذرات ذات نوع واحد. ومثل هذا التركيب الجزيئي يطلق عليه حلقي متجانس (Homocyclic). والقليل من العناصر غير الكربون قادر على تكوين حلقات متجانسة.
– ومن أمثلة المركبات الحلقية المتجانسة التي لا تحتوي على عنصر الكربون خماسي مثيل – خماسي ارستيول.
(2) مركبـات حلقية غير متجـانسـة Heterocyclic Compounds
– هي عبارة عن مركبات حلقية تحتوي فيها الحلقة على ذرة واحدة على الأقل من عنصر آخر غير عنصر الكربون.
– وأكثر هذه العناصر شيوعا الأكسجين، الكبريت والنتروجين وبصورة أقل انتشارا تدخل عناصر الزئبق، الفسفور، الزرنيخ، الرصاص، وغيرها من العناصر الأخرى.
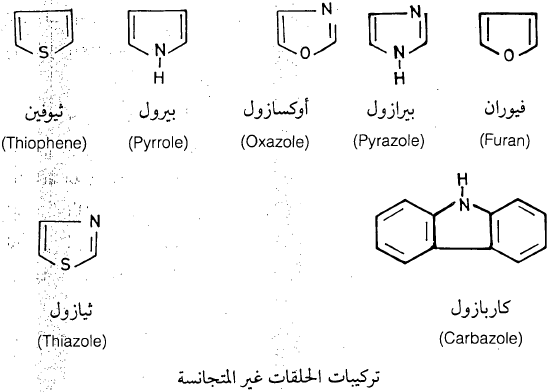
– قد تكـون المركبات أليفـاتية مثـل: التتراهيدروفوران ( Tetrahydrofuran) وقـد تكـون أروماتية مثل الفيوران (Furan) والثيوفين (Thiophene) وغيرها.
– ومن المركبات المعروفة يمكن أن نورد الصيغ الكيميائية الآتية لتوضيح القليل من الاحتمالات العديدة.
– وسبب كون عناصر الأكسجين والكبريت والنتروجين ذات قدرة كبيرة على تكوين مركبات حلقية غير متجانسة أن زاوية تكافؤ هذه العناصر قريبة جداً من زاوية تكافؤ الكـربـون وعلى هذا يمكن لهذه الذرات أن تحل محل ذرة واحدة أو أكثر من ذرات الكربون في حلقة ما، دون أن تؤدي إلى توتر ملحوظ.
مصادر المركبات الحلقية غير المتجانسة وأهميتها
– أغلب المركبات العضوية غير المتجانسة تستخلص من مصادر حيوانية أو نباتية. ولها أهمية حيوية كبيرة حيث تدخل في صناعة كثير من الأدوية.
– تلعب تلك المركبات دوراً مهماً في بعض العمليات الحيوية ولذلك تستحق الكثير من الدراسة والبحث.
– من المركبات العضوية غير المتجـانسـة القلويدات مثل الكوكايين والكونين والنيكوتين والمبيدات الحشرية التي يمكن أن تحضر بطريقة عملية، كما أنها تدخل في بعض الصناعات مثل النايلون المستخدم في صناعة الملابس بالإضافة إلى عدد من الفيتامينات مثل فيتامين C
–على العموم فإن معرفة كيمياء المركبات غير المتجانسة لها أهمية كبيرة في مجال دراسة المنتجات الطبيعية والتحضيرات الحيوية وعمليات الأيض الدوائية.
– يمكن تحضير هذه المركبات وكثير غيرها في المختبرات الكيميائية حيث إن المركبات الحلقية غير المتجانسة تستخدم في صناعة العقاقير الطبية والأصباغ عديدات الأجزاء.
– تمثل المركبات الحلقية غير المتجانسة المجموعة الفعالة في كثير من الإنزيمات والإنزيمات المساعدة (Co-enzymes). وأخيرا تعزى الوراثة لارتباط ست حلقات أو أكثر الحلقات غير المتجانسة بالسلاسل الطويلة للحموض النووية.
تسمية المركبات الحلقية غير المتجانسة Nomenclature of Heterocyclic Compounds
إن كثيراُ من المركبات الحلقية غير المتجانسة تُعرف بأسمائها الشائعة مما يجعل من الصعب على الكيميائي أن يتذكر جميع الأسماء مما إلى وجوب إيجاد طريقة نظامية لتسميتها.
– ولذلك فإن الاتحاد الدولي للكيمياء البحتة والتطبيقية (IUPAC) بوضع نظام عالمي متفق عليه لتسمية هذه المركبات، وهذا ما سوف نقوم بشرحه لكل من المركبات أحادية الحلقة والمركبات الحلقية عديدة الحلقات غير المتجانسة والتي تملك ذرة أو أكثر غير الكربون.
وعلى العموم فسوف نرى أن تسمية المركبات أحادية الحلقة غير المتجانسة سهلة ومباشرة. أما مع المركبات غير المتجانسة عديدة الحلقات فإن هناك بعض الاستثناءات التي سوف نذكرها في حينه.
أولاً/ تسمية المركبات غير المتجانسة أحادية الحلقة
– لقد اتبع النظام الدولي ( IUPAC) في تسمية مثل هذه المركبات طريقة سهلة وبسيطة حيث وضع لكل منها اسماً يصف أي مركب من حيث:
- حجم الحلقة.
- عدد الذرات غير المتجانسة.
- نوع الذرات وموقعها.
- تحديد درجة التشبع في الحلقة.
– ويمكن تلخيص القواعد العامة للتسمية كما يلي:
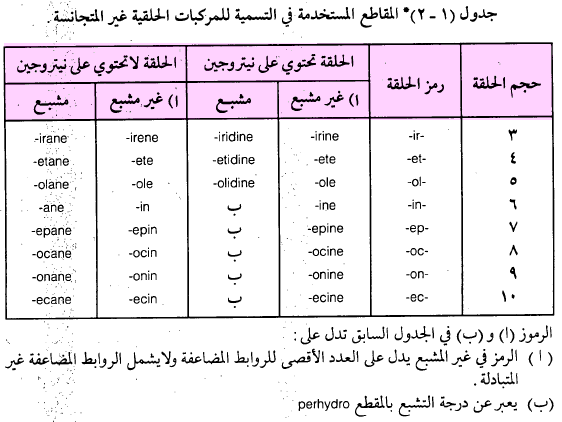
(1) يرمز لكل حلقة من الحلقات التي تحتوي على 3، 4، 5، 6، ۷، ۸، ۹، ۱۰ ذرات برمز يدل عليها وهذه الرموز هي ec, on, oc, ep, In, ol, et, ir على التوالي (جدول 1-2)
(2) حيث إن لكـل ذرة غير متجانسة رمزاً يدل عليها كما هو مبين في جدول (۱۱) فإن رمـز الـذرة يوضع في مقدمة (Prefix) الاسم للدلالة على نوع الذرة غير المتجـانسـة المـوجـودة في المركب مثل oxa للدلالة على الأكسجين وthia للدلالة على الكبريت وaza للدلالة على النيتروجين.
(3) إذا وجدت أكثر من ذرة غير متجانسة فإن مقدمة الاسم يجب أن تدل على ذلك. فعلى سبيل المثال إذا وجدت ذرتا أكسجين نضع dioxa في المقـدمـة وإذا وجـدت ذرتـا كبريت نضع المقطع dithia وإذا وجدت ذرتا نيتروجين فإننا نضع المقطع diaza في مقدمة الاسم.
(4) إذا كانت الذرتان غير المتجانستين مختلفتين فإننا نضع في مقدمة الاسم رمز كلتا الذرتين على أن يأتي المقطع الذي يدل على ذرة الأكسجين قبل ذلك الذي يدل على الكبريت وهذا بدوره يأتي قبل ذلك الذي يدل على النتروجين. فالمقطع oxaza يشير إلى وجود ذرة أكسجين وذرة نتروجين وthiaza يشير إلى وجود ذرة كبريت وذرة نيتروجين.
(5) يمكن التعرف على حالة التشبع في المركب غير المتجانس أحادي الحلقة من المقطع الذي يوضع في آخر اسمه (Suffix) كما هو موضح في جدول (١-٢) وقد وضعت هذه المقاطع طبقاً لحجم الحلقة.
– ويمكن ملاحظة من جدول (۱ – ۲) أن المركبات قد قسمت إلى قسمين إحداهما تحمل نيتروجين وهذه لها مقاطع خاصة تدل على حالة التشبع من عدمه والثانية لا تحتوي على نيتروجين وهذه لها مقاطعها الخاصة. أما إذا كان المركب مشبعا جزئياً فإنه يمكن استعمال المقـاطـع التالية dihydro, etc tetrahydro, قبل بداية الاسم أو بوضع رمز الهيدروجين H مسبوقاً برقم يدل على موضع التشبع وذلك قبل اسم المركب غير المشبع.
(6) ترقيم الحلقات الأحادية غير المتجانسة
عنـد ترقيم الحلقات الأحادية غير المتجانسة يبدأ الترقيم من الذرة غير المتجانسة أي أنها تأخذ الرقم (1) وفي حالة وجود ذرة غير متجانسة أخرى أو وجود مجموعة بديلة على الحلقة نفسها فإن اتجاه الترقيم يتم بحيث تأخذ هذه الذرات أو المجموعات أصغر عدد ممكن بعد الرقم (1).
– وإذا وجدت ذرتان غير متجانستين فإن الأفضلية في إعطاء الرقم الأصغر يكون لذرة الأكسجين ثم الكبريت ثم النتروجين.
وبذلك يمكن تطبيق القـواعـد السابقة على المركبات الحلقية الأحادية غير المتجانسة التي يمكن أن تصنف إلى:
(أ) مركبات النيتروجين الحلقية غير المتجانسة.
(ب) مركبات الأكسجين الحلقية غير المتجانسة.
(جـ) مركبات الكبريت الحلقية غير المتجانسة.
(د) المركبات الحلقية غير المتجانسة والتي تحتوي على ذرتين غير متجانستين.
(أ) مركبات النيتروجين الحلقية غير المتجانسة.
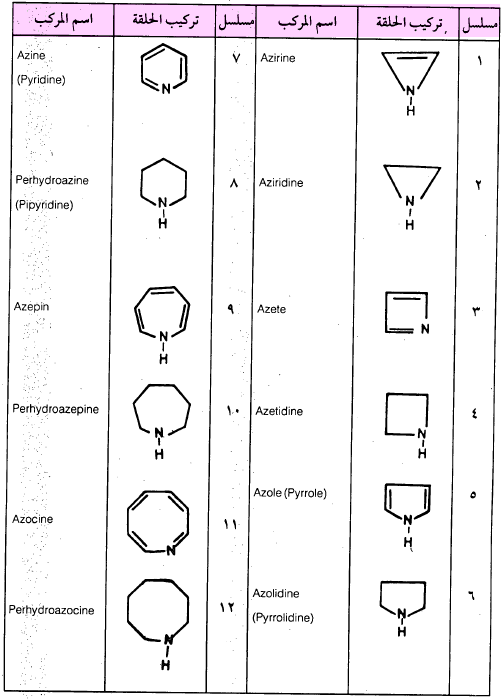
الحلقات الثلاثية وحتى الثمانية والتي تحتوي على ذرة النتروجين كذرة غير متجانسة موضحة اسماؤها المشتقة حسب النظام الدولي ( IUPAC) وكذلك أسماؤها الشائعة في جدول (1-3) في الحالتين عندما تكون في أقصى درجة من التشبع وكذلك عندما تكون في أقصى درجة من عدم التشبع.
هذا وقد وضعت الأسماء الشائعة لهذه المركبات بين قوسين، وعلى العموم فإن كثيراً من هذه المركبات تعرف بأسمائها الشائعة.
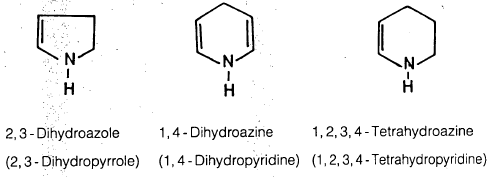
أما في حالة المركبات غير المتجانسة المشبعة جزيئاً فإنه يمكن تسميتها كما يلي:
(ب) مركبات الأكسجين الحلقية غير المتجانسة
– إذا طبقنا القواعد السابقة على هذه المركبات فإننا نجد أن:
- الحلقات الثلاثية غير المشبعة تسمى أكسيرين Oxirene والمشبعة تسمى اكسيران Oxirane
- والحلقات الرباعية غير المشبعة تسمى أكسيت Oxete والمشبعة تسمى أوكسيتين Oxetane ،
- الحلقات الخماسية غير المشبعة فتسمى أوكسـول Oxole ولها اسم شائع هو الفيوران (Furan) وهو أكثر شهـرة. والمشبعـة تسمى أكســولــين Oxolane والأخير يشتهر بالاسم الشـائع تتراهيدروفيوران Tetrahdrofuran
- الحلقات السداسية غير المشبعة أوكسين Oxin والاسم الشائع هو بيران أما المشبع فيسمى بيرهيدروكسين Perhydroxin.
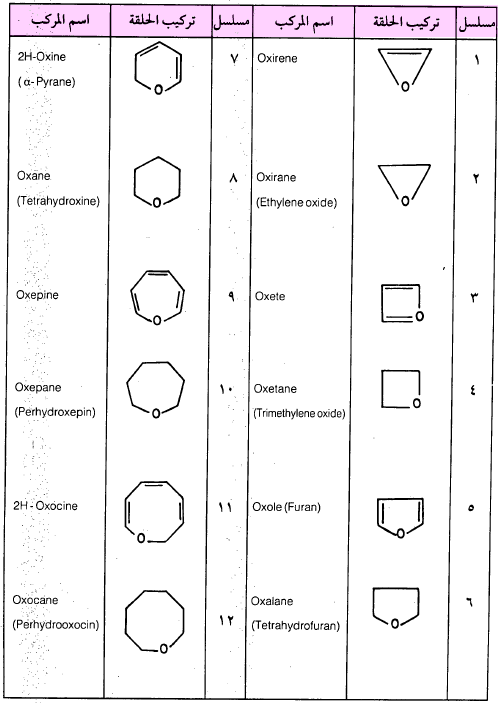
– جدول (١-٤) يوضح بعضاً من تلك المركبات وأسمائها النظامية، أما الأسماء الشائعة فقد وضعت بين قوسين.
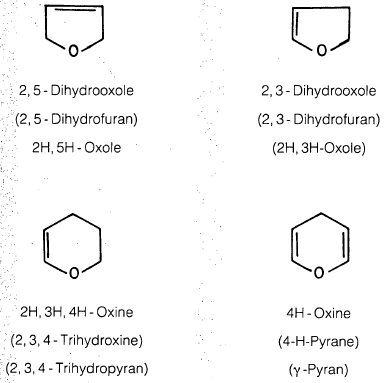
– يمكن تسمية المركبات غير المتجانسة المشبعة جزئياً، والتي تحتوي على الأكسجين كما يلي:
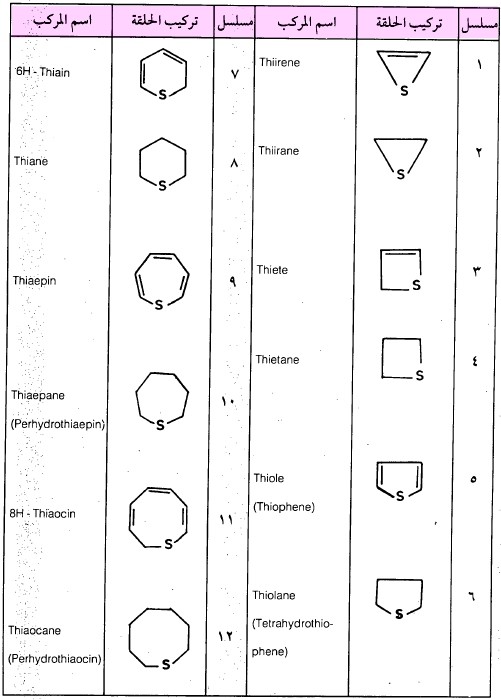
(جـ) مركبات الكبريت الحلقية غير المتجانسة.
– إذا طبقنا قواعد التسمية الدولية على هذه المركبات نجد أن:
- الحلقة الثلاثية غير المشبعة تسمى ( Thiirene) أما المشبعة منها فتسمى ( Thiirane)
- والحلقات الرباعية غير المشبعة تسمى المشبعة تسمى (Thiete) والمشبعة ( Thietane)
- والحلقات الخماسية غير المشبعة تسمى ( Thiole) والمشبعة منها (Thiolane)
– وهكذا كما هو مبين في الأمثلة التالية الموضحة في جدول (1 – 5)، الأسماء بين قوسين أسماء شائعة.
– أما المركبات غير المتجانسة المشبعة جزئياً فتسمى كما يلي:
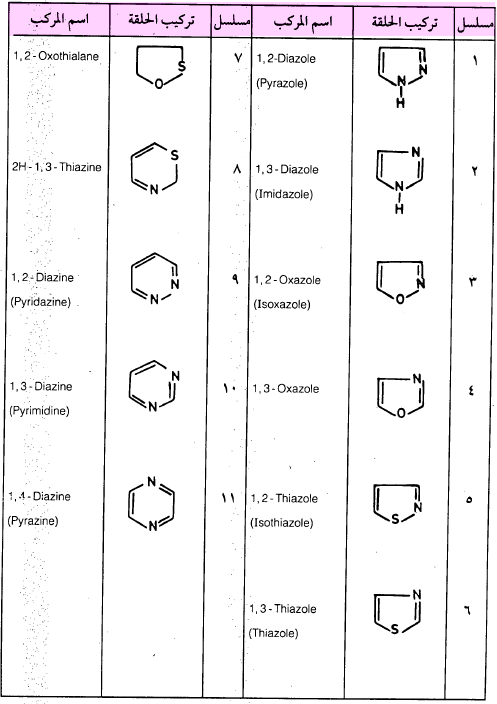
(د) المركبات الحلقية غير المتجانسة والتي تحتوي على ذرتين غير متجانستين.
– تسمى هذه المركبات طبقاً للقواعد السابقة ولذلك تستخدم المقاطع التي توضع في مقدمة الاسم والتي تدل على عدد الذرات فإذا وجدت ذرتا أكسجين نضع المقطع dioxa حيث di تدل على اثنين وoxa تدل على الأكسجين.
– كذلك الحال في حالة وجود ذرتي كبريت نضع المقطع dithia وفي حالة النيتروجين نضع المقطع diaza وهكذا . . .
– أما إذا وجدت ذرتان مختلفتان فإن الأسبقية تكون للأكسجين ثم الكبريت ثم النيتروجين فإذا وجدت ذرتا أكسجين ونيتروجين نضع المقطع oxaza وإذا وجدت ذرتا كبريت ونيتروجين نضع المقطع thiaza وهكذا.
– يتضح من الأمثلة التالية الموضحة في جدول (1 – 6) وفي هذا الجدول وضعت الأسماء الشائعة بين قوسين.
ثانياً/ تسمية المركبات غير المتجانسة عديدة الحلقات
على الرغم من الصعوبات التي تواجه تسمية مثل هذه المركبات إلا أنه يمكن اتباع الخطوات التالية في تسميتها:
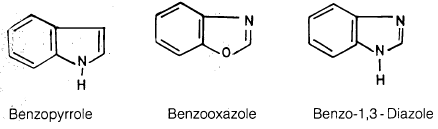
(1) في المركبات غير المتجانسة عديدة الحلقة يؤخذ اسم الحلقة غير المتجانسة على أساس أنه المركب الأم ويسبقه اسم الحلقة المتكاثفة معه.
ومن الأمثلة على ذلك:
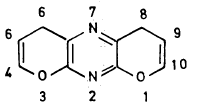
(2) إذا وجدت في مثل هذه المركبات أكثر من حلقة غير متجانسة فإن الحلقة التي تحتوي على النتروجين تعطي الأقدمية تليها تلك التي تحتوي على الأكسجين وهذه تسبق تلك التي تحتوي على الكبريت.
ويجب ملاحظة أنـه عنـد الترقيم فإن الأكسجين تأخذ الرقم الأصغر. ومن الأمثلة على ذلك:
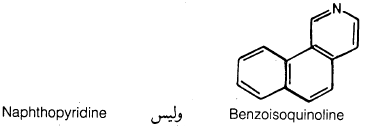
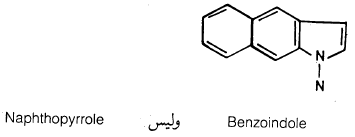
(3) يؤخذ الاسم البسيط والذي يمثل الجزء الأكبر في الصيغة التركيبية للمركب غير المتجانس والذي يحتوي على الحلقة غير المتجانسة على أنه المركب الأساسي. مثل:
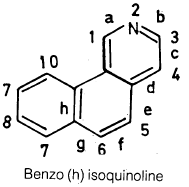
(4) وعلى العموم فإن اسم المركب السابق Benzoisoquinoline لا يُعرف المركب بصورة كاملة ولذلك فإنه من الضرورة بمكان أن يوضع في الاسم ما يدل على موضع اتصال الحلقات، ولذلك فإنه يمكن إعطاء أضلاع المركب الأم Isoquinoline حروفاً تدل عليها بدءاً بالرابطة التي تقع بين الذرتين ١ و٢ كما هو موضح أدناه.
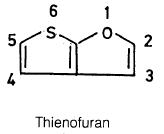
ويعني هذا الاسم أن مجموعة Benzo تكون متكاثفة مع الرابطة (h) ولذلك فإن اسـم المـركـب Benio (h) isoquinoline هو الـصـحـيـح ومن الأمثلة الأخـرى مرکب Thienofuran
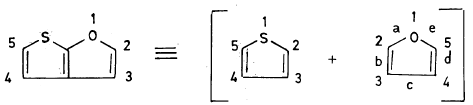
فهذا الاسم غير وافي وذلك لأن موضع التحام الحلقات غير موضح لأي من الحلقتين ولذا نلجأ إلى تجزئة المركب وترقيم كل حلقة وإعطاء أضلاعها حروفا مناسبة كما هو موضح أدناه.
وبذلك يصبح اسم المركب السابق Thieno [ 2, 3 -b] furan
ومن الأمثلة الأخرى:
(5) عند ترقيم أضلاع مركب عديد الحلقات يجب اتباع الخطوات الآتية:
(أ) يجب أن يكون أكبر عدد ممكن من الحلقات ممتداً على محور أفقي.
(ب) عند وجود حلقات أخرى غير التي على المحور الأفقي يجب أن تكون في أعلى المحور الأفقي وعلى يمينه.
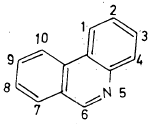
(جـ) يبدأ الترقيم من الحلقة أعلى المحور وعلى اليمين. ويتجه الترقيم باتجاه عقارب الساعة مع عدم ترقيم اتصال الحلقات كما هو مبين أدناه.
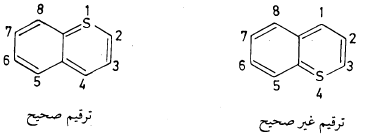
(هـ) يجب أن يعطي الترقيم الذرة غير المتجانسة أصغر عدد ممكن كما هو موضح في المثال التالي:
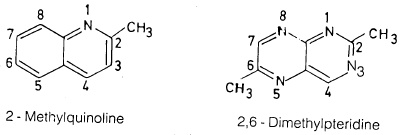
ومن الأمثلة الأخرى على القواعد السابقة ما يلي:
– وطريقة التسمية الدولية مهمة جداً إلا أن أغلب المركبات غير المتجانسة عديدة الحلقات لها أسماء شائعة.
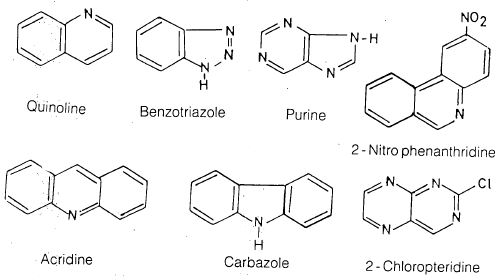
– ومن المركبات الحلقية غير المتجانسة الأمثلة التالية:
المراجع: كتاب المركبات الحلقية غير المتجانسة والحيوية للدكتور حمد بن عبدالله اللحيدان والدكتور محمد بن إبراهيم الحسن والدكتور سالم سليم الذياب – الطبعة الثانية – جامعة الملك سعود – المملكة العربية السعودية









دمتم موفقين إن شاء الله
بارك الله فيك وجزاك الله خيرا