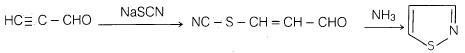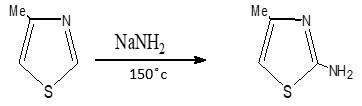الحلقات الخماسية ذات ذرتين غير متجانستين
الحلقات الخماسية ذات ذرتين غير متجانستين
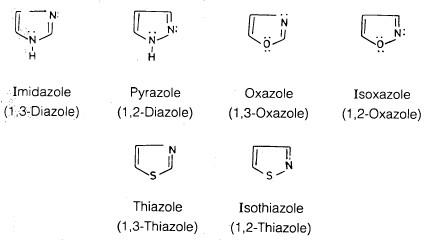
– تسمى الحلقات الخماسية ذات ذرتين غير متجانستين بالأزولات
– الأزولات وهي مركبات ذات الحلقات الخماسية الأضلاع ولها صفات أروماتية.
– وتحتوي على ذرتين مخالفتين غير ذرات الكربون قد تكونان متشابهين أو غير متشابهين.
– وهذه الذرات غير المتجانسة قد تكون النتروجين أو الأكسجين أو الكبريت أو اثنتين من أي منها. وهي قد توجد في وضع متجاور أو في وضع متبادل.
– وهذه المركبات أكثر مقاومة للحموض عند درجة حرارة الغرفة من مثيلاتها أحادية الذرة غير المتجانسة، ويعزى ذلك إلى وجود الذرة غير المتجانسة الأخرى.
– أمثلة على الحلقات الخماسية ذات ذرتين غير متجانستين.
وسوف يتم مناقشة كل الحلقات الخماسية السابقة بالتفصيل في هذا الموضوع.
أولاً/ البيرازول والإيميدازول Imidazole and Pyrazole
– البيرازول والإيميدازول أحدى الحلقات الخماسية ذات ذرتين غير متجانستين.
– البيرازول والإيميدازول كل من هذين المركبين عبارة عن حلقة خماسية تحتوي على ذرتين غير متجانستين هما النيتروجين.
– فالبيرازول عبارة عن 1 ، 2 داي أزول (1,2Diazole).
– أما الإيميدازول فهو عبارة عن 1، 3 داي أزول (1,3Diazole).
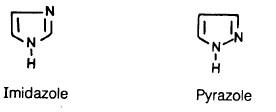
(أ) طرق تحضير البيرازول والإيميدازول
(1) تحضير البيرازول preparation of Pyrazole
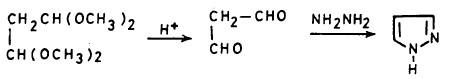
يمكن تحضير البيرازول بسهولة من مادة متوفرة تجارياً هي 3،3،1،1 رابع ميثوكسي بروبان حيث تتحلل في الوسط الحمضي إلى مالونالدهید (Malonaldehyde) الذي يتفاعل بدوره مع الهيدرازين ويعطي البيرازول كما هو موضح بالمعادلة التالية:
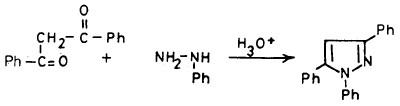
هذا ويمكن تحضير مشتقات البيرازول عنـد معـاملة 3،1 ثنـائي الكربونيل مع الهيدرازين أو مشتقاته كما يتضح من المعادلة التالية:
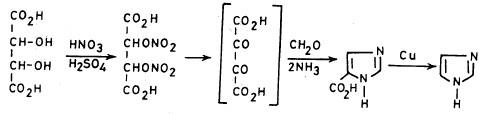
(2) تحضير الإيميدازول preparation of Imidazole
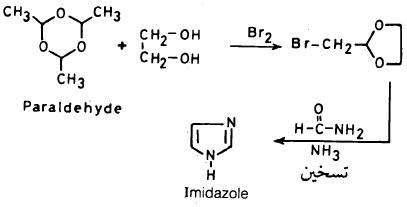
كما يمكن أن يحضر الإيميدازول من البارالدهيد حيث إنه يتفاعل مع البروم في وجود إثيلين جيلكول ويتحول إلى أسيتال حلقي من برومواستالدهيد وهذا عند تسخينه مع الفورماميد في وجود الأمونيا يتحول إلى إيميدازول .
كما يوجد هناك طرق أخرى لتحضير الإيميدازول حسب ما هو موضح بالطريقة التالية:
(ب) خواص البيرازول والإيميدازول
(1) البيرازول والإيميـدازول عبارة عن مركبات صلبة بلورية.
(2) البيرازول ينصهر الأول على 70°م والإيميدازول عند 90مo
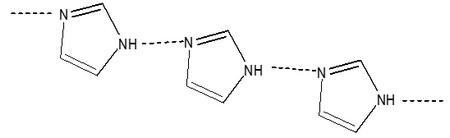
يرجع الاختلاف في درجة انصهارهما إلى أن جزيئات الايميدازول تترابط فيما بينها بروابط هيدروجينية وتشكل سلسلة يصل عدد الجزيئات المشتركة فيها نحو 20 فأكثر كما يوضح الشكل التالي:
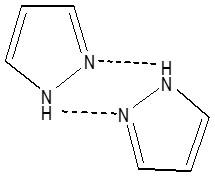
أما عند البيرازول فلا يقوم بهذا الدور إلا جزئيان فقط كما يوضح الشكل التالي:
(3) البيرازول والإيميدازول يذوبان في الماء ولكن لا يذوبان في إيثر البترول.
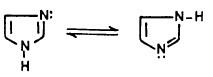
(4) البيرازول والإيميدازول عبارة عن مركبـات تـوتـومـيرية.
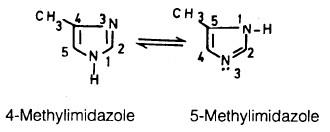
وذلك لأن ذرة الهيدروجين يمكن أن تتصل بأي من ذرتي النيتروجين وعليه فإن إحدى ذرات النيتروجين تشبه تلك التي في البريدين والأخرى التي تحمل الهيدروجين تشبه تلك التي توجد في البيرول كما يتبين ذلك من الاتزان التالي:
ولذلك فإن مشتقات هذه المركبات تعاني من صعوبة التسمية فإذا كان لدينا المركب التالي فيمكن أن يرقم كما يلي:
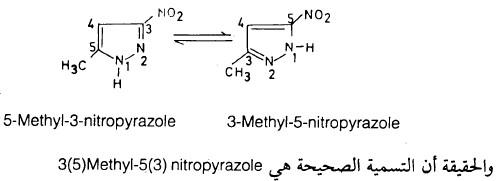
وعلى هذا فإنه غير صحيح أن يكون اسم المركب السابق 4- مثيل إيميدازول أو 5- مثيل إيميدازول لكن الاسم الصحيح هو 4 (5) ـ مثيــل ايميدازول وهذه القاعدة تنطبق على البيرازول كما يتضح من المثال التالي:
(5) البيـرازول والإيميدازول قواعد ضعيفة
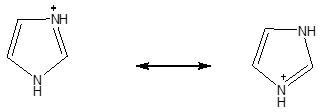
وعلى العموم فإن البيرازول والإيميـدازول عبارة عن قواعد ضعيفة مع العلم أن الإيميدازول أقـوى قاعـدية من البيرازول ومن البريدين.
(6) البيـرازول والإيميدازول لها خواص حمضية
وبالإضافة إلى خواصها القاعدية لها خواص حمضية حتى أن الإيميدازول أقوى حمضية من البيرول وأكثر ثباتاً منه في المحاليل الحمضية. وذلك بسبب التأثير التحريضي الناتج عن ذرة النيتروجين المشابهة لنتروجين البريدين.
(7) الخواص العطرية للإيميدازول والبيـرازول
أما الخواص العطرية للإيميدازول والبيرازول فتعكسها مقاومة هذه الحلقات لتفاعلات الأكسدة والإضافة وسهولة تفاعلات الاستبدال مع العوامل الإلكتروفيلية.
وتفاعلات الاستبدال تفضل موضع (4) في كلا المركبين. كما أن لكل منها تراكيب تأرجحية تساعد على ثباته.
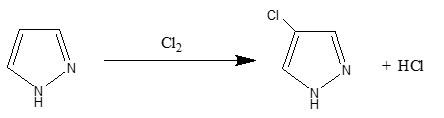
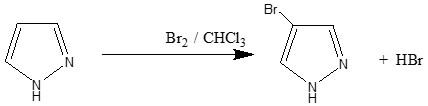
(أ) الهلجنة
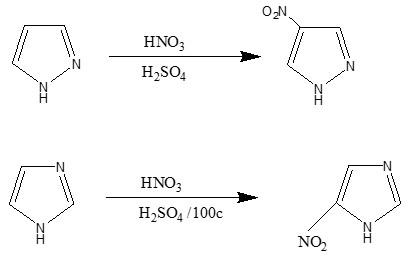
(ب) النيترة
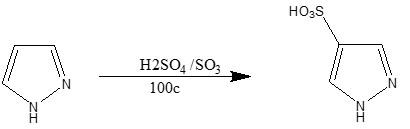
(جـ) السلفنة
(8) الخواص الكيميائية للايميدازول والبيرازول عبارة عن خليط من خواص كل من البريدين والبيرول.
– ومن ناحية أخرى يمكن القول إلى حد ما، إن الخواص الكيميائية للايميدازول والبيرازول عبارة عن خليط من خواص كل من البريدين والبيرول.
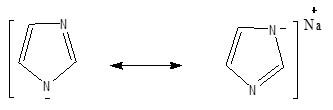
– وعلى ذلك فإن هذه المركبات تقوم بتكوين أملاح مع الحموض القوية كما هو الحال في البريدين وتتفاعل مع القواعد، مثل KOH كما هو الحال في البيرول.
(جـ) أهمية البيرازول والايميدازول
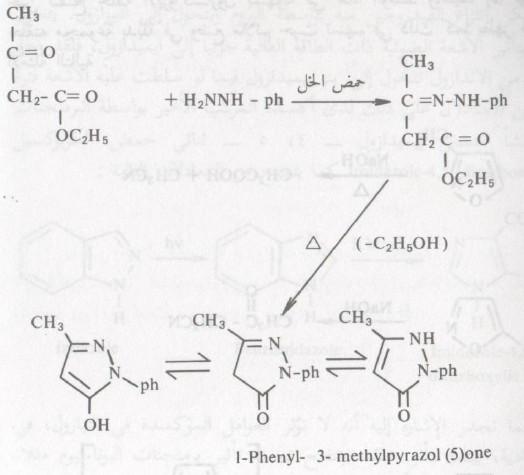
للبيرازول مشتقات مهمة في مجال المواد الطبية نذكر منها مركب أنتيبايرين Antipyrin الذي يحضر بمعاملة إستر أسيتواسينات Acetoacetic ester بالفينيل هيدرازين في وسط حمض الخل حيث يتكون في باديء الأمر مشتق الهيدرازون الذي يتحول بالتسخين إلى حلقة البيرازول المطابقة بأشكال ثلاثة كما يظهر من المعادلات التالية:
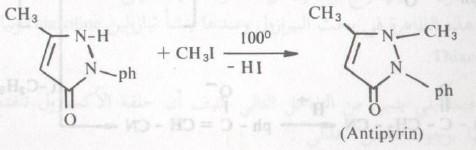
مثيلة مشتق البيرازول يؤدي إلى المركب المعروف أنتيبايرين Antipyrin كما هو موضح كالتالي:
Antipyrin أنتيبايرين
هو مركب عبارة عن:
- مركب صلب يذوب في الماء والكحول
- له طعم يأخذ محلوله المائي اللون الأحمر البني عند معاملته بكلوريد الحديديك FeCl3.
- درجة انصهاره ۱۱۳°م
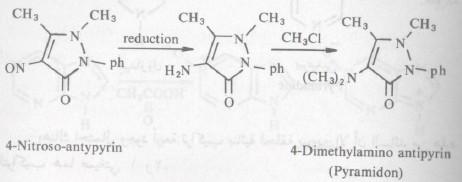
يتفاعل مع حمض النيتروز حيث يتكون مركب 4-نیتروزو أنتيبایرین 4Nitroso-antipyrin الذي يختزل بسهولة إلى الأمين المطابق، هو الأخير إذا ماعومل بكلوريد المثيل فإنه ينتج المركب المعروف باسم بامير اميدون Pyramidon كما يلي:
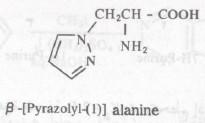
إن لكل من أنتيبايرين وبايراميدون و Pyramidon مركبات أخرى شبيهة لهما البنية التركيبية، مركبات تستخدم كعقاقير لتخفيف الحمى وعلاج الاضطرابات العصبية وعلاج الروماتزم. والجدير بالذكر أن هناك مشتق آخر للبيرازول متوفر في بذور ثمار البطيخ يساعد على النوم وله الصيغة التالية:
– إن حلقة الايميدازول لا تقل شأناً مشتقات البيرازول وعلى الأخص من الناحية البيولوجية.
– إن حلقة الايميدازول هي جزء من تركيب قاعدة حلقية غير متجانسة لها أهميتها البيولوجية وتعرف بحلقة البيورين Purine.
– هذا وتلعب قاعدية الإيميدازول دوراً هاماً فى العمليات البيولوجية حيث توجد هذه الحلقة في الحمض الأميني هيستدين الذي يعمبل كمتقبل للبروتون فى الأنزيمات.
ثانياً/ الأوكسازول والأيزواكسازول Oxazole and Isoxazole
– الأوكسازول والأيزواكسازول أحدى الحلقات الخماسية ذات ذرتين غير متجانستين.
– الأوكسازول والأيزواكسازول مركبان عبارة عن حلقة خماسية تحتوي على ذرتين غير متجانستين هما النيتروجين والأكسجين.
– الأيزوإكسازول عبارة عن 1 ، 2 أوكسازول 1,2Oxazole
– والأوكسازول عبارة عن 1 ، 3 أوكسازول 1,3Oxazole

(أ) تحضير الأوكسازول والأيزواكسازول
تحضير الأكسازول Preparation of Oxazole
يحضر الأكسازول من الطرق الآتية:
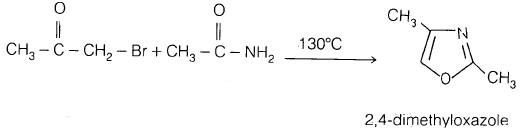
(1) تفاعل الأسيتاميد وبرومو أسيتون
يحضر الأوكسازول أو أحد مشتقاته من تفاعل ألفا ـ هالوجين كيتون α-halogen ketone مثل بروموأسيتون مع أميد الحمض acid amide مثل الأسيتاميد ليعطي 2 ، 4 – ثنائي مثيل أوكسازول ، كما يتضح من المعادلة التالية:
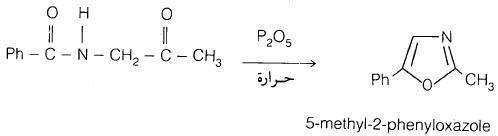
(2) نزع الماء من مركبات 1 , 4 – ثنائي مجموعة الكربونيل
كما يتضح من المعادلة التالية:
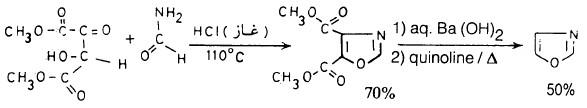
(3) نزع مجموعة الكربوكسيل Decarboxylation من المركب الـوسـطي 5،4 – كربونيل ثنائي الميثوكسي (4,5Dimethoxy carbonyl)
كما يتضح من المعادلة التالية:
تحضير الأيزواكسازول Preparation of Isoxazole
يحضر مشتق الأيزواكسازول من:
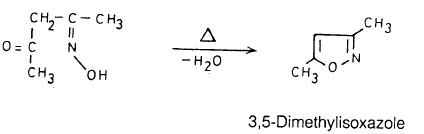
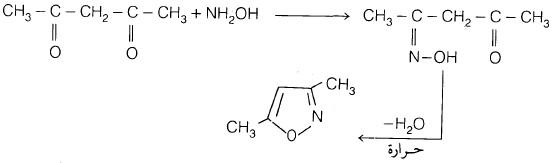
(1) تسخين أسيتيل أسيتون أكزيم
كما يتضح من المعادلة التالية:
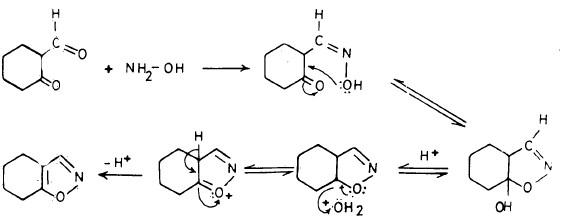
(2) معاملة 3،1 ثنائي الكربونيل بهيدروكسيل أمين
يمكن تحضير هذا المركب من تفاعل هيدروكسيل أمين مع مركب 1 , 3 ثنائي مجموعة الكربونيل بحيث يعطي أحادي أوكسيم مركب 1 , 3 مجموعة الكربونيل.
وهذا يتم نزع جزئ ماء منه عن طريق التسخين كما يلي:
أو كما بالمعادلة التالية:
(ب) خواص الأوكسازول والأيزواكسازول Properties of Isoxazole and Oxazole
(1) الأيزواكسازول والأوكسازول كلاهما مركب سائـل وله رائحة تشبه رائحة البريدين.
(2) لم يحظ هذان المركبان باهتمام كبير إلا في السنوات الأخيرة.
(3) الأيزواكسازول والأوكسازول لها صفات قاعدية ضعيفة ، وهما أضعف قاعدية من البريدين والسبب في ذلك وجود ذرة الأكسجين ذات الكهروسالبية العالية ولكل منها تراكيب تأرجحية تساعد على ثباتها.
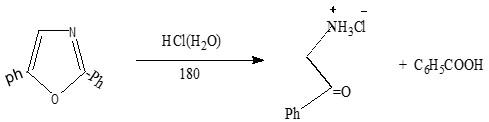
(4) الأيزواكسازول والأوكسازول أكثر ثباتاً من الفيوران تجاه الأحماض المركزة عند درجة الحرارة العادية أما عند درجة الحرارة العالية فإنها تنفتح. كما يتضح من المعادلة التالية:
(5) الأيزواكسازول والأوكسازول لهم القدرة على تكوين أملاح رباعية (Quaternary salt) مع عوامل الألكلة.
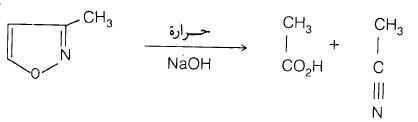
(6) في الوسط القاعدي فأن الأوكسازول ثابت، أما الايزوأوكسازول فإنه ينفتح بكل سهولة وسهولة الإنفتاح تعتمد على المجاميع البديلة. كما تبين المعادلة:
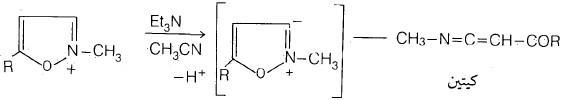
(7) تستطيع هذه المركبات تكوين أملاح رباعية يمكن ان تتفاعل بدورها مع القواعد وتعطي (كيتين إيميد)، وهذا يمكن أن يستخدم في تحضير كثير من المركبات مثل الببتيدات والأحماض الأمينية. كما يتضح من المعادلة التالية:
(8) تفاعل ديلز- الدر Diels -alder reaction
يخضع الاوكسازول لتفاعل ديلز – الدر حيث انه يتفاعل مع الدائيينوفيل.
يستخدم هذا التفاعل لتحضير مركبات حلقيه غير متجانسة.
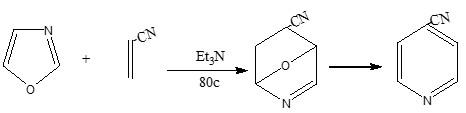
فمثلاً تفاعل الاوكسازول مع الاكريلونيتريل يمثل طريقه عمليه لتحضير مشتقات البيريدين. كما يتضح من المعادلة التالية:
ثالثاَ/ الثيازول والأيزوثيازول Thiazole and Isothiazole
– الثيازول والأيزوثيازول أحدى الحلقات الخماسية ذات ذرتين غير متجانستين.
– الثيازول والأيزوثيازول عبارة عن مركبات ذات حلقة خماسية ذات ذرتين غير متجانستين هما الكبريت والنيتروجين.
– أما الثيازول فهو عبارة عن 3,1 ثيازول (1,3thiazole)
– فالأيزوثيازول عبارة عن 2,1 ثيازول (1,2thiazole)
(أ) طرق تحضير الثيازول والايزوثيازول Thiazole and Isothiazole
تحضير الثيازول Preparation of thiazole
أن الطرق المستخـدمـة في تحضير الثيازول فهي طريقة هانتـزش (Hantzch method).
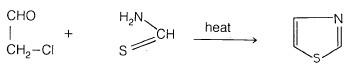
– تتضمن هذه الطريقة تسخين ألفا – هالوجين ألدهيد أو كيتون (مثل: كلوراسيتالدهيد) مع الثيامد (مثل: الثيوفورماميد) كما في المعادلة التالية:
تحضير الأيزوثيازول Preparation of isothiazole
– يحضر الأيزوثيازول من البروباينات وأيزوثيوسيانيد الصوديوم NaSCN في وجود النشادر وعامل مساعد.
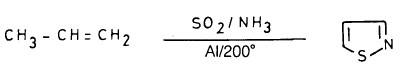
– ويحضر أيضا من تفاعل البروبلين مع ثاني أكسيد الكبريت والأمونيا وباستخدام عامل مساعد كالألومنيوم عند درجة حرارة عالية. كما بالمعادلة التالية:
(ب) خواص الثيازول والايزوثيازول Thiazole and Isothiazole
– هذان المركبان عبارة عن قاعدة ضعيفة ذات رائحة ودرجة غليان تشبه تلك التي للبريدين ويمكن القول إلى حد ما إن خواصها الكيميائية هي خليط من خواص البريدين والثيوفين.
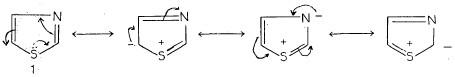
– ويتميز الثيازول بأنه قاعدة أضعف من البريدين له القدرة على تكوين أملاح مع الحموض القوية كما أنه يكون أملاحاً رباعية مع هاليدات الألكيل وهذه تتحلل في الوسط القاعدي (Decomposed) وهذا المركب له أشكال تأرجحية تساعد على استقراره يمكن توضيحها كما يلي:
والصيغة الأولى هي التي تمثل الثيازول بصـورة رئيسة.
تفاعلات الاستبدال الإلكتروفيلية
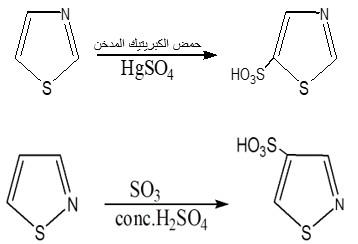
– وتتم تفاعلات الاستبدال الإلكتروفيلية في الموضع (5) وعندما يكون مشغولاً فإن عملية الاستبدال تتم في الموضع (4) كما في المعادلات التالية:
(1) السلفنة
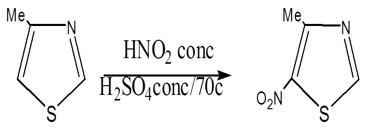
(2) النيترة
تفاعلات الاستبدال النيكلوفيلية
– أمـا تفاعلات الاستبدال النيكلوفيلية فإنها تتم في الموضع (2) فإذا كان مشغولاً فتتم في الموضع (5) كما بالمعادلة التالية:
والثيازول يقاوم بصفة عامة عمليات الاختزال وعمليات الأكسدة بواسطة حمض النيتريك إلا أنه عند معاملته بمحلول برمنجنات البوتاسيوم فغالباً تتكسر الحلقة.
(جـ) أهمية الثيازول والأيزوثيازول Importance of Thiazole and Isothiazole
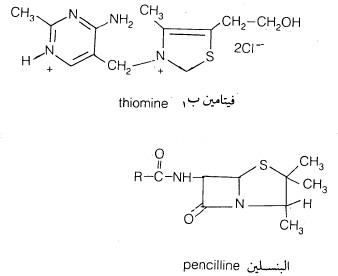
– يعتبر الثيازول مركباً ذا أهمية بيولوجية كبيرة وذلك أن البنسلين وفيتامين ب1 ومركب السلفاثيازول من أهم مشتقاته.
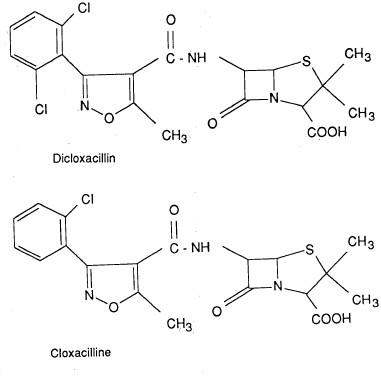
– أما الإيزوثيازول فإن الاهتمام به لم يكن كبيراً إلى زمن قريب. حيث ثبت أنه يدخل في تركيب العديد من البنسلينات كما هو واضح في مركب كلوكساسيلين Cloxacillin وداي كلوكساسيلين.
– وجدير بالذكر أن وجـود الايزوكسازول في هذه المركبات جعل هذا النوع من البنسلينات يقاوم حموضة المعدة ويقاوم بعض الإنزيمات البكتيرية ولذلك أصبح من الممكن أخذ مثل هذه الأدوية عن حلقة طريق الفم.
– كما أن من المشتقات الأخرى ذات النشاط الحيوي والتي تستعمل كمضادات حيوية مجموعة B-lactam antibiotic وهي تشمل البنسلينات وتركيبها في الغالب عبارة عن حلقة رباعية غير متجانسة Azetidinone ملتحمة مع حلقة خماسية Thiazolidine بالإضافة إلى مجموعة السيفالوسبورونات Cephalosporins حيث تركيبها الأساسي عبارة عن حلقة رباعية غير متجانسة Dihydrothiazine. هذا بجانب العديد من المضادات الحيوية التي تحتوي على حلقات غير متجانسة .
المراجع:
- كتاب المركبات الحلقية غير المتجانسة والحيوية للدكتور حمد بن عبدالله اللحيدان والدكتور محمد بن إبراهيم الحسن والدكتور سالم سليم الذياب – الطبعة الثانية – جامعة الملك سعود – المملكة العربية السعودية
- كتاب الكيمياء العضوية الأروماتية للدكتور محمد بن أبراهيم الحسن – الطبعة الأولى 1992م
- محاضرات 341 كيم كيمياء المركبات الحلقية غير المتجانسة Chemistry of Heterocyclic Compounds للدكتور عبدالله بن محمد الماجد – جامعة الملك سعود – السعودية
- كتاب الكيمياء العضوية للمؤلف د. حسن محمد الحازمي / الجزء الثاني