أسئلة وإجابات
-
مسائل محلولة على خواص الغازات Gas Properties – الجزء الثاني
في هذا الموضوع سوف نقدم لك عشر مسائل محلولة عن خواص الغاز المثالي. وتشمل المسائل أفكار رائعة ومتنوعة مع الحلول…
أكمل القراءة » -
مسائل محلولة على خواص الغازات Gas Properties – الجزء الأول
فى هذا الموضوع سوف نتطرق إلى (10) مسائل محلولة عن خواص الغازات بأفكار مختلفة وحلول بسيطة وطرق سهلة وفى موضوع…
أكمل القراءة » -
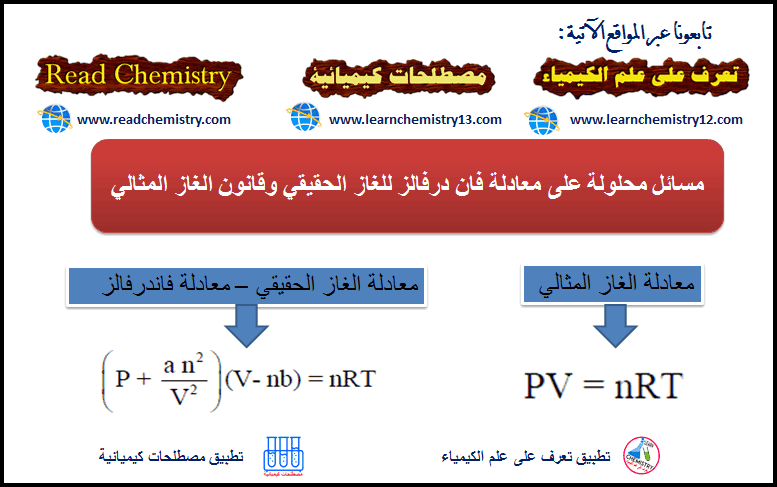
مسائل محلولة على معادلة فان درفالز للغاز الحقيقي وقانون الغاز المثالي
احسب الضغط الذي یؤدیه mol 1.0 من بخار الماء في حجم قدره 20.0 L عند Co 27.0 باستخدام: (أ) قانون الغاز المثالي…
أكمل القراءة » -
الطاقة الحرة Free Energy والإتزان الكيميائي
من أھم المعادلات في علم الثیرمودینامیك (الدینامیكا الحراریة) لربطھا ثابت التوازن للتفاعل (K) بالتغیر في الطاقة الحرة القیاسیة (ΔGo) هي…
أكمل القراءة » -
مسائل محلولة على العلاقة بين الإنثالبي والأنتروبي والطاقة الحرة
فى هذا الموضوع سوف نستعرض (8) مسائل بأفكار مختلفة على العلاقة بين الإنثالبي والأنتروبي والطاقة الحرة حيث قمنا بعرض الإجابات…
أكمل القراءة » -
السرعة الجزيئية Molecular Speed + مسائل محلولة
السرعة الجزيئية Molecular Speed ھي السرعات التي تتحرك بھا الجزیئات. وتعتمد فقط على درجة الحرارة (T) وعلى طبيعة الغاز المستخدم......
أكمل القراءة » -
الطاقة الداخلية ΔE والإنثالبي Enthalpy ΔH + مسائل محلولة
في هذا الموضوع سوف ندرس العلاقة بين الطاقة الداخلية والإنثالبي Internal Energy and Enthalpy ، وجدير بالذكر أننا قد تكلمنا في…
أكمل القراءة » -
مسائل محلولة على القانون الأول للديناميكا الحرارية
ينص القانون الأول للديناميكا الحرارية (قانون حفظ الطاقة): على أن الطاقة الكلیة لنظام معزول تظل ثابتة ویمكن تحول الطاقة من…
أكمل القراءة » -
الخواص الفيزيائية والخواص الكيميائية في الأحماض الكربوكسيلية
الأحماض الكربوكسيلية التي تحتوي على ذرة كربون من (1-4) تكون سوائل خفيفة. أما التي تحتوي على (5-9) ذرات كربون عبارة…
أكمل القراءة » -
مسائل محلولة على قانون جراهام للتدفق والانتشار
كنا قد تناولنا في الدرس السابق شرح قانون جراهام للتدفق والانتشار Graham’s Law of Diffusion and Effusion وفى هذا الدرس…
أكمل القراءة »