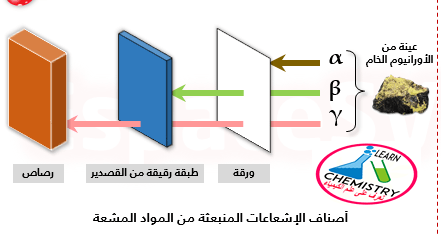
إخفاق الفيزياء الكلاسيكية فى تفسير الخطوط الطيفية الذرية
– في هذا الموضوع سيتم مناقشة إخفاق الفيزياء الكلاسيكية فى تفسير الخطوط الطيفية الذرية (نموذج بور لتفسير طيف ذرة الهيدروجين). وكيف كانت هذا الأخفاق واحد من أهم الاسباب فى ظهور ما يعرف بكيمياء الكم.
– كان الاعتقاد السائد عند بعض الفيزيائيين فى القرن التاسع عشر بأن التركيب النظري للفيزياء الكلاسيكية هي العلم الذي نما قبل 1900. ويتضمن ميكانيكا نيوتن الكلاسيكية ونظرية ماكسويل فى الكهربائية والمغناطيسية والأشعة الكهرومغناطيسية والديناميكا الحرارية ونظرية الحركية للغازات.
– ثم بعد ذلك أصبح العلم متكاملاً وبمقدوره إعطاء التفسير عن الظواهر الملحوظة ولكن فى الربع الأخير من هذا القرن، ظهرت نتائج عملية لم تتمكن نظريات الفيزياء الكلاسيكية من تفسيرها.
– وهذه النتائج العملية كانت تتعلق بظواهر ذرية وجزيئية. وقد حدا هذا الأمر آنذاك الباحثين إلى صياغة نظرية جديدة بإمكانها إعطاء تفسير مقبول منسجم مع النتائج العملية. هذه النظرية تسمي بنظرية الكم Quantum theory.
محتويات الموضوع
إخفاقات الفيزياء الكلاسيكية
– أخفقت الفيزياء الكلاسيكية فى تفسير المسائل المتعلقة بالظواهر الذرية والجزيئية وهي تتضمن كما يلي:
(1) اشعاع الجسم الأسود.
(2) التأثير الكهروضوئي.
(3) الخطوط الطيفية الذرية.
– في الموضوعات السابقة تم مناقشة ظاهرة إشعاع الجسم الأسود ، وكذلك ظاهرة التاثير الكهروضوئي، ولكن فى هذا الدرس سوف نتكلم فقط عن تفسير الخطوط الطيفية الذرية (نموذج بور لتفسير طيف ذرة الهيدروجين) ، وإخفاق الفيزياء الكلاسيكية فى تفسيرها.
الخطوط الطيفية الذرية
– عندما نضع غاز الهيدروجين في أنبوبة تحت ضغط مخلخل وتخضعه لتفريغ عالي الفولتية فسوف ينبعث ضوء.
– وعند مروره خلال منشور فسوف يتجزأ إلى سلسلة من الخطوط الطيفية كل منهما مرتبط بطول موجي أو تردد مختلف.
– ولم تتمكن النظرية الكلاسيكية من إعطاء قيم مضبوطة لترددات الخطوط الطيفية أو حتى قيم قريبة منها.
– وخلال الفترة من 1885 إلى 1910 توصل بالمر Balmer وريدبيرج Rydberg إلى إيجاد علاقة تجريبية تعطي الترددات المضبوطة لخطوط طيف الهيدروجين.
– ولم يوجد تفسير لهذه العلاقة التجريبية إلى أن جاء العالم بور عام 1913.
نظرية بور لتفسير الخطوط الطيفية الذرية
– بين العالم بور أن انبعاث ترددات معينة من الضوء من ذرات الهيدروجين يشير إلى أن ذرة الهيدروجين موجودة فقط فى حالات طاقية معينة.
– وبذلك فقد افترض بور الفروض الآتية :
(1) إن طاقة الهيدروجين توجد بشكل كمات، أي أن الذرة تتخذ طاقات منفصلة معينة فقط E3 , E2 , E1 , ……الخ.
– وقد سمى بور هذه الحالات المسموحة ذات الطاقة الثابتة بالحالات المستقرة stationary states للذرة (ولا يقصد بهذا التعبير على أن الإلكترون يكون عند سكون فى الحالة المستقرة).
(2) لا تنبعث من الذرة فى حالتها المستقرة أشعة كهرومغناطيسية.
(3) إذا حدث انتقال إلكترون من حالتها المستقرة Ea إلى أخري أقل طاقياً Eb فإن تردد الضوء المنبعث υ يعطى حسب قانون حفظ الطاقة كما يلي:
– وبصورة مشابهة يحدث انتقال إلكترون من حالة طاقية واطئة إلى أخرى أعلى طاقياً وذلك بامتصاص ضوء تردده معطى بالمعادلة (5-4).
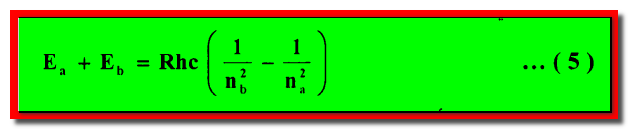
– والآن عند ربط معادلتي (3) ، (4) نحصل على المعادلة الآتية كما يلي:
– وهذه المعادلة تشير بقوة إلى أن طاقات الحالات المستقرة لذرة الهيدروجين التى تعطي بالمعادلة كما يلي:
(4) يتحرك الإلكترون في ذرة الهيدروجين في مدار دائري حول ويخضع لقوانين الميكانيكا الكلاسيكية.
– وأن طاقة الإلكترون تساوي حاصل جمع طاقته الحركية وطاقة جهد التجاذب الكهروستاتيكي بين إلكترون-نواة.
– ووفقاً للميكانيكا الكلاسيكية تعتمد الطاقة على نصف قطر المدار. وطالما أن الطاقة هي مكممة (أى موجودة بشكل مضاعفات لـ كم ثابت) لذا يوجد فقط مدارات معينة مسموحة وقد استخدم بور فرضية أخري لاختيار المدارات المسموحة.
(5) أن المدارات المسموحة هي تلك التى تكون لها عزم الإلكترون الزاوي كما يلي:
حيث أن: π2/h=ђ
m ، v هما كتله وسرعة الإلكترون
r هو نصف قطر المدار
…… ,n = 1,2,3,4
نتائج فرضيات بور
– ومع هذه الفرضيات تمكن بور من اشتقاق التعبير التالي لمستويات الطاقة فى ذرة الهيدروجين
– حيث e شحنة الإلكترون وعند مقارنة معادلتي (6)، (7) ينتج لنا المعادلة الآتية كما يلي:
– كما أنه عند التعويض عن قيم m ، e ، h ، c فإننا سنحصل على قيمة ثابت ويدبيرج R منسجمة مع قيمته التجريبية (العملية) وهو دليل على أن بور قد أعطي مستويات طاقته مضبوطة لذرة الهيدروجين.
موضوعات ذات صلة: (أضغط على الموضوع)
(1) إخفاق الفيزياء الكلاسيكية في تفسير ظاهرة إشعاع الجسم الأسود
(2) إخفاق الفيزياء الكلاسيكية في تفسير ظاهرة التأثير الكهروضوئي
المراجع : الفصل الأول ” مقدمة فى كيمياء الكم ” من كتاب مبادئ كيمياء الكم للمؤلف / محمد مجدي واصل أستاذ الكيمياء الفيزيائية – جامعة الأزهر – جمهورية مصر العربية .